Clear Sky Science · de
Zielgerichtete Eliminierung von Staphylococcus aureus‑Mastitisinfektionen mit synthetischen, phagenbasierten CRISPR‑Cas‑Übertragungssystemen
Kampf gegen eine kostspielige Milchvieh‑Infektion
Die Milch von Kühen und anderen Nutztieren kann durch eine schmerzhafte Gesäugeentzündung, Mastitis genannt, beeinträchtigt werden, die häufig durch das Bakterium Staphylococcus aureus verursacht wird. Die Behandlung dieser Infektionen erfordert in der Regel lange Antibiotikakuren, die kostspielig sind, Stress für die Tiere bedeuten und zur wachsenden Problematik der Antibiotikaresistenz beitragen. Diese Studie untersucht einen radikal anderen Ansatz: ein natürliches, virusähnliches Bakterienparasiten‑System in eine präzise Waffe zu verwandeln, die selektiv die DNA des Bakteriums zerschneidet und Infektionen beseitigt, ohne Resistenzen zu verbreiten.
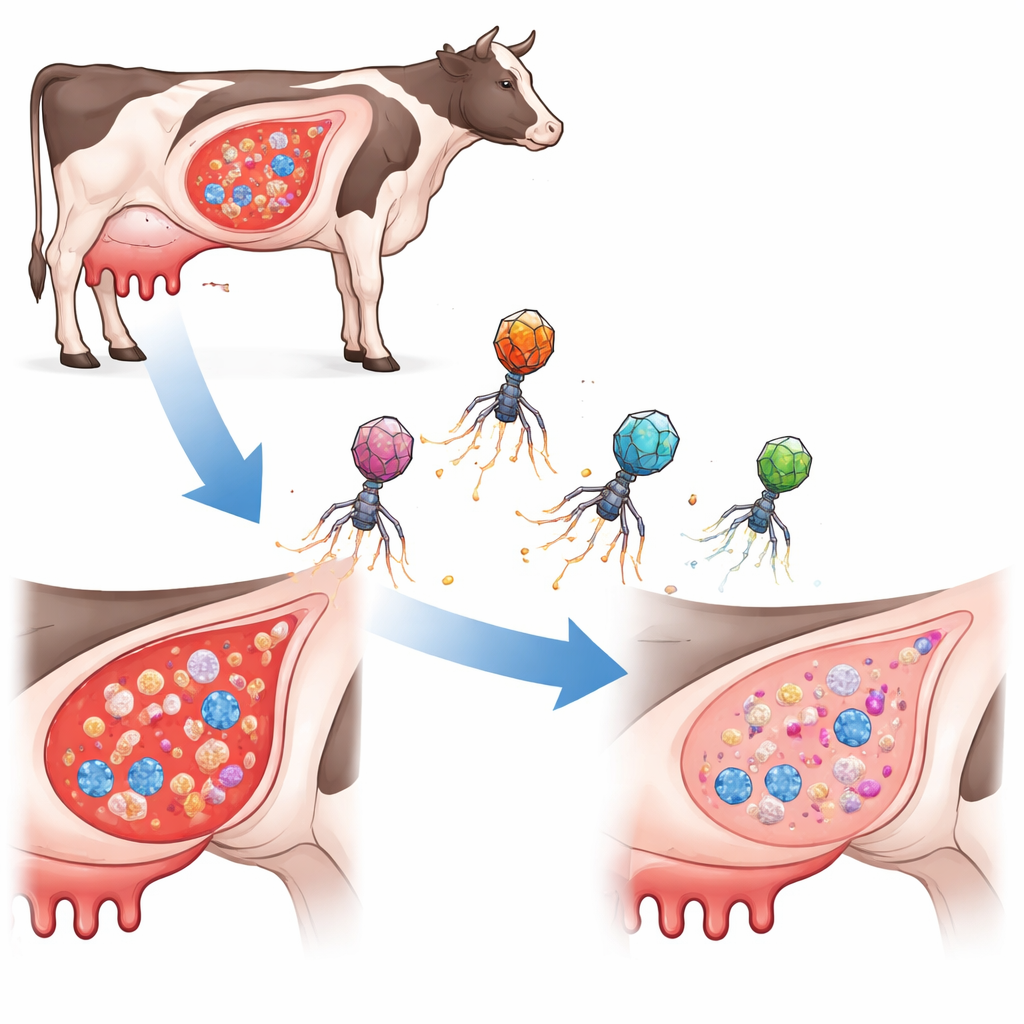
Ein neuer Typ gezielter Bakterienjäger
Anstatt traditionelle Antibiotika oder gewöhnliche Bakteriophagen (Viren, die Bakterien infizieren) zu verwenden, konstruierten die Forschenden winzige DNA‑tragende Elemente, sogenannte phageninduzierbare chromosomale Inseln. In der Natur nutzen diese Inseln Phagenhüllen, um zwischen Bakterienzellen zu springen. Hier bauten die Autorinnen und Autoren sie als „ePICIs“ neu auf, die das Geneditierwerkzeug CRISPR‑Cas9 sowie kurze Führungssequenzen tragen, die auf drei kleine, aber wichtige regulatorische RNAs von S. aureus zielen. Wenn ein ePICI in eine Zielzelle gelangt, wird Cas9 produziert und schneidet das Chromosom des Bakteriums an der gewählten Stelle, wodurch die Zelle von innen getötet wird. Entscheidend ist, dass diese konstruierten Partikel sich nicht eigenständig vermehren, was ihre Ausbreitung begrenzt und das Risiko der unbeabsichtigten Verbreitung schädlicher Gene verringert.
Wie der bakterielle Schutz die Auseinandersetzung verändert
S. aureus überlebt Behandlungen oft durch Bildung von Biofilmen – klebrigen Gemeinschaften, in denen Zellen in eine selbst erzeugte Matrix eingebettet sind. Das Team verglich zwei gängige Matrix‑Typen: eine, die hauptsächlich aus einem Protein namens Bap aufgebaut ist, und eine andere, die aus einem Zuckerpolymer bekannt als PIA/PNAG besteht. In Labortests schützten Bap‑reiche Biofilme die Bakterien stark gegen die ePICIs und gegen einen standardmäßigen Helferphagen, indem sie wie eine dichte Rüstung die Infektion blockierten. Im Gegensatz dazu machten Biofilme auf Basis des Zuckerpolymers die Bakterien leichter angreifbar, vermutlich weil Enzyme auf den Virushüllen diese Zucker zersetzen und den Partikeln helfen können, ihre Ziele zu erreichen.
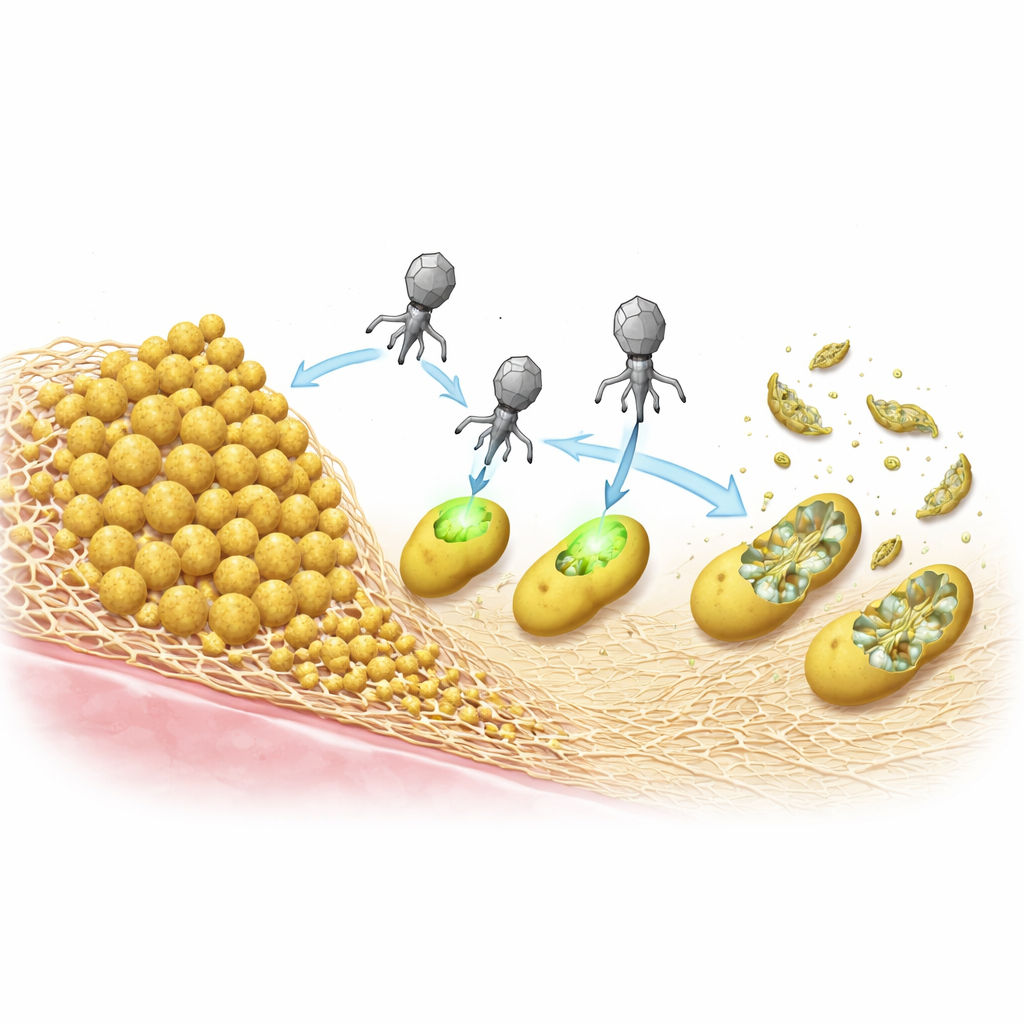
Bakterien töten, ohne sich in deren DNA einzuschreiben
Einmal in der Zelle können ePICIs ins bakterielle Chromosom integrieren, doch fragten die Forschenden, ob dieser Schritt tatsächlich für das Töten nötig ist. Sie erzeugten eine Version, die sich nicht mehr integrieren konnte, und zeigten, dass sie, solange das Partikel korrekt im Ausgangsstamm produziert wurde, genauso tödlich für S. aureus war wie das Original. Das bedeutet, dass das CRISPR‑System direkt von der eintreffenden zirkulären DNA exprimiert werden kann, seine Aufgabe erfüllt und dann verloren geht, wenn die Zelle stirbt. Diese integrationsfreie Wirkung verringert weiter die Wahrscheinlichkeit unbeabsichtigter Genübertragungen und unterscheidet diese Partikel von klassischer Phagentherapie, die auf viraler Replikation und Zelllyse zur Verbreitung angewiesen ist.
Vom Petrischale‑Experiment zu infizierten Mammadrüsen
Weil Bap‑produzierende Stämme bei Mastitis im Milchvieh häufig vorkommen, testete das Team ihren leistungsstärksten Konstrukt, genannt ePICIrsaE, in einem Mausmodell, das eine Euterinfektion nachahmt. In Milch und in Laborkulturen dämpften Bap‑reiche Biofilme deutlich die ePICI‑Aktivität. Doch in der Mammadrüse reduzierten wiederholte Gaben von ePICIrsaE die Bakterienzahlen deutlich bei allen getesteten Stämmen, einschließlich der Bap‑bildenden. Seine Wirkung war vergleichbar mit Vancomycin, einem starken Antibiotikum der letzten Linie. Die Ergebnisse deuten darauf hin, dass Bedingungen im lebenden Gewebe – zum Beispiel geringere Bap‑Produktion, das Vorhandensein freischwimmender Bakterien oder helfende Komponenten in der Milch – den konstruierten Partikeln erlauben, weit besser zu wirken als in statischen Laborbiofilmen.
Was das für Landwirtschaft und darüber hinaus bedeuten könnte
Die Studie zeigt, dass nicht‑replizierende, phagenverpackte CRISPR‑Systeme S. aureus gezielt in einer schwierigen, biofilmassoziierten Infektion eliminieren können, ohne sich selbst auszubreiten oder große Mengen an Zellen gleichzeitig zum Platzen zu bringen. Obwohl hohe Partikeldosen erforderlich sind und die Skalierung von Mäusen auf Rinder herausfordernd sein wird, bieten diese Partikel eine vielversprechende, kontrollierbare Alternative zu Antibiotika für lokalisierte Infektionen wie Mastitis. Allgemeiner hebt die Arbeit hervor, dass Behandlungen, die in einfachen Labortests enttäuschend wirken, in der komplexen Umgebung eines lebenden Tieres dennoch erfolgreich sein können, und sie öffnet die Tür zu Bibliotheken maßgeschneiderter ePICIs, die auf verschiedene Bakterien, Phagenhüllen und Führungssequenzen abgestimmt sind.
Zitation: Garmendia-Antoñana, N., Dorado-Morales, P., Gil, C. et al. Targeted elimination of Staphylococcus aureus mastitis infections with synthetic phage-based CRISPR-Cas delivery systems. npj Biofilms Microbiomes 12, 67 (2026). https://doi.org/10.1038/s41522-026-00931-x
Schlüsselwörter: Rindermastitis, Staphylococcus aureus, CRISPR‑Therapie, phagenbasierte Behandlung, Biofilm‑Infektionen