Clear Sky Science · de
Das Darmmikrobiom vermittelt depressionsähnliches Verhalten bei Mäusen mit chronischer Echinococcus multilocularis-Infektion
Wenn eine verborgene Infektion den Geist beeinflusst
Die meisten Menschen denken bei Parasiten an Probleme im Darm oder in der Leber, nicht am Geist. Dennoch berichten viele Patientinnen und Patienten mit lang anhaltenden Infektionen von gedrückter Stimmung, Müdigkeit und verminderter Lebensfreude. Diese Studie untersucht eine überraschende Verbindung: wie eine chronische Bandwurminfektion, die in der Bauchhöhle und der Leber sitzt, über Veränderungen der Darmbakterien und der Chemie im Körper depressionsähnliches Verhalten bei Mäusen auslösen könnte. Das Verständnis dieser Kausalkette könnte langfristig auf neue Wege hinweisen, um die psychische Gesundheit bei Menschen mit hartnäckigen Infektionen zu schützen.
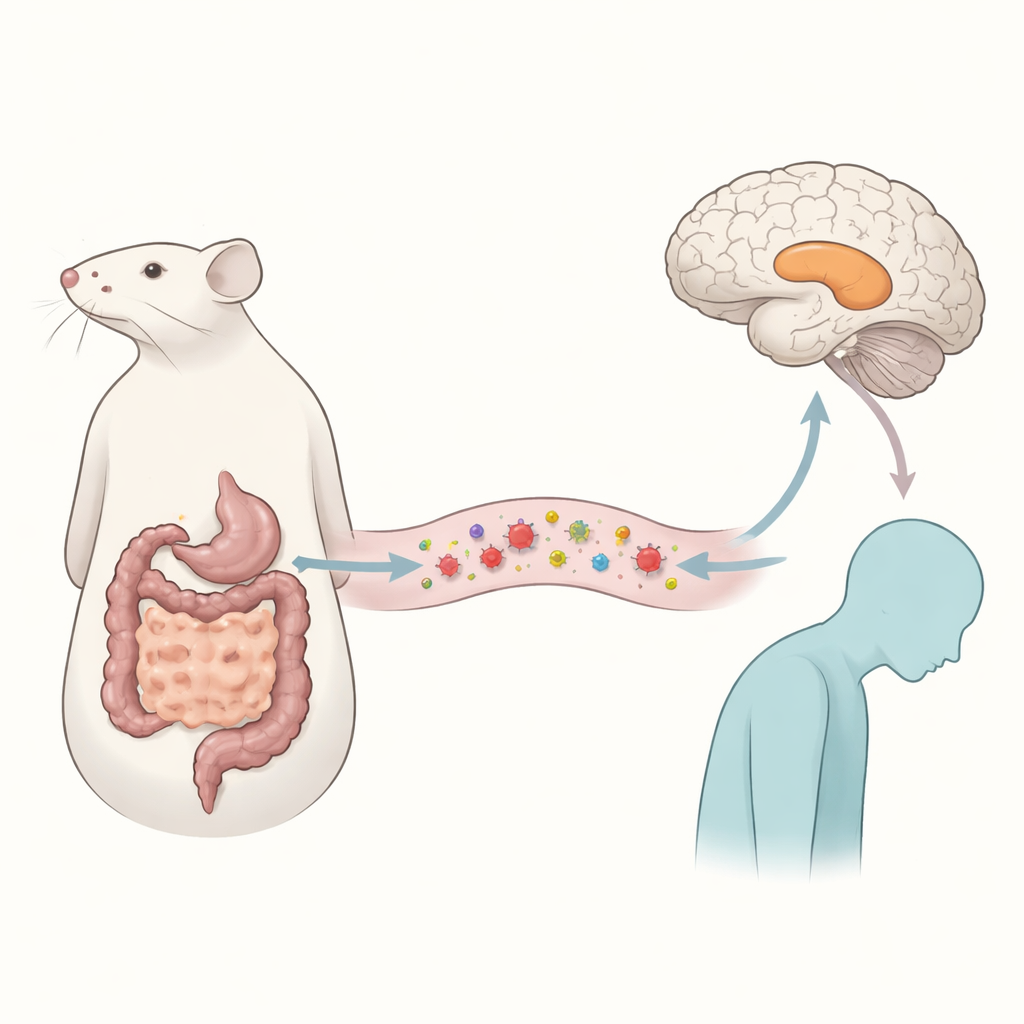
Ein parasitärer Mitbewohner und Stimmungsveränderungen
Die Forschenden konzentrierten sich auf Echinococcus multilocularis, den Erreger der alveolären Echinokokkose, einer schweren Erkrankung, die vorwiegend die Leber befällt. Betroffene berichten häufig über schlechten psychischen Zustand, doch die Ursachen blieben unklar. Um dies zu untersuchen, infizierte das Team Mäuse mit dem Parasiten und wartete zwei Monate, eine Zeitspanne, die einer chronischen Infektion ähnelt. Die Tiere absolvierten anschließend eine Reihe von Verhaltenstests, die dazu dienen, einfache Krankheitssymptome von spezifischeren Stimmungsänderungen zu unterscheiden. Infizierte Mäuse bewegten sich ebenso viel wie gesunde Tiere und lernten sowie erinnerten Aufgaben normal, zeigten jedoch deutliche Anzeichen von depressionsähnlichem Verhalten: geringeres Interesse an süßen Belohnungen und mehr Immobilität in stressbasierten Tests, die bei Nagetieren oft als Messwerte für verzweiflungsähnliche Zustände herangezogen werden.
Feine Veränderungen im Gehirn und Immun‑Signale
Bei der Untersuchung des Gehirns richteten die Wissenschaftlerinnen und Wissenschaftler den Fokus auf Hippocampus und Amygdala, Bereiche, die stark an Emotion und Stress beteiligt sind. Die Gesamtstruktur dieser Regionen blieb intakt, doch unter dem Mikroskop wirkten einige Neurone geschrumpft oder ungewöhnlich geformt, und die äußere Membran ihrer Zellkerne erschien eingefallen. Die im Gehirn ansässigen Immunzellen, die Mikroglia, waren in bestimmten Regionen zahlreicher und zeigten einfachere, weniger verzweigte Formen – Kennzeichen eines Übergangs von einem ruhigen, wachenden Zustand zu einem aktivierten Zustand. Gleichzeitig wiesen sowohl Darmgewebe als auch Blut infizierter Mäuse höhere Konzentrationen entzündlicher Moleküle auf, insbesondere der Zytokine IL‑6 und MCP‑1, und die Gene für einige dieser Signale waren im Hippocampus stärker aktiv. Zusammengenommen deuten diese Befunde auf einen langsam anhaltenden Entzündungszustand hin, der sich vom Darm bis ins Gehirn erstreckt und die dortigen Immunzellen aus dem Gleichgewicht bringt.
Darmbakterien und verlorene chemische Botenstoffe
Das Team fragte dann, ob die Gemeinschaft der im Darm lebenden Mikroben Teil der Erklärung sein könnte. Mithilfe von DNA-Sequenzierung stellten sie fest, dass die Infektion das intestinale Mikrobiom umformte: Nützliche Gruppen wie Lactobacillus und Bifidobacterium gingen drastisch zurück, während andere Gattungen, darunter Ruminococcus und Prevotella, zunahmen. Mäuse mit weniger freundlichen Bakterien hatten tendenziell höhere Werte entzündlicher Zytokine im Darm und im Blut. Gleichzeitig zeigten Bluttests und ein breit angelegtes Metabolitenprofil, dass Schlüsselkomponenten der Tryptophan‑Serotonin‑Achse vermindert waren. Die Spiegel von Tryptophan (einer ernährungsbedingten Aminosäure), des Zwischenprodukts N‑Acetylserotonin und des Neurotransmitters Serotonin (5‑HT) sanken bei infizierten Tieren. Diese Veränderungen spiegeln Befunde wider, die bei Menschen mit Major Depression berichtet wurden, und standen in engem Zusammenhang mit der Häufigkeit bestimmter Darmmikroben.
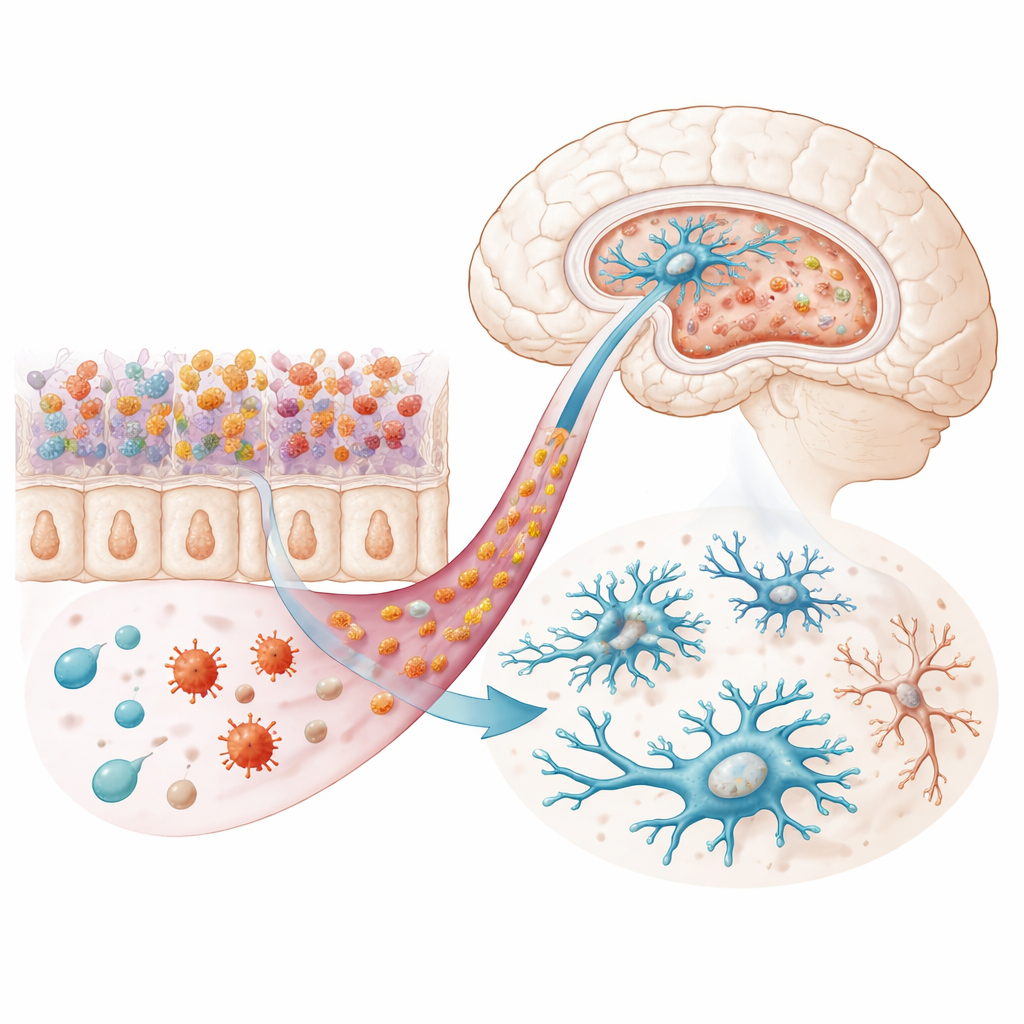
Das Mikrobiom übertragen, die Stimmung übertragen
Um zu prüfen, ob das veränderte Mikrobiom allein das Verhalten verändern kann, führten die Forschenden eine fäkale Mikrobiota-Transplantation durch. Zunächst machten sie das Darmmikrobiom gesunder Mäuse mit Antibiotika frei und setzten dann Kot von entweder infizierten oder nicht infizierten Spendern ein. Bemerkenswerterweise entwickelten Empfängerinnen und Empfänger von Mikrobiota aus infizierten Spendern depressionsähnliches Verhalten und eine angstähnliche Vermeidung der Mitte eines offenen Areals, obwohl sie selbst nie dem Parasiten ausgesetzt waren. Diese Mäuse zeigten zudem verstärkte Entzündungszeichen, reduzierte Werte von Tryptophan- und serotoninbezogenen Molekülen im Blut und Mikroglia, die denen direkt infizierter Tiere ähnelten – in bestimmten Regionen zahlreicher, weniger verzweigt und mit lysosomähnlichen Strukturen gefüllt, was auf erhöhten zellulären Stress oder vermehrte Aufräumaktivität hindeutet.
Was das für die menschliche Gesundheit bedeutet
Für Laien lautet die Kernbotschaft: Eine chronische Infektion im Körper kann die mikrobiellen Bewohner des Darms und die von ihnen mitbeeinflussten chemischen Botenstoffe stören, und dies kann wiederum die Immunzellen und Schaltkreise des Gehirns sowie die Stimmung beeinflussen. Die Studie behauptet nicht, dass dieser Bandwurm beim Menschen klinische Depression verursacht, bietet aber eine detaillierte Landkarte dafür, wie ein langfristiger Parasit, ein entzündeter Darm, ein gestörtes Mikrobiom und veränderter Tryptophan‑Serotonin‑Stoffwechsel zusammenwirken könnten, um depressionsähnliches Verhalten zu erzeugen. Dieses Bild legt nahe, dass die Behandlung psychischer Folgen chronischer Infektionen eines Tages nicht nur das Abtöten des Parasiten umfassen könnte, sondern auch das Beruhigen von Entzündungen und die Wiederherstellung eines gesunden Darmmikrobioms.
Zitation: Wen, R., Xin, Y., Bao, S. et al. The gut microbiota mediates depression-like behaviors in mice with chronic Echinococcus multilocularis infection. npj Biofilms Microbiomes 12, 63 (2026). https://doi.org/10.1038/s41522-026-00929-5
Schlüsselwörter: Darm–Gehirn-Achse, Mikrobiom, parasitische Infektion, Depression, Tryptophan-Stoffwechsel