Clear Sky Science · de
Der ppGpp–HpaR1–gum-Regulationsweg moduliert die Produktion von Exopolysacchariden in Xanthomonas campestris pv. campestris
Warum "klebrige" Bakterien für Nutzpflanzen wichtig sind
Viele krankheitserregende Bakterien überleben und verbreiten sich, indem sie sich in schleimigen Zuckerschichten einhüllen, die als Biofilme bezeichnet werden. In Gemüsearten wie Kohl und Brokkoli können diese Schichten die Wasserleitungsbahnen der Pflanzen verstopfen, was zur bekannten "Schwarzfäule" (black rot) und zu erheblichen Ertragsverlusten führt. Diese Studie blickt in ein solches Bakterium, Xanthomonas campestris, und zeigt, wie ein internes chemisches Alarmsystem die Produktion seiner zuckrigen Schutzschicht steuert. Das Verständnis dieses verborgenen Steuerkreises könnte Forschern helfen, bessere Strategien zum Pflanzenschutz zu entwickeln oder diese Zucker für nützliche Materialien zu nutzen.
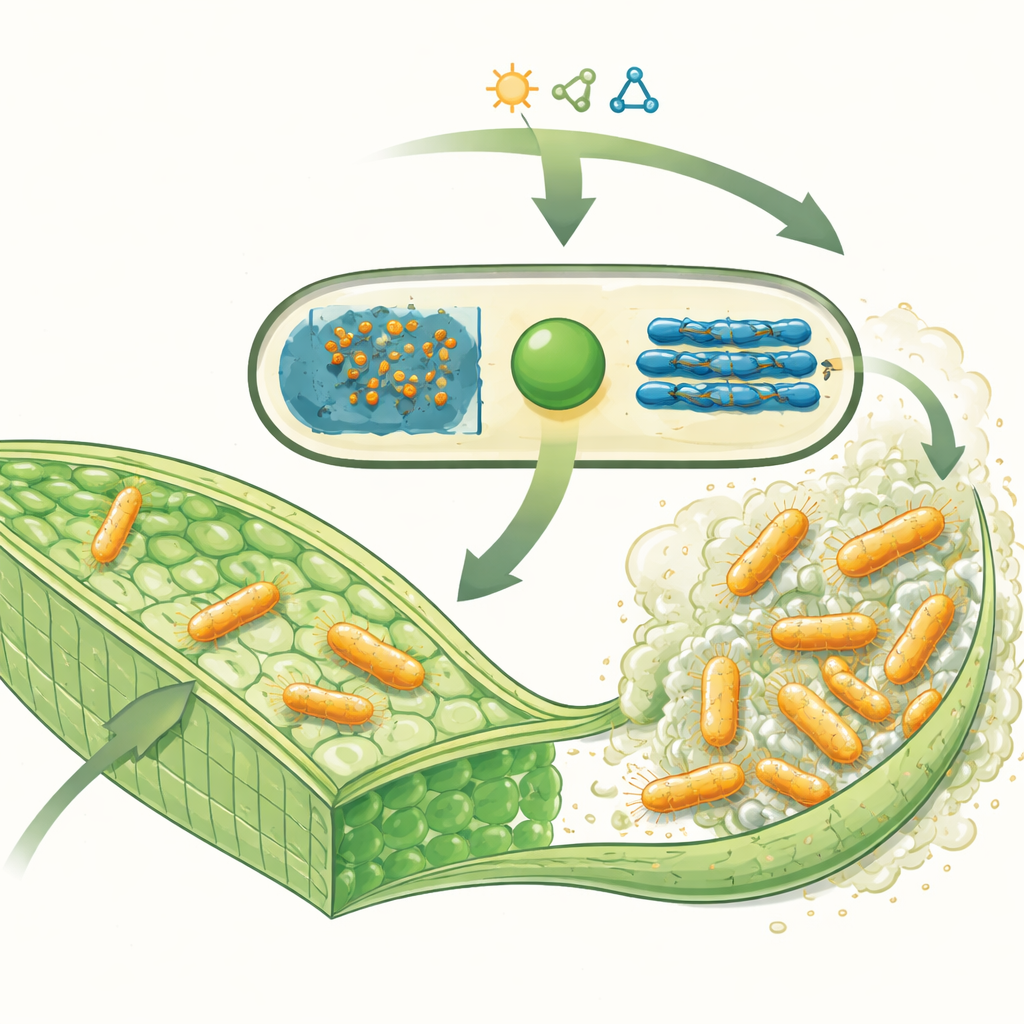
Der pflanzeninfizierende Mikroorganismus und seine Zuckerpanzerung
Xanthomonas campestris dringt in die Leitbahnen von Kreuzblütlern—Pflanzen wie Kohl, Blumenkohl und Senf—ein und produziert große Mengen einer klebrigen Substanz namens Xanthan-Gummi. Dieses Material besteht aus langen Zuckerketten und bildet einen Hauptbestandteil des Biofilms, der den Bakterien hilft, an Pflanzengewebe zu haften, pflanzliche Abwehrmechanismen zu überstehen und unter widrigen Bedingungen zu überleben. Im Pflanzengewebe können diese dicken Zuckerschichten den Wasserfluss blockieren, was zu abgestorbenem Gewebe und den charakteristischen V-förmigen Blattnekrosen der Schwarzfäule führt. Interessanterweise wird derselbe Xanthan-Gummi auch weit verbreitet als Verdickungsmittel in Lebensmitteln und anderen Produkten verwendet, wodurch dieser bakterielle Zucker sowohl ein landwirtschaftlicher Schädling als auch ein industrieller Rohstoff ist.
Ein innerer Alarm, der bakterielles Verhalten formt
Tief in vielen Bakterien wirkt ein kleines Signalmolekül namens ppGpp wie ein Notfallalarm. Wenn Nährstoffe knapp werden oder andere Stressfaktoren auftreten, steigen die ppGpp-Spiegel und lösen eine umfassende "stringente Reaktion" aus, die Wachstum, Stoffwechsel und Überlebensstrategien umgestaltet. Frühere Arbeiten zeigten, dass ppGpp die Biofilmbildung in mehreren Arten fördern kann und dass dessen Entfernung aus Xanthomonas die Fähigkeit der Bakterien schwächt, Biofilme zu bilden und Krankheit zu verursachen. Unklar blieb jedoch, wie dieses winzige Molekül konkret mit der Maschinerie verbunden ist, die den dicken Exopolysaccharid-(EPS-)Mantel dieses Pflanzenpathogens herstellt.
Den Weg vom Signal zum Zucker verfolgen
Die Forschenden verglichen normale Bakterien mit Mutanten, die kein ppGpp herstellen können. Auf zuckerreichen Nährböden bildeten ppGpp-defiziente Mutanten kleinere, weniger muzipöse Kolonien, und direkte Messungen zeigten, dass sie deutlich weniger EPS produzierten. Chemische Profilierung mittels Infrarotspektroskopie und bildgebende Elektronenmikroskopie enthüllten jedoch, dass die Grundzusammensetzung und die höhere Ordnungsform des EPS gleich blieben: Die Mutanten stellten es einfach in geringerer Menge her. Der Fokus richtete sich auf den "gum"-Gencluster, eine Gruppe von Genen, die die Enzyme für den Aufbau von Xanthan-Gummi kodieren. Mithilfe von Genexpressionsmessungen und RNA-Sequenzierung stellte das Team fest, dass nahezu alle gum-Gene in ppGpp-defizienten Zellen herunterreguliert waren, wodurch ppGpp in der Hierarchie oberhalb dieses Clusters eingeordnet wird.
Ein Schlüsselvermittler: der Schalter HpaR1
Zwischen dem ppGpp-Alarm und den gum-Genen steht ein Regulationsprotein namens HpaR1, ein Transkriptionsfaktor, der an DNA bindet und die Aktivität der gum-Gene verstärkt. Die Studie zeigte, dass ppGpp auf zwei Ebenen wirkt. Erstens hatten Zellen ohne ppGpp eine reduzierte Aktivität des hpaR1-Gens, sodass weniger HpaR1-Protein verfügbar war. Zweitens verstärkte in gereinigten Laborversuchen die Zugabe von ppGpp direkt die Bindung von HpaR1 an die DNA-Regionen, die die gum-Gene kontrollieren, und sogar an seine eigene Kontrollregion. Bei moderaten ppGpp-Spiegeln war diese Bindung deutlich stärker, obwohl extrem hohe Spiegel die Wirkung teilweise abschwächten, was auf ein fein abgestimmtes Gleichgewicht hindeutet. Als die Wissenschaftler die HpaR1-Spiegel künstlich erhöhten, stieg die EPS-Produktion wieder an—even in Bakterien, denen ppGpp fehlte—was bestätigt, dass HpaR1 der entscheidende Vermittler zwischen dem Alarmsignal und der Zuckerproduktionsmaschinerie ist.
Was dieser Steuerkreis für Pflanzenbau und darüber hinaus bedeutet
Vereinfacht gesagt deckt diese Arbeit eine dreistufige Relaiskette in einem Pflanzenpathogen auf: Ein inneres Alarmsignal (ppGpp) steigert und stabilisiert einen DNA-bindenden Schalter (HpaR1), der wiederum eine Zuckerfabrik (die gum-Gene) hochfährt, was zu einem dickeren, schützenden Schleimfilm um die Bakterien führt. Durch die detaillierte Kartierung dieses ppGpp–HpaR1–gum-Wegs erklärt die Studie, wie Umweltstresssignale in veränderte Produktion der Biofilmmatrix umgesetzt werden können. Für Landwirte und Pflanzenwissenschaftler deuten diese Einsichten auf neue Angriffspunkte hin, um die Bakterienpanzerung zu stören und Schwarzfäule-Schäden zu verringern. Für Mikrobiologen allgemein fügen die Ergebnisse ein wichtiges Puzzleteil dazu, wie universelle Stresssignale die Bildung komplexer mikrobieller Gemeinschaften steuern.
Zitation: Bai, K., Xu, X., Yu, C. et al. The ppGpp-HpaR1-gum regulatory pathway modulates exopolysaccharides production in Xanthomonas campestris pv. campestris. npj Biofilms Microbiomes 12, 60 (2026). https://doi.org/10.1038/s41522-026-00926-8
Schlüsselwörter: bakterielle Biofilme, Pflanzenpathogene, Xanthan-Gummi, Stresssignalisierung, Exopolysaccharide