Clear Sky Science · de
Echtzeit‑, hochauflösende metabolische Charakterisierung lebender Bakterien mittels label‑freier optischer Stoffwechselbildgebung
Keime in Echtzeit beobachten
Bakterien sind überall auf und in uns und prägen stillschweigend unsere Gesundheit. Sie helfen bei der Verdauung, schützen unsere Haut und verursachen manchmal hartnäckige Infektionen, die Antibiotika trotzen. Diese Studie stellt eine Methode vor, mit der sich lebende Bakterien in Echtzeit auf Einzelzell‑Ebene beobachten lassen, wie sie auf Stress und Wirkstoffe reagieren — ganz ohne Farbstoffe oder Marker. Diese Fähigkeit könnte Ärzten künftig ermöglichen, schneller die passende Behandlung auszuwählen, und Wissenschaftlern helfen zu verstehen, warum manche Infektionen so schwer zu heilen sind.
Licht als Fenster ins bakterielle Leben
Anstatt Farbstoffe oder genetische Marker zu verwenden, nutzen die Forschenden die Tatsache, dass Bakterien von Natur aus sehr schwach leuchten, wenn bestimmte Moleküle in ihnen durch Laserlicht angeregt werden. Zwei dieser Moleküle, bekannt als NAD(P)H und FAD, sind zentrale Akteure darin, wie Zellen Nahrung in Energie umwandeln. Mit schneller, hochauflösender Lasermikroskopie kann das Team sowohl die Helligkeit als auch die winzige zeitliche Verzögerung dieses Leuchtens messen und so erkennen, wie aktiv der Stoffwechsel einer Zelle ist. Da die Methode label‑frei und nicht‑destruktiv ist, können dieselben lebenden Bakterien über Sekunden bis Minuten verfolgt werden, während sich ihre Umgebung ändert. 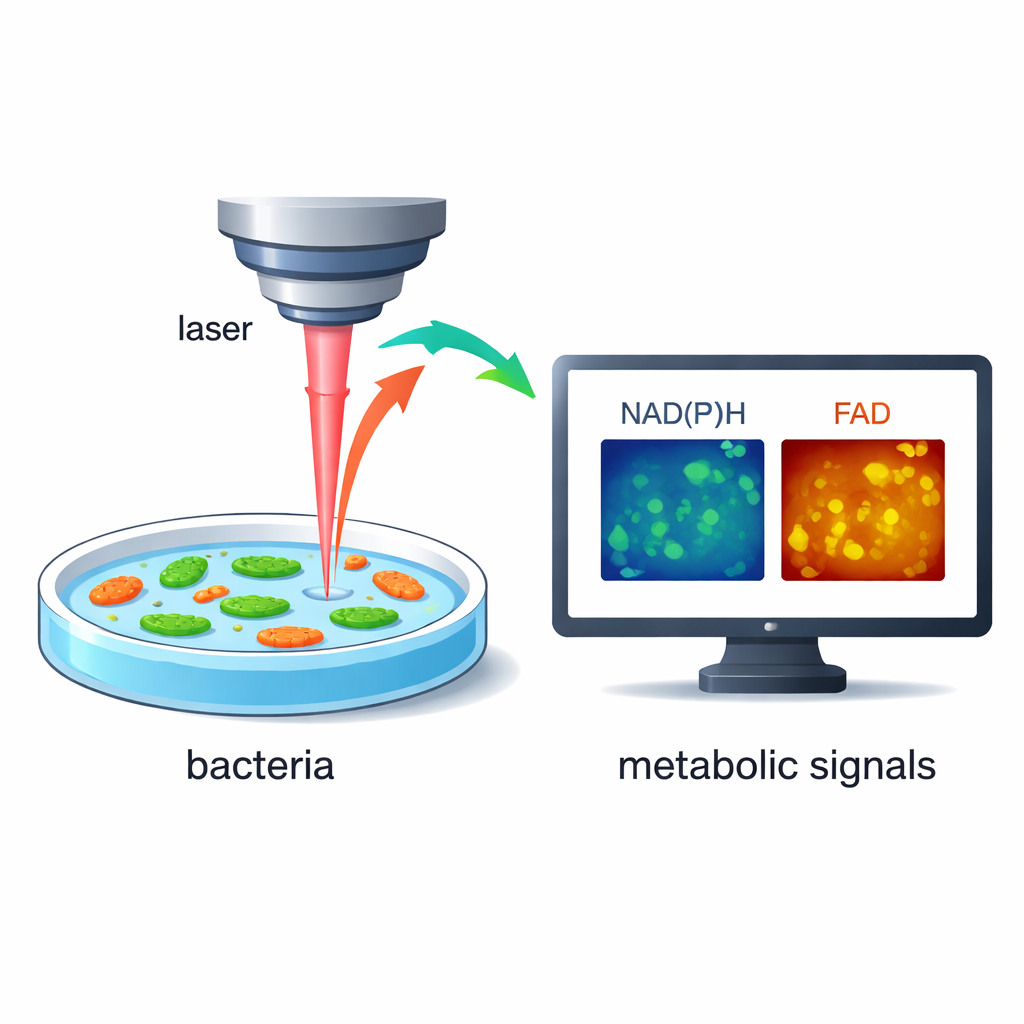
Unterschiede zwischen einzelnen Bakterien sehen
Die meisten Standardlabor‑Tests fassen Millionen von Bakterien zusammen und liefern nur einen Mittelwert. Hier zeigen die Autorinnen und Autoren, dass ihre Bildgebungsmethode einzelne Staphylococcus‑aureus‑Zellen in Flüssigkultur herausfiltern und jede einzelne analysieren kann — selbst bei hoher Zelldichte. Beim Vergleich zweier unter gleichen Bedingungen gewachsener S. aureus‑Kolonien unterschied sich ein wichtiger Signalparameter (von FAD) zwischen den Kolonien, und innerhalb jeder Kolonie gab es ebenfalls eine Spannweite von Werten. Das bedeutet, dass selbst genetisch ähnliche Bakterien im selben Gefäß sehr unterschiedliche metabolische Zustände einnehmen können — eine verborgene Vielfalt, die in herkömmlichen Bulk‑Tests unbemerkt bleiben kann, aber für die Reaktion von Infektionen auf Behandlungen relevant sein dürfte.
Antibiotika innerhalb von Sekunden beobachten
Das Team verfolgte anschließend einzelne S. aureus‑Zellen, während sie verschiedenen antibakteriellen Behandlungen ausgesetzt wurden, darunter gängige Antibiotika und Haushaltsbleiche. Mit ihrem schnellen Bildgebungsaufbau erfassten sie Veränderungen vom Moment an, in dem die Wirkstofflösung die Zellen berührte, bis in die folgenden 30 Minuten. Starke Behandlungen führten dazu, dass NAD(P)H‑Signale abnahmen und FAD‑Signale zunahmen, oft innerhalb von Sekunden — ein Zeichen für gestörte Energieproduktion und eine Verschiebung hin zu einem stärker oxidierten Zustand in der Zelle. Das genaue Timing und Muster dieser Veränderungen hing vom Wirkstofftyp und der Dosis ab: Beispielsweise erzeugten proteinhemmende und zellwandzielende Antibiotika einen kurzen Einbruch mit teilweiser Erholung, während Bleiche eine scharfe, anhaltende Verschiebung bewirkte. Diese charakteristischen „Licht‑Signaturen“ deuten darauf hin, dass die Technik nicht nur erkennen kann, ob Zellen gestresst sind oder sterben, sondern auch, wie sie geschädigt werden. 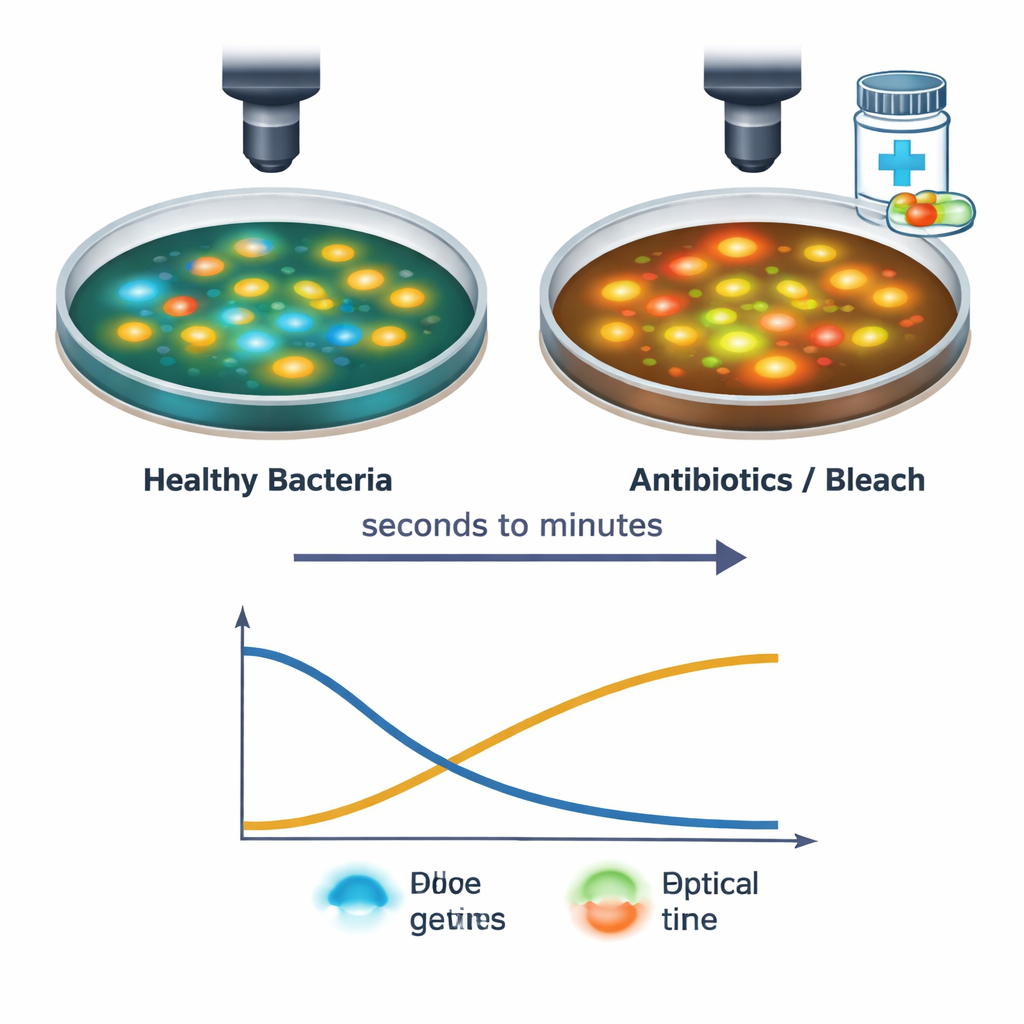
Ein Blick in die verborgene Welt der Biofilme
Bakterien leben in der Natur selten allein; stattdessen bilden sie schleimige, schützende Gemeinschaften — sogenannte Biofilme — auf Oberflächen von medizinischen Implantaten bis zu Zähnen. In diesen dichten Schichten sind manche Zellen hochaktiv, andere ruhen, eine Mischung, die der Gemeinschaft hilft, Antibiotika zu überstehen. Mithilfe großflächig zusammengesetzter Bilder kartierten die Forschenden die metabolische Landschaft innerhalb von S. aureus‑Biofilmen und verglichen sie mit frei schwimmenden Zellen. Sie fanden helle, metabolisch aktive Nischen, umgeben von weniger aktiven Regionen, und zeigten, dass Biofilm‑Bakterien über mehrere Arten hinweg tendenziell ein stärker oxidiertes Stoffwechselprofil aufwiesen als ihre frei lebenden Gegenstücke. Zusätzliche optische Signale deuteten auf vermehrte Lipide und Proteine hin, konsistent mit dem klebstoffartigen Material, das Biofilme zusammenhält.
Warum das für die Medizin der Zukunft wichtig ist
Insgesamt zeigen diese Ergebnisse, dass label‑freie optische Stoffwechselbildgebung schnelle, detaillierte und nicht‑invasive Momentaufnahmen darüber liefern kann, wie Bakterien leben, sich anpassen und sterben. Für eine allgemein interessierte Leserschaft lautet die zentrale Botschaft: Wissenschaftler können nun in Echtzeit den Energiehaushalt von Bakterien „mithören“, ohne die Zellen zu stören — allein mit sorgfältig abgestimmtem Licht. Langfristig könnte diese Technologie helfen, schwer zu kultivierende Bakterien zu identifizieren, resistente Zellnester in Biofilmen aufzuspüren oder schnell zu testen, wie eine Infektion eines Patienten auf verschiedene Antibiotika anspricht. Das könnte schnellere, gezieltere Behandlungen ermöglichen und unser Verständnis der unsichtbaren mikrobiellen Welten vertiefen, die unsere Gesundheit jeden Tag beeinflussen.
Zitation: Sorrells, J.E., Yang, L., Iyer, R.R. et al. Real-time, high-resolution metabolic characterization of live bacteria using label-free optical metabolic imaging. npj Biofilms Microbiomes 12, 55 (2026). https://doi.org/10.1038/s41522-026-00920-0
Schlüsselwörter: bakterieller Stoffwechsel, optische Bildgebung, Biofilme, Antibiotika‑Reaktion, Mikrobiom