Clear Sky Science · de
Lactobacillus-vermittelte Nanobodies verbessern die Mastleistungsfähigkeit bei subklinischer nekrotischer Enteritis mit begleitenden Veränderungen im Mikrobiom und Transkriptom
Warum die Darmgesundheit von Hühnern auf Ihrem Teller eine Rolle spielt
Moderne Geflügelfarmen balancieren auf einem Drahtseil: Sie müssen Milliarden von Vögeln effizient aufziehen und zugleich den Einsatz von Antibiotika reduzieren, die zur Entstehung multiresistenter Erreger beim Menschen beitragen können. Eine der größten versteckten Bedrohungen für Masthühner ist eine Darmerkrankung namens subklinische nekrotische Enteritis. Betroffene Tiere wirken oft normal, wachsen aber langsamer und benötigen mehr Futter, um dasselbe Gewicht zu erreichen — was die Kosten und die Umweltbelastung von Hühnerfleisch heimlich erhöht. Diese Studie untersucht einen neuen, sehr gezielten probiotischen Ansatz, bei dem freundliche Bakterien mit winzigen Antikörperfragmenten ausgerüstet werden, die krankheitsverursachende Toxine direkt im Darm neutralisieren.
Eine kostspielige, meist unsichtbare Darmerkrankung
Nekrotische Enteritis wird durch das verbreitete Darmbakterium Clostridium perfringens verursacht, wenn es übermäßig wächst und starke Toxine freisetzt. In schwerer Form tötet die Krankheit Tiere und verursacht offensichtliche Darmschäden. Deutlich häufiger ist jedoch die subklinische Form, bei der Toxine wie NetB und Alpha-Toxin die Darmschleimhaut subtil schädigen. Vögel verdauen Futter weniger effizient, nehmen weniger zu und zeigen dennoch kaum äußere Krankheitszeichen. Weltweit wird dieser stille Produktivitätsverlust auf mehr als 2 Milliarden US-Dollar jährlich für Geflügelproduzenten geschätzt. Historisch wurde das Problem durch antibiotikahaltiges Futter kontrolliert, doch die wachsende Sorge um antimikrobielle Resistenzen und die Nachfrage der Verbraucher nach „ohne Antibiotika aufgezogenem“ Geflügel haben den Einsatz solcher Medikamente unattraktiver gemacht und den Bedarf an präzisen, medikamentenfreien Alternativen erhöht.
Probiotika als gezielte Toxinblocker
Die Forschenden bauten auf früheren Arbeiten auf, in denen zwei Stämme des probiotischen Bakteriums Limosilactobacillus reuteri so gentechnisch verändert wurden, dass sie „Nanobodies“ — sehr kleine Antikörperfragmente — sezernieren, die an NetB- bzw. Alpha-Toxin binden und diese neutralisieren. In der neuen Studie prüften sie, ob diese Designer-Probiotika die Leistungsfähigkeit von Masthühnern unter einer milden, kommerziell realistischen Form der Erkrankung verbessern können. In einem 43-tägigen Versuch wurden mehr als 2.000 Vögel in vier Gruppen aufgeteilt: eine herausgeforderte Kontrollgruppe; eine Gruppe, die ein übliches prophylaktisches Antibiotikum (Bacitracin methylene disalicylate, BMD) erhielt; eine Gruppe, die die gentechnisch veränderten Nanobody-produzierenden Stämme (NE01 und NE06) bekam; und eine Gruppe, die die ursprünglichen, nicht veränderten Elternstämme des Probiotikums erhielt. Alle Vögel wurden gegen Kokzidiose geimpft und anschließend mit C. perfringens exponiert, um eine subklinische Erkrankung auszulösen.
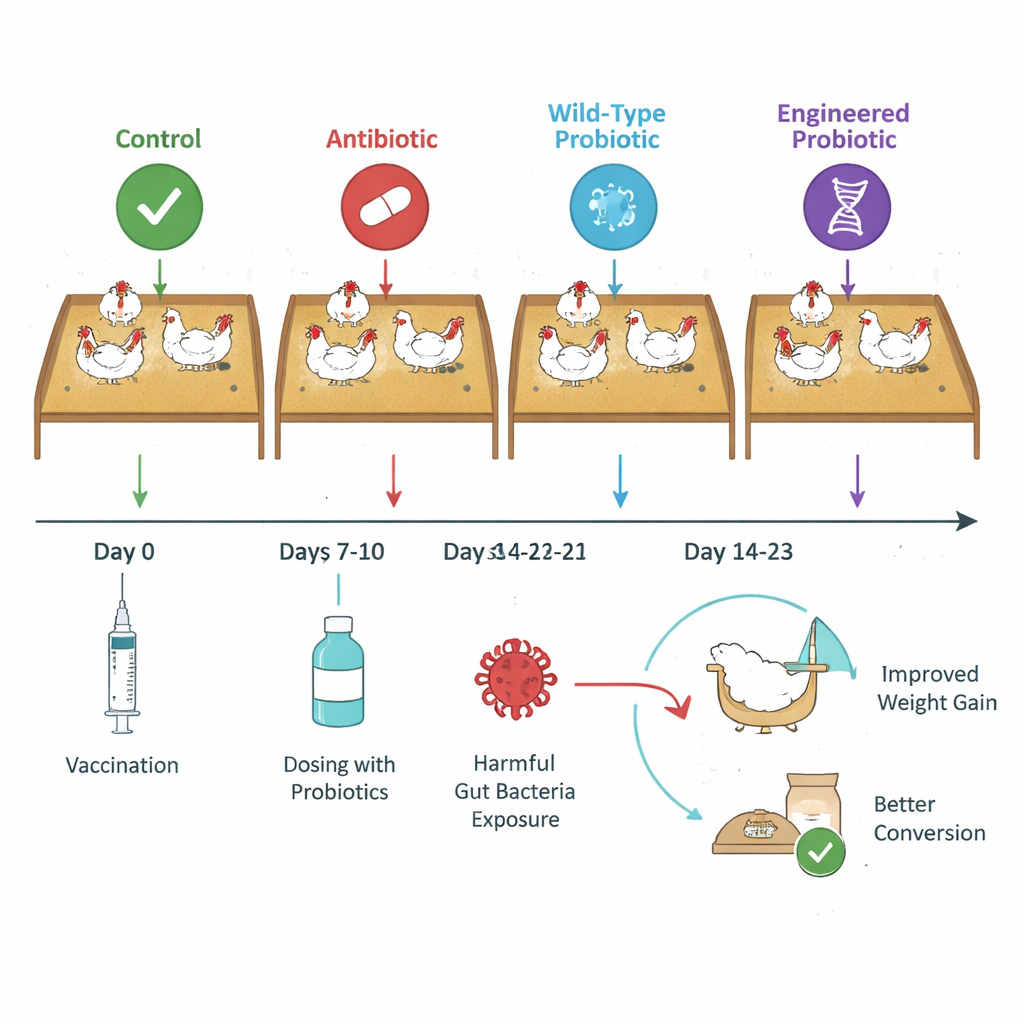
Besseres Wachstum bei geringeren versteckten Kosten
Vögel, die die Nanobody-produzierenden Stämme erhielten, verwerteten Futter über verschiedene Zeitpunkte hinweg konstant effizienter als die anderen Gruppen. Ihr futterbereinigter Futterverwertungsquotient (mortality-adjusted feed conversion ratio) verbesserte sich um 4–7 „Punkte“ (0,04–0,07 Einheiten) gegenüber unbehandelten Vögeln, und sie waren zum Ende der Studie 34–81 Gramm schwerer als entweder die herausgeforderte Kontrollgruppe, die Antibiotikagruppe oder die Vögel mit herkömmlichen Probiotika. Interessanterweise zeigten klassische Krankheitsmaße — wie sichtbare Darmläsionen und Zählungen von C. perfringens in Kot und Blinddarminhalt — nur geringe Unterschiede zwischen den Behandlungen. Das bedeutet, dass alle Vögel ein ähnliches Maß an schwacher Belastung erlebten, die Nanobody-Gruppe diese Belastung jedoch deutlich effizienter bewältigte und dasselbe Futter in mehr Fleisch umwandelte.
Beruhigtere Mikrobiome und ruhigere Immunsysteme
Um zu verstehen, warum die Leistungsparameter besser waren, blickte das Team über die grobe Pathologie hinaus und untersuchte das Mikrobiom sowie die Genaktivität im Darm und in der Leber. Metatranskriptomische Analysen des Jejunuminhalts (Dünndarm) zeigten, dass in den Vögeln, die die gentechnisch veränderten Stämme erhielten, mehr L. reuteri-Transkripte und nachweisbare Expression der Nanobody-Gene vorhanden waren, was bestätigt, dass die Probiotika im Darm überlebten und ihre toxinblockierenden Moleküle produzierten. Die Gesamtkonstitution des Mikrobioms veränderte sich primär mit dem Alter der Vögel und weniger durch die Behandlung, doch die Nanobody-Gruppe wies eine geringere Stichproben-zu-Stichproben-Variabilität auf, was auf eine stabilere und widerstandsfähigere Darmgemeinschaft hindeutet. Funktionell exprimierten die Darmmikroben in dieser Gruppe mehr Gene, die mit Fermentation und Proteinsynthese verknüpft sind, und weniger Gene, die mit Atmung und Nitratnutzung assoziiert sind — Muster, die mit einer weniger entzündeten Umgebung korrelieren. Die Forschenden beobachteten außerdem eine erhöhte Expression von Enzymen zur Produktion einer Verbindung namens 2,3-Butandiol, die in Tiermodellen entzündungshemmende Effekte zeigt.
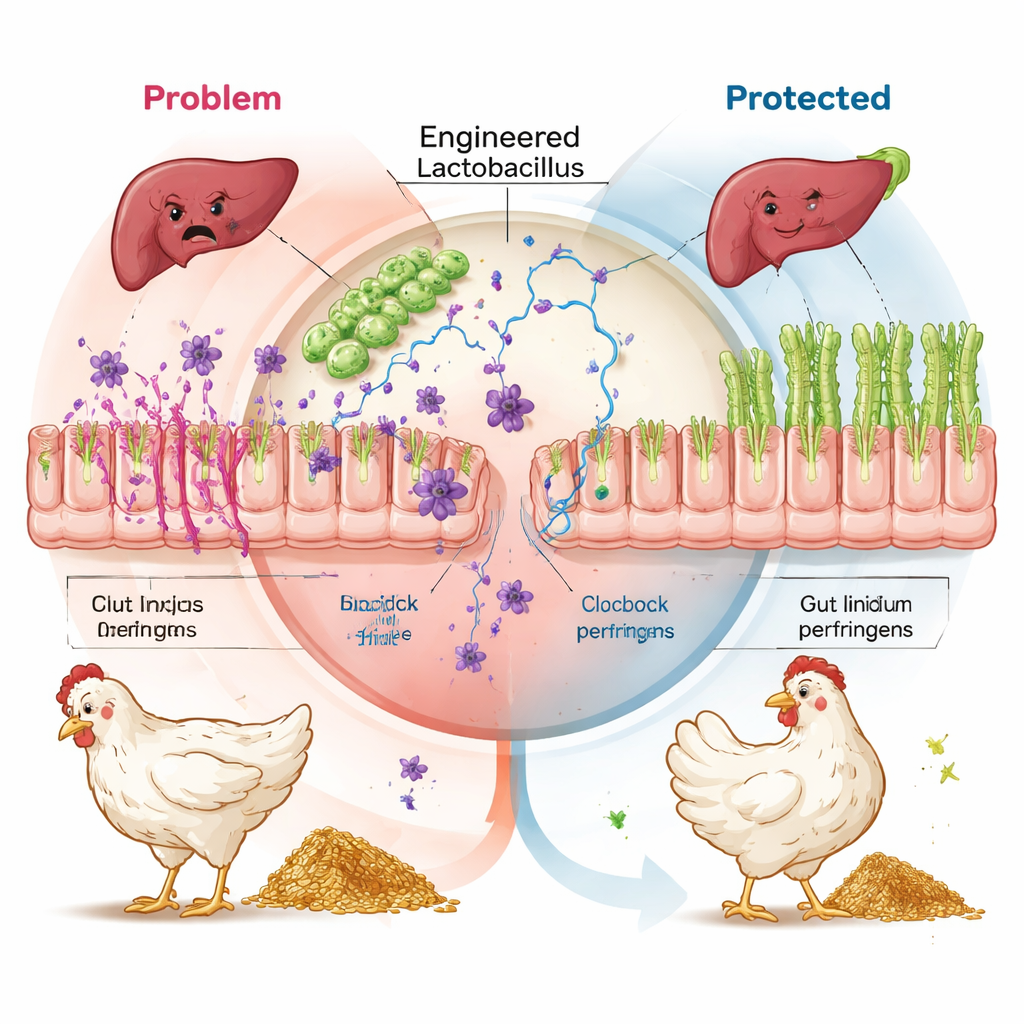
Schutz entfernter Organe und erhöhte Effizienz
Die Effekte reichten über den Darm hinaus. Die Genexpression im Jejunum und in der Leber zeigte, dass Vögel, die die gentechnisch veränderten Probiotika erhielten, deutlich geringere Aktivierung von Immun- und oxidativem Stresswegen aufwiesen als die herausgeforderten Kontrollen und in vielen Fällen auch im Vergleich zu den Antibiotika- und herkömmlichen Probiotikagruppen. In der Leber — einem Organ, das als Kollateralschaden durch bakterielle Toxine leidet — zeigte die Nanobody-Gruppe eine reduzierte Signalgebung durch Insulin- und mTOR-Wege, die bei toxininduzierter Schädigung hochgefahren werden, während antioxidative und energieerzeugende Wege verstärkt wurden. Zusammengenommen deuten diese Befunde darauf hin, dass die Neutralisierung von NetB- und Alpha-Toxin an der Darmoberfläche eine Kaskade von Entzündung und Gewebeschädigung verhindert und den Vogel so vor den hohen metabolischen Kosten schützt, die mit dem ständigen Bekämpfen versteckter Infektionen verbunden sind.
Was das für die Zukunft von Geflügel- und Humanmedizin bedeutet
Für die breite Leserschaft lautet die Kernbotschaft: Nicht alle „Probiotika“ sind gleich. Indem hilfreiche Bakterien mit präzise gezielten Nanobodies ausgerüstet werden, schufen die Forschenden eine lebende Therapie, die Hühner vor einer häufigen, weitgehend unsichtbaren Darmerkrankung schützt, ohne auf traditionelle Antibiotika zurückzugreifen — und die sowohl einer Antibiotikabehandlung als auch Standardprobiotika überlegen war. Die Vögel benötigten weniger Futter, um das Schlachtgewicht zu erreichen, und zeigten weniger Anzeichen innerer Belastung. Wenn ähnliche Strategien auf andere Nutztiere und langfristig auf den Menschen übertragbar sind, könnten gentechnisch veränderte Probiotika eine wirkungsvolle Möglichkeit bieten, schädliche Darmaustritte zu entschärfen, während nützliche Mikroben erhalten bleiben und die Verbreitung von Antibiotikaresistenzen verlangsamt wird.
Zitation: Hall, A.N., Manuja, S., Payling, L.M. et al. Lactobacillus-vectored nanobodies improve broiler productivity under sub-clinical necrotic enteritis with associated microbiome and transcriptome changes. npj Biofilms Microbiomes 12, 52 (2026). https://doi.org/10.1038/s41522-026-00916-w
Schlüsselwörter: konstruktive Probiotika, nekrotische Enteritis, Darmgesundheit von Geflügel, Nanobodies, Alternative zu Antibiotika