Clear Sky Science · de
Enzymverstärkte Antibiotikatherapie reduziert Biofilme im Modell einer implantatassoziierten Infektion auf nicht nachweisbare Werte
Warum hartnäckige Implantatinfektionen wichtig sind
Hüft‑ und Knieendoprothesen verändern Leben, aber wenn sich Bakterien auf diesen Metallimplantaten ansiedeln, können sie schleimige Gemeinschaften bilden, sogenannte Biofilme. Diese Biofilme wirken wie gepanzerte Städte, die Keime sowohl vor dem Immunsystem als auch vor Antibiotika abschirmen, was zu schmerzhaften, langwierigen Infektionen führt, die nur schwer zu heilen sind. Diese Studie untersucht eine neue, zweigleisige Behandlung, die zunächst die Abwehr des Biofilms aufbricht und anschließend den Bereich mit hohen Antibiotikadosen durchflutet — ein Ansatz, der eines Tages helfen könnte, mehr Implantate zu retten, anstatt sie zu ersetzen.
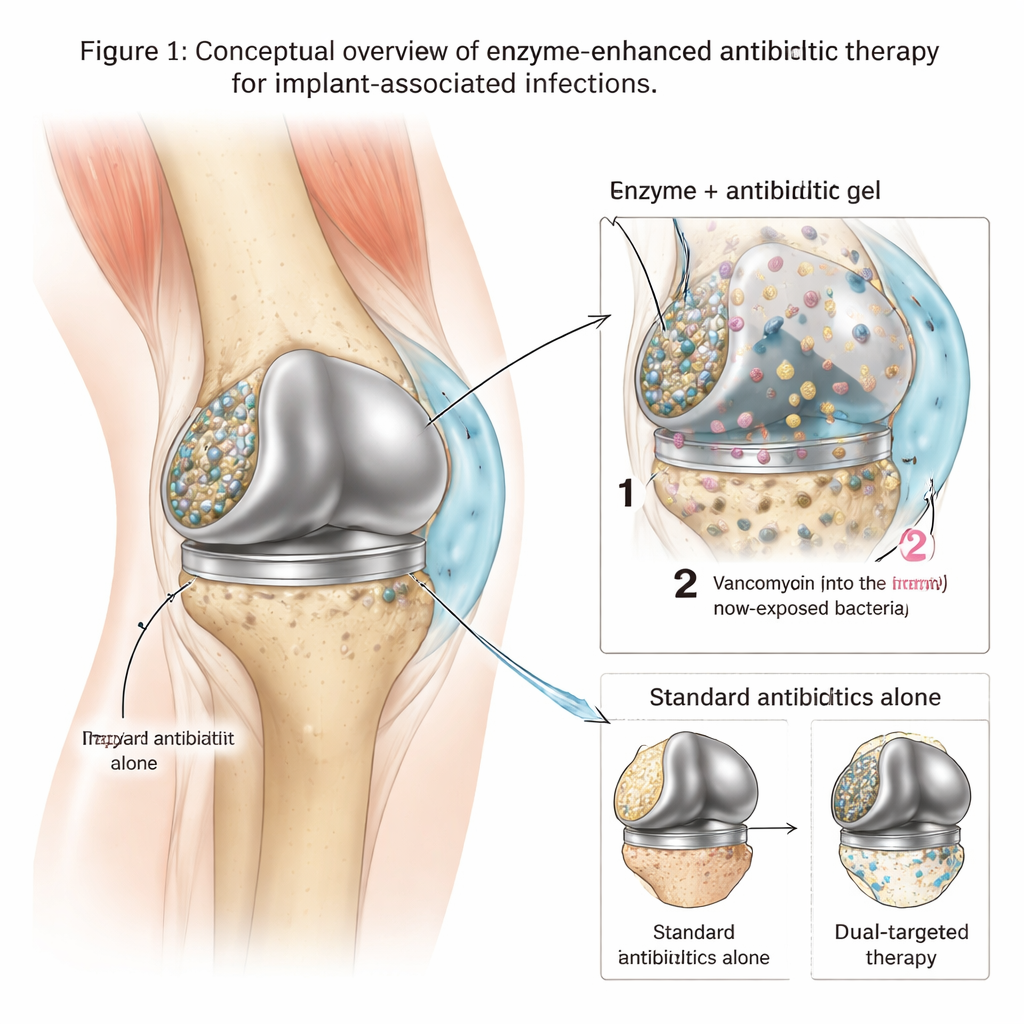
Die verborgenen Hochburgen auf Metallimplantaten
Wenn sich Bakterien wie methicillinresistenter Staphylococcus aureus (MRSA) an einem künstlichen Gelenk anheften, bauen sie schnell eine klebrige Matrix aus DNA, Zuckern und anderen Molekülen auf der Metalloberfläche auf. Innerhalb dieses geschützten Biofilms wachsen die Bakterien langsam, ändern ihr Verhalten und können Antibiotikakonzentrationen tolerieren, die hunderte oder sogar tausende Male höher sind als jene, die frei schwebende Keime abtöten. Infolgedessen schlagen Standardbehandlungen — selbst starke Wirkstoffe wie Vancomycin — oft nicht vollständig zu, wodurch Patienten wiederholte Operationen oder einen kompletten Implantataustausch erleiden müssen. Ärztinnen und Ärzte brauchen Werkzeuge, die nicht nur Bakterien abtöten, sondern auch ihre schützende Festung öffnen, damit die Medikamente sie erreichen können.
Ein intelligentes Gel, das Enzyme und Antibiotika liefert
Die Forschenden entwickelten eine lokale Therapie auf Basis eines thermosensitiven Hydrogels aus dem Stoff Poloxamer 407. Dieses Gel ist kalt flüssig, wodurch es sich leicht um ein Implantat injizieren lässt, verwandelt sich aber schnell bei Körpertemperatur in einen weichen Feststoff und bleibt so am Ort. In dieses Gel luden die Forscher zwei zentrale Bestandteile: ein starkes Antibiotikum (Vancomycin) und einen Cocktail aus drei Enzymen, die die Hauptbestandteile der Biofilmmatrix zerschneiden. Im Labor stellten sie das Gel so ein, dass die Enzyme zuerst freigesetzt werden — wodurch der Biofilm gelockert und ausgedünnt wird — während Vancomycin langsamer über mehrere Tage abgegeben wird und so sehr hohe lokale Wirkstoffspiegel genau dort aufrechterhält, wo die Bakterien leben.
Vom Labor in Versuchstiere
Um zu prüfen, ob die Strategie wirklich wirkt, testete das Team sie zunächst an Biofilmen, die auf Titanstücken im Labor gewachsen waren, und anschließend in einem Meerschweinchenmodell, das infizierte Implantate nachbildet. In vitro reduzierten zwei Anwendungen des Enzym‑Antibiotika‑Gels im Abstand von 48 Stunden die Anzahl lebensfähiger Bakterien auf Metalloberflächen um mehr als den Faktor 100.000 und tilgten nahezu die Biofilmmasse. In den Tieren setzten die Forschenden chirurgisch durchlochte Käfige mit Titanperlen unter die Haut, infizierten diese mit MRSA und behandelten sie dann mit verschiedenen Kombinationen aus systemischen Antibiotika und lokalen Gelen. Das wirksamste Regime kombinierte: (1) das lokale Gel mit Enzymen und Vancomycin, zweimal verabreicht, und (2) eine körpersystemische Behandlung mit Vancomycin plus einem zweiten Antibiotikum, Rifampicin, das besonders gut in Biofilme eindringt.
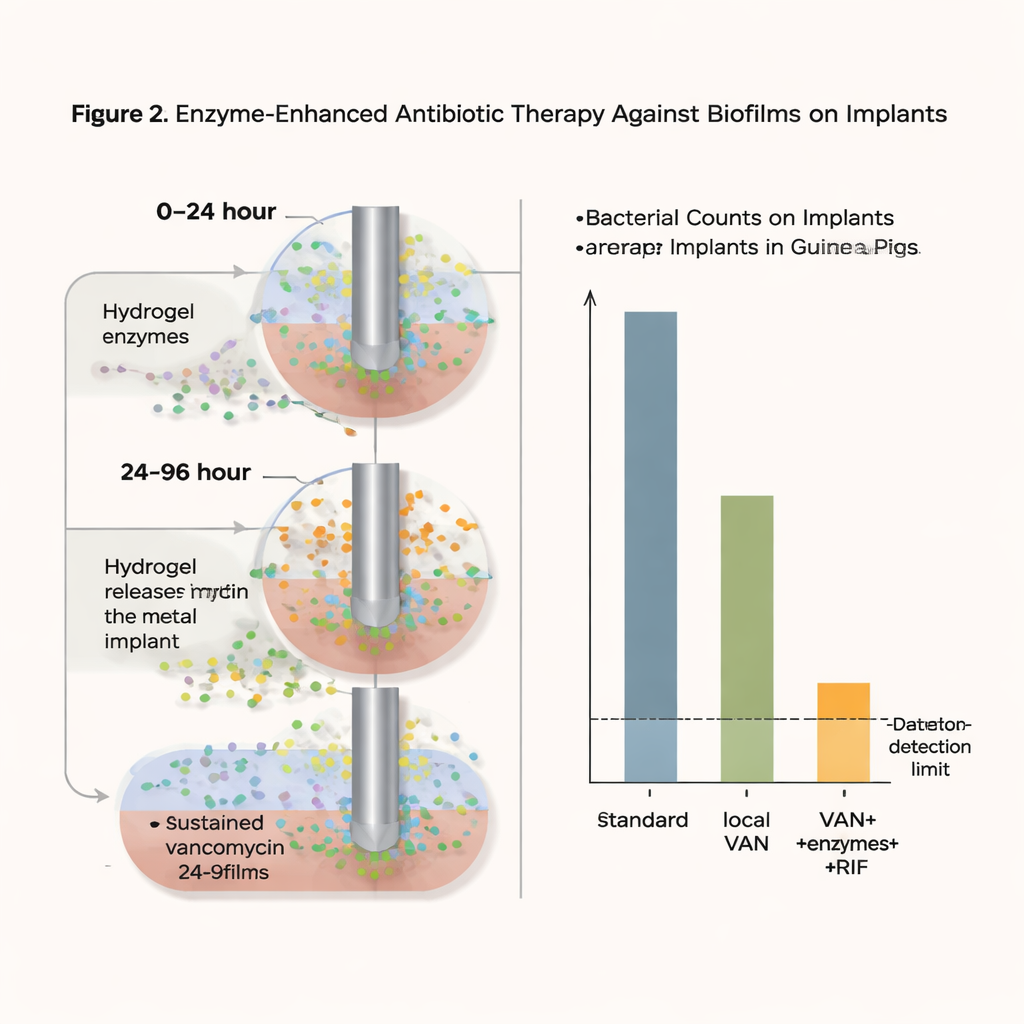
Was der neue Ansatz erreichte
Mit dieser intensiven, aber lokal begrenzten Strategie sanken die bakteriellen Zahlen auf dem Implantatmaterial in diesem Modell auf die Nachweisgrenze — effektiv „keine kultivierbaren Bakterien mehr“ — in 75 Prozent der behandelten Käfige einen Tag nach Therapieende und in 37,5 Prozent sogar fünf Tage später. Wichtig ist, dass keine Zunahme der Vancomycin‑Resistenz beobachtet wurde, und hohe lokale Vancomycinwerte schienen zudem das Entstehen Rifampicin‑resistenter Stämme zu verhindern. Sicherheitstests an kultivierten Zellen und an einem rekonstituierten menschlichen Hautmodell zeigten keine Anzeichen von Toxizität oder Reizung durch die Gelformulierungen. Obwohl in einigen Fällen ein leichtes Nachwachsen der Bakterien auftrat und die Behandlungsdauer kürzer war als üblich beim Menschen, zeigen die Ergebnisse, dass die Kombination aus biofilmauflösenden Enzymen und anhaltender lokaler Antibiotikafreisetzung hartnäckige Infektionen dramatisch verkleinern kann.
Was das für Patientinnen und Patienten bedeuten könnte
Für Menschen mit implantatbezogenen Infektionen deutet diese Arbeit auf eine Zukunft hin, in der Chirurginnen und Chirurgen möglicherweise ein intelligentes Gel um ein infiziertes Gelenk injizieren, statt die Hardware sofort zu entfernen oder zu ersetzen. Indem zuerst der Schutzschild des Biofilms geschwächt und dann der Bereich mit hohen, anhaltenden Antibiotikadosen durchflutet wird — abgesichert durch eine systemische Behandlung — zielt diese doppelt ausgerichtete Strategie darauf ab, die Bakterienzahlen auf nicht nachweisbare Werte zu drücken und das Risiko von Resistenzen zu verringern. Obwohl weitere Studien, längere Behandlungszeiträume und Humanstudien noch nötig sind, bietet der Ansatz eine vielversprechende Blaupause, um einige der hartnäckigsten orthopädischen Infektionen besser beherrschbar und potenziell heilbar zu machen.
Zitation: Buzisa Mbuku, R., Poilvache, H., Maigret, L. et al. Enzymes-enhanced antibiotic therapy reduces biofilms to undetectable levels in an implant-associated infection model. npj Biofilms Microbiomes 12, 44 (2026). https://doi.org/10.1038/s41522-026-00910-2
Schlüsselwörter: Biofilminfektion, orthopädische Implantate, Vancomycin, enzymatische Therapie, Rifampicin