Clear Sky Science · de
Eine theoretische Untersuchung von Protokollen zur Behandlung von Infektionen bei Gelenkprothesen mit Kombinationen aus Antibiotika und Bakteriophagen
Warum Infektionen von Gelenkimplantaten wichtig sind
Hüft- und Kniegelenk-Ersatzoperationen haben das Leben von Millionen Menschen verändert und ermöglichen schmerzfreies Gehen. Wenn sich jedoch Bakterien auf diesen künstlichen Gelenken ansiedeln, können sie schleimige Gemeinschaften bilden, sogenannte Biofilme, die sich fest an Metall- und Kunststoffoberflächen heften. Ist ein Biofilm erst etabliert, haben normale Antibiotikadosen und die körpereigenen Abwehrkräfte oft Schwierigkeiten, ihn zu vernichten, was mitunter erneute Operationen erforderlich macht. Diese Studie fragt, ob das Hinzufügen von auf Bakterien spezialisierten Viren — sogenannten Bakteriophagen oder Phagen — zu Standardantibiotika einen besseren Ansatz zur Behandlung dieser hartnäckigen Infektionen bieten kann.
Kleine Viren, die Bakterien jagen
Phagen sind natürliche Räuber von Bakterien. Sie heften sich an eine Bakterienzelle, injizieren ihr genetisches Material, verwandeln die Zelle in eine Virusfabrik und lassen sie schließlich platzen, wodurch eine Vielzahl neuer Phagen freigesetzt wird. Manche Phagen tragen außerdem Enzyme, die das klebrige Material von Biofilmen zersetzen können und so schützende Schichten öffnen, die Bakterien vor Medikamenten abschirmen. Wegen dieser Eigenschaften hoffen viele Forschende, dass die Kombination von Phagen und Antibiotika einen wirksamen Doppelschlag gegen Infektionen von Gelenkprothesen liefern könnte — insbesondere wenn Bakterien gegen Antibiotika resistent werden.
Infektionen im Computer nachbilden
Anstatt sofort Tierversuche oder klinische Studien durchzuführen, erstellten die Autoren zunächst ein detailliertes mathematisches und computergestütztes Modell einer Infektion von Gelenkprothesen. Ihr virtuelles System hatte zwei Hauptzonen: frei schwimmende Bakterien in Körperflüssigkeiten und in einem Biofilm auf der Implantatoberfläche eingebettete Bakterien. Das Modell verfolgte zudem Immunzellen, Nährstoffe für das Bakterienwachstum, Antibiotika und Phagen, die alle in das Gelenk hinein- und herausdiffundierten. Durch Variation von Bedingungen wie Wirkstoffdosis, Zeitpunkt und dem Vorhandensein antibiotikaresistenter Bakterien konnten sie viele Behandlungsstrategien untersuchen, die in realen Patienten schwer, langsam oder teuer zu testen wären.
Wenn Medikamente allein und zusammen wirken
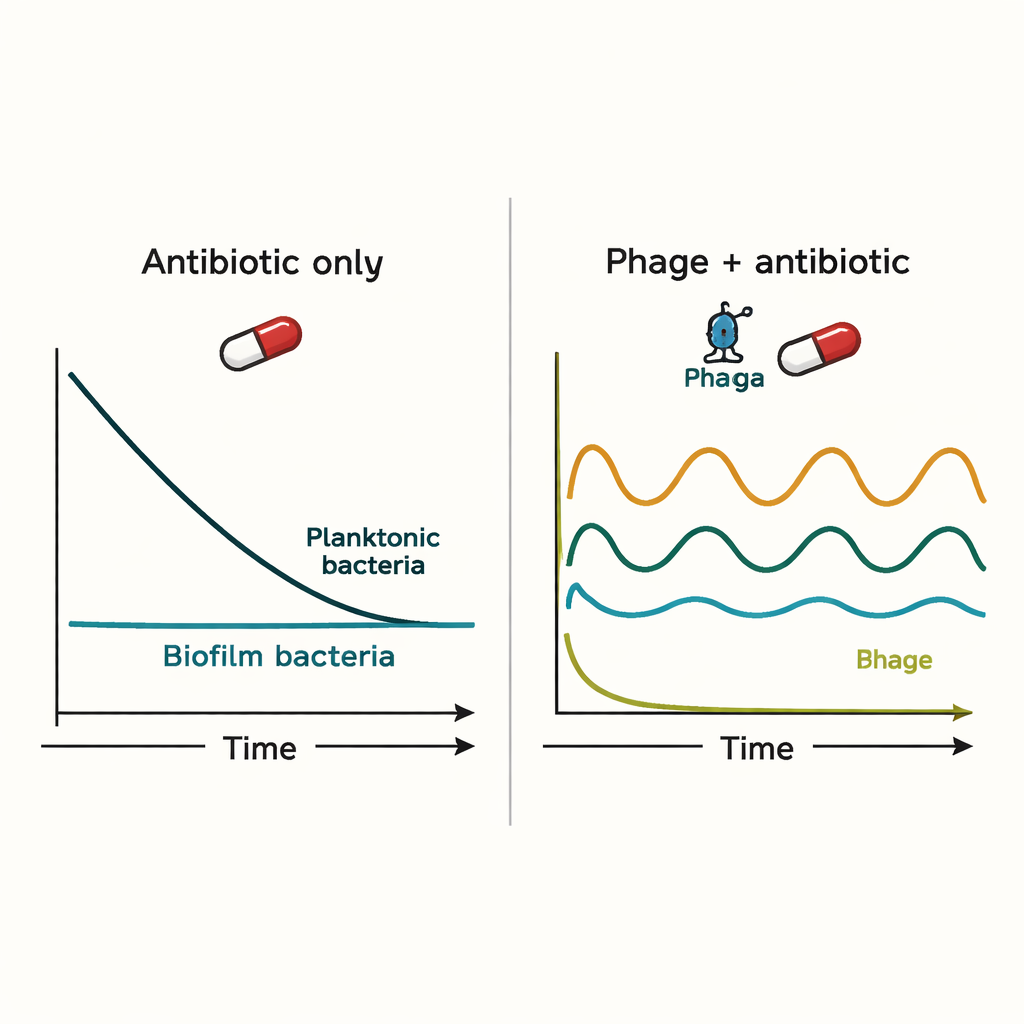
Die Simulationen zeigten, dass weder das Immunsystem noch Antibiotika allein Biofilminfektionen leicht beseitigen. Antibiotika reduzierten frei schwimmende Bakterien stark, hatten aber kaum Einfluss auf die Biofilmpopulation. Phagen konnten die Infektion zunächst effektiver kontrollieren, führten jedoch zu Boom‑und‑Bust‑Zyklen: Wenn Phagen Bakterien abtöteten, wurden ihre Wirte zu selten, woraufhin die Phagenpopulation sank und den Bakterien ein Wiederaufleben ermöglichte. Wurden Antibiotika und Phagen gleichzeitig verabreicht, dominierte oft das Antibiotikum das Ergebnis, und das Hinzufügen von Phagen bewirkte häufig nur wenig mehr als das Antibiotikum allein.
Die besondere Rolle von Timing und Resistenz
Das Modell wurde optimistischer, als antibiotikaresistente Bakterien berücksichtigt wurden. Phagen konnten diese resistenten Zellen angreifen und sie in manchen Fällen vollständig entfernen. Wenn die Phagenbehandlung zuerst begonnen und die Antibiotika einige Stunden später hinzugefügt wurden, verringerte die kombinierte Strategie in den Simulationen die frei schwimmenden Bakterien um viele Größengrade und beseitigte resistente Unterpopulationen. Dennoch wurden die biofilmassoziierten Bakterien nicht vollständig eliminiert; stattdessen wurden ihre Zahlen auf niedrigere Werte gehalten, die das Immunsystem möglicherweise leichter bewältigen kann. Das deutet darauf hin, dass Phagen eher als Helfer nützlich sein könnten, die Resistenz verhindern und Infektionen in Schach halten, statt als Wunderwaffen.
Was das für Patientinnen, Patienten und Ärztinnen und Ärzte bedeutet
Für Menschen mit einer infizierten Gelenkprothese bietet diese Arbeit sowohl Vorsicht als auch Hoffnung. Das Modell legt nahe, dass das bloße Hinzufügen von Phagen zu Standardantibiotika allein wahrscheinlich keine tiefsitzenden Biofilminfektionen heilt. Phagen könnten jedoch weiterhin wertvolle Werkzeuge sein: Sie könnten dabei helfen, antibiotikaresistente Bakterien zu beseitigen und die Gesamtzahl der Keime so weit zu reduzieren, dass der Körper sie bewältigen kann — insbesondere, wenn sie vor oder zeitlich abgestimmt mit Antibiotika eingesetzt werden. Die Autoren betonen, dass dies theoretische Vorhersagen und keine klinischen Beweise sind. Ihre Hauptbotschaft lautet, dass sorgfältig geplante Experimente — geleitet von Modellen wie diesem — notwendig sind, um zu entdecken, wann die Phagentherapie die Ergebnisse für Patientinnen und Patienten mit Infektionen von Gelenkprothesen tatsächlich verbessern kann.
Zitation: Levin, B.R., Gil-Gil, T., Berryhill, B.A. et al. A theoretical exploration of protocols for treating prosthetic joint infections with combinations of antibiotics and bacteriophage. npj Biofilms Microbiomes 12, 51 (2026). https://doi.org/10.1038/s41522-025-00908-2
Schlüsselwörter: Infektion von Gelenkprothesen, Biofilm, Bakteriophagentherapie, Antibiotikaresistenz, mathematische Modellierung