Clear Sky Science · de
Molekulare Einblicke in die Transkriptom-Profilierung aerobes Training induzierter Veränderungen im alternden Skelettmuskel
Warum das für gesundes Altern wichtig ist
Mit zunehmendem Alter verlieren unsere Muskeln allmählich an Masse und Kraft, ein Prozess, der zu Gebrechlichkeit und Verlust der Selbstständigkeit führen kann. Ärztinnen und Ärzte wissen, dass Bewegung älteren Menschen hilft, stärker zu bleiben, aber was sich genau in alternden Muskeln beim Training verändert, war bislang unklar. Diese Studie nutzt eine leistungsfähige Methode zum Auslesen von Genen, um tief in die Muskeln älterer Mäuse zu blicken, die regelmäßig aerobes Laufbandtraining absolvierten, und zeigt, wie Tausende von Genen reagieren und wie diese Veränderungen dazu beitragen können, die Muskelfunktion und sogar die Gehirngesundheit zu erhalten.
Muskeln im späteren Leben: was schiefläuft
Die Forschenden verglichen zunächst Muskeln von „jungen“ Mäusen mit denen deutlich älterer, nicht trainierter Tiere. Ältere Muskeln zeigten große Verschiebungen in der Aktivität von mehr als 40.000 RNA-Molekülen, den Arbeitskopien der Gene in den Zellen. Viele der Veränderungen hingen mit der Maschinerie zusammen, die Kontraktionen ermöglicht, sowie mit der Struktur, die Muskelfasern zusammenhält. Das Muster bestätigt Befunde aus Humanstudien: Mit dem Alter gehen eher die schnellen, leistungsstarken Fasern verloren als die langsameren, ausdauerorientierten, und die Verbindungen zwischen Nerven und Muskeln werden weniger zuverlässig. Außerdem beobachteten sie reduzierte Aktivität in Genen, die elektrische Signale und Energieverbrauch regulieren, was auf einen Rückgang der Effizienz bei Bewegung und Stoffwechsel in alternden Muskeln hindeutet.
Alte Muskeln aufs Laufband schicken
Anschließend untersuchte das Team, was passiert, wenn alte Mäuse acht Wochen lang regelmäßiges Laufbandtraining absolvierten — vergleichbar mit einem Menschen, der in seinen siebziger Jahren eine konstante Geh‑ oder leicht joggende Routine beginnt. Nach diesem aeroben Training zeigten die älteren „Interventions“-Muskeln markante Verschiebungen in der Genaktivität gegenüber untrainierten alten Muskeln. Hunderte Gene wurden stärker aktiviert, darunter viele, die mit der Zelloberfläche, der die Muskelfasern umgebenden extrazellulären Matrix, und mit Signalwegen zusammenhängen, die Entzündungen und Gewebereparatur steuern. Ein zentrales Gen, Slpi, das zerstörerische Enzyme kontrolliert und schädliche Entzündungsreaktionen dämpft, wurde durch das Training stark hochreguliert. Gleichzeitig wurden einige Gene, die am Abbau beschädigter Proteinkomplexe und an Stressantworten beteiligt sind, heruntergefahren, was darauf hindeutet, dass gut trainierte alternde Muskeln weniger internen Stress erfahren könnten.
Neuverdrahtung der Kommunikation zwischen Muskel, Nerven und Körper
Als die Forschenden die trainierten alten Muskeln nicht nur mit alten, sondern auch mit jungen Muskeln verglichen, zeigte sich noch ein anderes Bild. Training im höheren Alter setzte Gene nicht einfach auf ein jugendliches Muster zurück; vielmehr entstand ein eigenständiges, adaptives Profil. Viele aktivierte Gene standen im Zusammenhang mit Nervensignalen, einschließlich Rezeptoren, die an der Kommunikation an Synapsen beteiligt sind — den Kontaktstellen, an denen Nerven mit Muskelfasern und miteinander kommunizieren. Signalwege im Zusammenhang mit Neurotransmitterrezeptoren und Signalübertragung wurden aktiver, was helfen könnte, die neuromuskuläre Verbindung im Alter zu stabilisieren und Koordination sowie Kraft zu unterstützen. Gleichzeitig wurden Gene herunterreguliert, die normalerweise bei Inaktivität der Muskeln oder bei Verlust der Nervenversorgung hochgeschaltet werden, was mit der Vorstellung übereinstimmt, dass regelmäßige Bewegung Disuse‑ und Denervationssignale unterdrückt.
Versteckte Akteure: nicht‑kodierende RNAs und Gewebegerüst
Über klassische proteinkodierende Gene hinaus hebt die Studie mehrere nicht‑kodierende RNAs hervor — kleine RNA‑Moleküle und lange intergene RNAs, die keine Proteine bilden, aber viele andere Gene fein steuern können. Manche dieser RNAs traten nur in alten Muskeln auf, andere stiegen oder fielen als Folge des Trainings und markieren sie als potenzielle Schalter, die steuern, wie Muskeln auf Alterung und Training reagieren. Das Training veränderte außerdem Gene, die mit der extrazellulären Matrix verbunden sind, dem unterstützenden Geflecht um Muskelfasern. Diese Veränderungen könnten dazu beitragen, die physische Integrität des Muskelgewebes zu erhalten, die Kraftübertragung bei Bewegung zu verbessern und die Signalübertragung zwischen Muskel, Knochen, Immunzellen und sogar dem Gehirn zu beeinflussen.
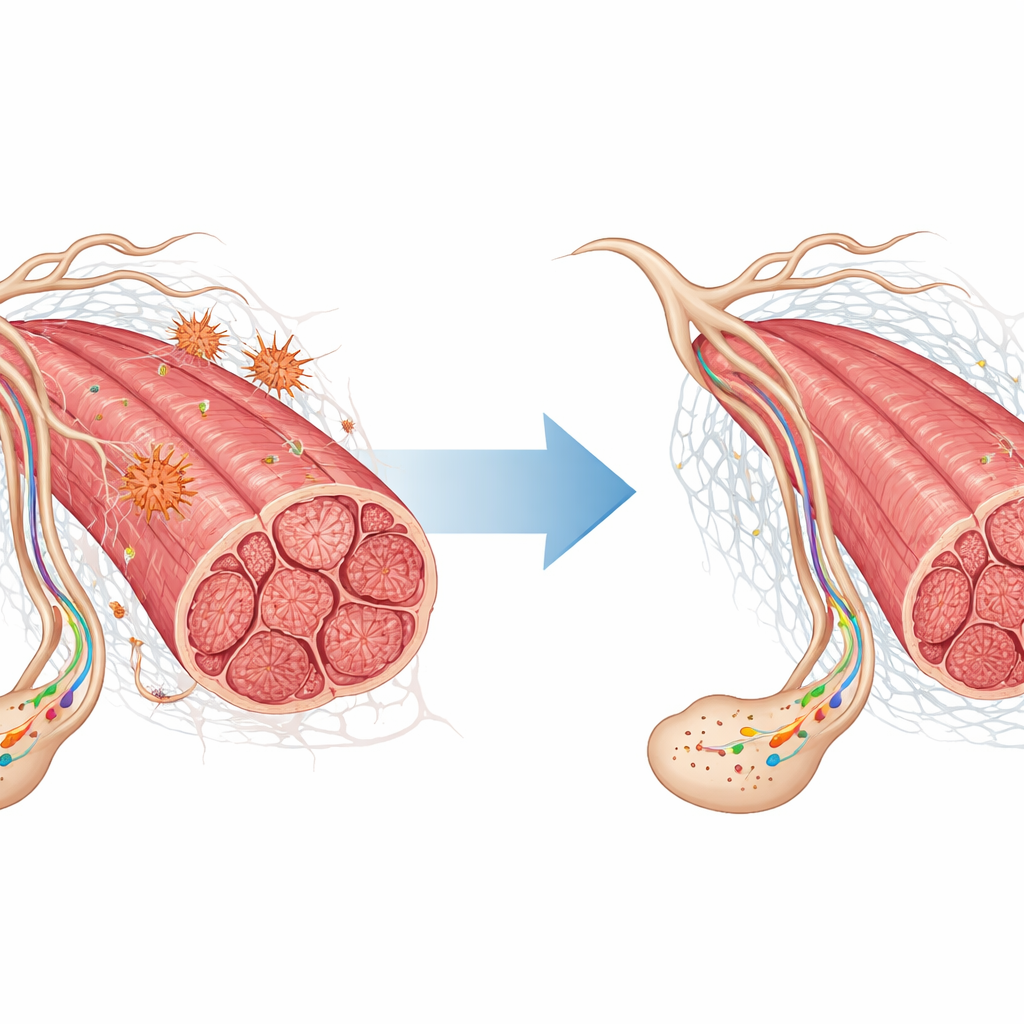
Was das fürs Starkbleiben im Alter bedeutet
Alltagsgemäß zeigt diese Arbeit, dass konsequentes aerobes Training im späteren Leben mehr bewirkt als nur äußere Fitness der Muskeln zu erhalten — es schreibt das molekulare Programm in alternden Muskelzellen um. Die Muster der Genaktivität deuten darauf hin, dass regelmäßiges Training alten Muskeln hilft, schädliche Entzündungen zu dämpfen, ihr strukturelles Gerüst zu stärken, die Nerven‑Muskel‑Kommunikation zu verfeinern und weniger bekannte RNA‑Regulatoren zur Unterstützung der Anpassung heranzuziehen. Obwohl die Studie an männlichen Mäusen durchgeführt wurde und weitere Untersuchungen an Menschen und an weiblichen Tieren notwendig sind, untermauert sie die Botschaft, dass es nie zu spät ist, sich zu bewegen: Regelmäßiges aerobes Training kann tiefgreifende, vorteilhafte Veränderungen in alternden Muskeln anstoßen, die helfen können, Erkrankungen wie Sarkopenie zu bekämpfen und Funktion sowie Lebensqualität zu erhalten.
Zitation: Anwar, M., Kaur, P., Gupta, D. et al. Molecular insight into transcriptome profiling of aerobic exercise induced changes in aged skeletal muscle. npj Aging 12, 45 (2026). https://doi.org/10.1038/s41514-026-00336-2
Schlüsselwörter: Sarkopenie, aerobes Training, Alterung der Skelettmuskulatur, Genexpression, Laufbandtraining