Clear Sky Science · de
Stadien der Bildung biomolekularer Kondensate beim Zusammenbau von Pro‑β‑Carboxysomen
Warum winzige Kohlenstoff‑Fabriken wichtig sind
Die Nahrungsnetze der Erde hängen von der Photosynthese ab, doch das Schlüsselenzym, das Kohlendioxid (CO2) aus der Luft bindet — Rubisco — ist langsam und lässt sich leicht durch Sauerstoff irritieren. Cyanobakterien — mikroskopisch kleine, photosynthetische Mikroben — haben dieses Problem längst gelöst, indem sie proteinbasierte „Mikrofabriken“ bauen, die Carboxysome genannt werden und CO2 um Rubisco herum konzentrieren. Diese Studie entschlüsselt, wie ein entscheidender Adapterkomplex aus den Proteinen ApN und CM schrittweise selbst‑assemblieret, um den Aufbau eines funktionierenden Carboxysoms zu unterstützen. Das Verständnis dieses Ablaufs kann Forschungen leiten, die ähnliche CO2‑verstärkende Systeme in Kulturpflanzen einbauen wollen, um Erträge zu steigern.
Wie Mikroben die Kohlenstoffaufnahme aufladen
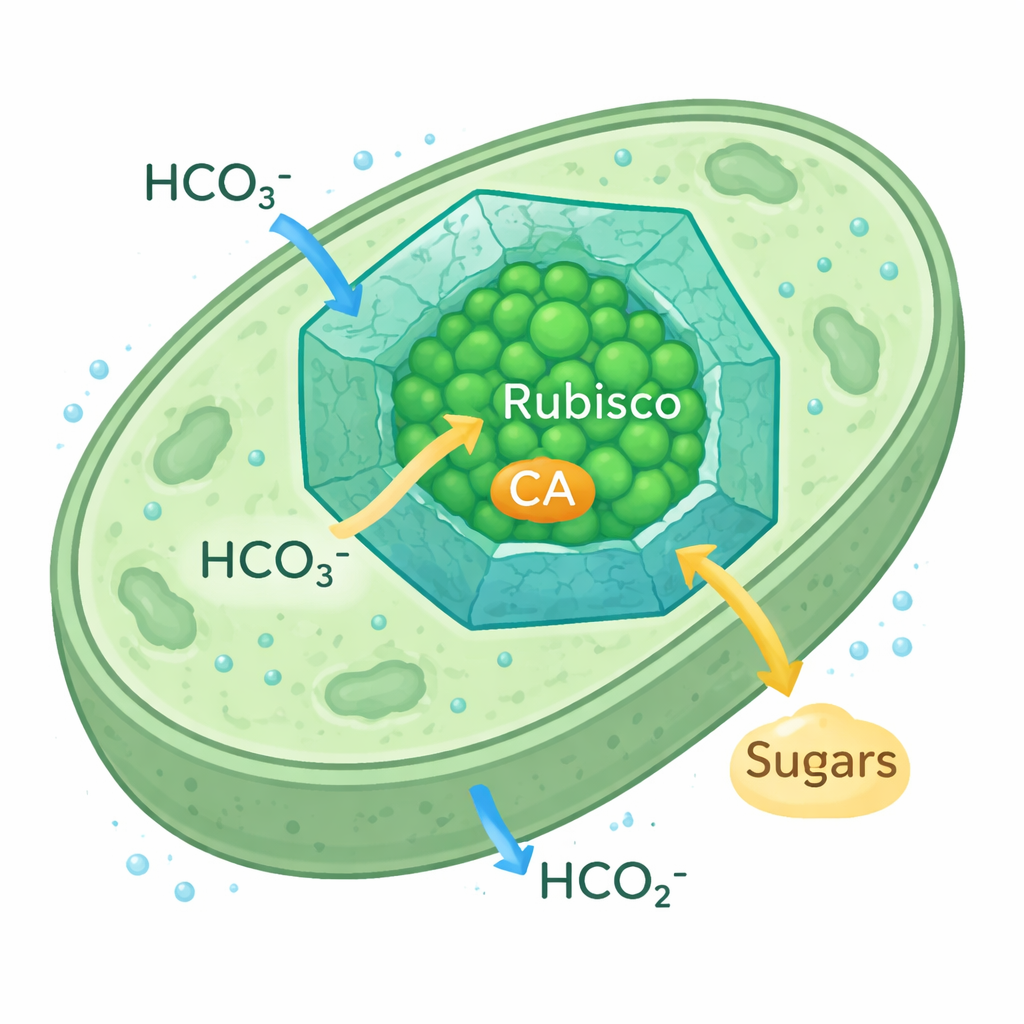
Cyanobakterielle Carboxysome sind winzige, ikosaedrische Proteinkompartimente im Zellinneren. Ihre Proteinhülle lässt Bikarbonat‑Ionen eindringen und verlangsamt gleichzeitig das Entweichen von CO2, wodurch um Rubisco und dessen Partnerenzym, die Karboanhydrase (CA), eine CO2‑reiche Zone entsteht. Dieser CO2‑Konzentrationsmechanismus ermöglicht Cyanobakterien das Gedeihen selbst bei niedrigen Umgebungs‑CO2‑Werten. Da die in diesen Carboxysomen verwendete Rubisco‑Variante der pflanzlichen Rubisco ähnelt, sehen Forscher in ihnen ein realistisches Modell, um Pflanzenchloroplasten für effizientere Kohlenstoffaufnahme umzubauen.
Das Puzzleteil, das mit der Hülle spricht
Bevor sich die harte Proteinhülle bildet, bauen Cyanobakterien zunächst einen weichen, tropfenähnlichen „Pro‑Carboxysom“‑Kondensat. Frühere Arbeiten zeigten, dass ein Gerüstprotein namens CM Rubisco und CA in diesem Tropfen zusammenbringt. Fehlte jedoch die Erklärung, wie der Hüllen‑Adapter ApN sich diesem Gebilde anschließt und später an die Hüllenproteine koppelt. Die Autoren fanden heraus, dass ApN allein eine vierteilige Bündelstruktur bildet, die die anderen Carboxysom‑Komponenten ausschließt. In diesem Zustand kann ApN nicht in Tropfen mit Rubisco, CM und CA gezogen werden, was nahelegt, dass während des echten Carboxysom‑Aufbaus eine andere Form von ApN vorliegen muss.
Gemeinsam gebaute Adapter und ein Redox‑Schalter
Beim Blick auf das genetische Arrangement in Cyanobakterien fiel dem Team auf, dass apn direkt hinter cm im selben Operon liegt, sodass die beiden Proteine üblicherweise zusammen produziert werden. Um dies nachzuahmen, koexprimierten sie ApN und CM aus einem gemeinsamen DNA‑Abschnitt. Unter diesen Bedingungen bildete ApN kein eigenständiges Tetramer mehr. Stattdessen assemblierten sich drei ApN‑Untereinheiten und eine CM‑Untereinheit zu einem spezifischen vierteiligen Adapterkomplex, bezeichnet als (ApN)3:CM. Dieser Hetero‑Komplex setzte sich leicht an Rubisco, CA und CM und konnte sich in Kondensate einfügen. Strukturmodellierung und Kryo‑Elektronenmikroskopie zeigten, dass ApN und CM durch eine fein abgestimmte „Zunge‑und‑Rille“‑Schnittstelle zusammenkommen; wenn Schlüsselreste von ApN in dieser Schnittstelle mutiert wurden, bildete sich der Adapter nicht und die Zellen konnten keine funktionsfähigen Carboxysome aufbauen.
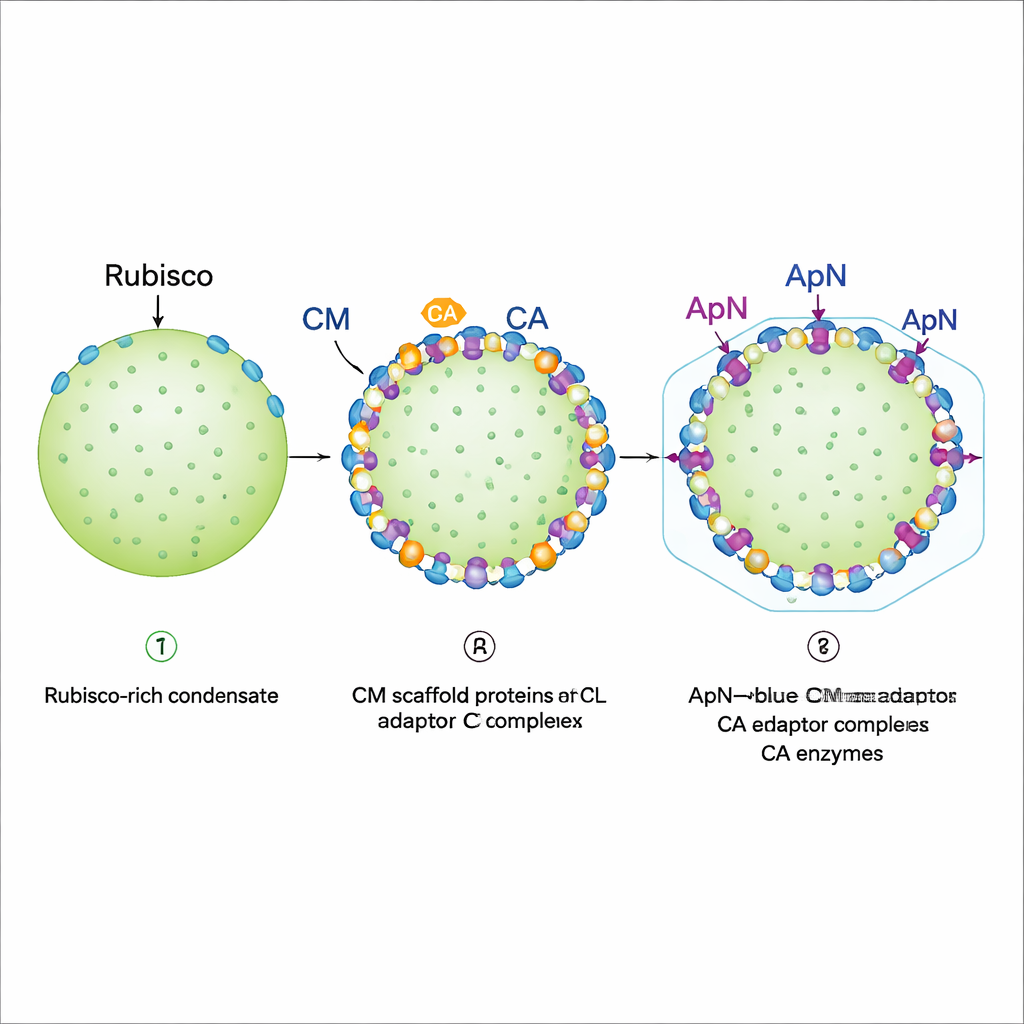
Positionierung am Rand und Vorbereitung für die Hülle
Fluoreszenzbildgebung rekonstituierter Tropfen zeigte ein schrittweises Assemblierungsprogramm. Zuerst bilden Rubisco, voll‑längiges CM und eine kürzere CM‑Variante einen dichten Kondensat, das sich wie ein Gel verhält: Rubisco ist im Wesentlichen fixiert. Danach werden CA und der (ApN)3:CM‑Komplex hinzugefügt. Beide setzen sich bevorzugt an den äußeren Rand des bestehenden Tropfens, vorausgesetzt CA trifft vor oder gleichzeitig mit (ApN)3:CM ein. Diese Randlokalisation ist entscheidend, weil das Schwanzende von ApN ein „Encapsulation Peptide“ trägt, das an Hüllenproteine bindet. Die Autoren entdeckten außerdem einen eingebauten Redox‑Schalter: Während das Innere des reifenden Carboxysoms oxidierender wird, können zwei konservierte Cystein‑Reste in ApN oxidiert werden, wodurch der Adapter von einem (ApN)3:CM‑Tetramer zu einem (ApN)2:CM‑Trimer umgestaltet wird. In lebenden cyanobakteriellen Zellen verlangsamten Veränderungen dieser Cysteine das Wachstum und führten zu übergroßen, aber noch funktionalen Carboxysomen, was ihre Rolle bei der Feinabstimmung der Reifung unterstreicht.
Lehren für den Bau besserer Nutzpflanzen
Für einen Nicht‑Spezialisten mögen diese molekularen Details abstrakt klingen, aber die Botschaft ist einfach: Timing und Partnerschaften sind entscheidend. Die Arbeit zeigt, dass ApN gemeinsam mit CM produziert werden muss, um die Bildung nutzloser Selbst‑Cluster zu vermeiden und stattdessen als Adapter zu dienen, der an der Oberfläche des Pro‑Carboxysoms parkt und bereit ist, die Hülle zu rekrutieren. Ein redox‑sensitiver Schritt hilft dann, diesen Adapter umzubauen, während das Kompartiment sich schließt und sich seine Innenchemie ändert. Für Pflanzeningenieure, die darauf hoffen, cyanobakterielle CO2‑konzentrierende Maschinerie in Nutzpflanzen zu übertragen, hebt die Studie hervor, dass es nicht ausreicht, einzelne Teile zu übertragen; man muss auch die Reihenfolge, Verhältnisse und chemischen Auslöser respektieren, die den Carboxysom‑Aufbau in der Natur steuern.
Zitation: Zang, K., Hong, X., Nguyen, N.D. et al. Stages of biomolecular condensate formation in pro-β-carboxysome assembly. Nat. Plants 12, 447–464 (2026). https://doi.org/10.1038/s41477-026-02227-6
Schlüsselwörter: Carboxysom‑Aufbau, cyanobakterieller CO2‑Konzentrationsmechanismus, Rubisco‑Kondensate, biomolekulare Kondensate, synthetische Photosynthese