Clear Sky Science · de
Mehrschichtige molekulare Profilierung informiert Diagnose und gezielte Therapie des desmoplastischen kleinrunden Zelltumors
Ein seltener Krebs, der bessere Antworten braucht
Der desmoplastische kleinrunde Zelltumor (DSRCT) ist ein extrem seltener und aggressiver Krebs, der vor allem Kinder, Jugendliche und junge Erwachsene trifft. Da er so ungewöhnlich ist und unter dem Mikroskop andere Tumoren nachahmen kann, haben Ärzte oft Schwierigkeiten, ihn korrekt zu diagnostizieren und wirksame Behandlungen auszuwählen. Diese Studie stellt eine einfache, aber kraftvolle Frage: Wenn wir DSRCT-Tumoren auf vielen molekularen Ebenen tiefgehend analysieren — nicht nur DNA, sondern auch RNA, Proteinmuster und chemische Markierungen auf der DNA — können wir dann sowohl die Diagnose schärfen als auch neue, präzisere Behandlungsoptionen für Patientinnen und Patienten entdecken, die bereits alle Standardtherapien ausgeschöpft haben?
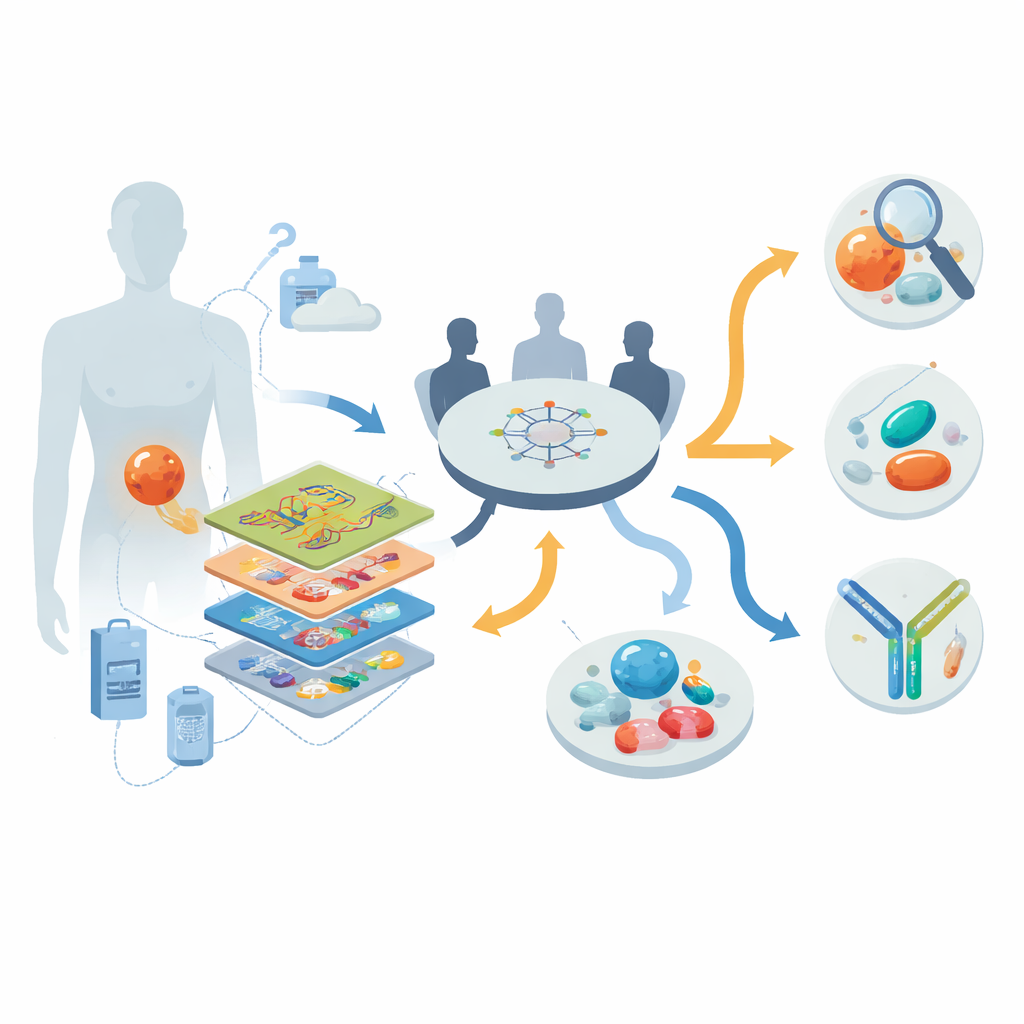
Schicht für Schicht in den Tumor blicken
Die Forschenden arbeiteten im Rahmen eines bundesweiten Präzisionsonkologie-Programms in Deutschland und nahmen zwischen 2013 und 2022 30 Personen mit fortgeschrittenem, meist therapieresistentem DSRCT auf. Für jede Patientin bzw. jeden Patienten setzten sie ein „Multi-Omics“-Werkzeugset ein: Whole-Genome- oder Exomsequenzierung zur Untersuchung der DNA; RNA-Sequenzierung, um zu sehen, welche Gene aktiv sind; DNA-Methylierungsprofiling, um epigenetische Fingerabdrücke zu erfassen; und bei neun Patientinnen bzw. Patienten detaillierte Protein- und Phosphoproteinmessungen, die zeigen, welche Signalwege tatsächlich aktiv sind. Ein multidisziplinäres Tumorboard überprüfte diese Daten zusammen mit der klinischen Vorgeschichte jeder Person, um individualisierte Empfehlungen zur Klärung der Diagnose, zu gezielten Medikamenten und zu klinischen Studien zu erstellen.
Fehldiagnosen korrigieren und verborgene Ziele aufdecken
Ein auffälliges Ergebnis war, wie oft die tiefe Profilierung die ursprüngliche Diagnose korrigierte. Bei acht von 30 Patientinnen bzw. Patienten wurden Tumoren, die zunächst als andere Entitäten — etwa Krebs unklarer Herkunft oder unspezifische Sarkome — klassifiziert worden waren, als DSRCT neu eingestuft, nachdem eine typische Genfusion (EWSR1::WT1) und ein charakteristisches Methylierungsmuster identifiziert worden waren. Gleichzeitig erwies sich die DNA dieser Tumoren als relativ ruhig: Es gab wenige Mutationen und nur gelegentliche Veränderungen in der Kopienzahl, sodass klassische „mutiertes Gen = Arzneimittelziel“-Ansätze wenig ergaben. Stattdessen kamen die reichhaltigsten Hinweise aus den RNA- und Proteinebenen. Durch den Vergleich der Genaktivität in DSRCT mit Hunderten anderer Sarkome fand das Team wiederholt Überexpressionen mehrerer Oberflächenmoleküle und Signal-Enzyme, die prinzipiell mit bestehenden oder in Entwicklung befindlichen Wirkstoffen angegriffen werden könnten.
Von molekularen Signalen zu maßgeschneiderten Behandlungen
Auf der Grundlage dieser Muster gab das Tumorboard 107 molekularinformierte Managementvorschläge für 28 der 30 Patientinnen bzw. Patienten heraus. Die meisten Empfehlungen betrafen Medikamente, die Tyrosinkinasen blockieren — Schlüsselenzyme, die Zellwachstum und Gefäßbildung antreiben — oder neuere Strategien, die an stark exprimierte Oberflächenproteine binden. Beispiele waren kleine Kinase-Inhibitoren wie Pazopanib; peptidbasierte Radioaktivitätsansätze, die auf Somatostatinrezeptoren abzielen; experimentelle CAR-T-Zellen gegen das Adhäsionsmolekül CLDN6; und Antikörper–Wirkstoff-Konjugate, die Toxine an Zellen mit dem ERBB2(HER2)-Rezeptor liefern. Siebzehn Patientinnen bzw. Patienten wurden als geeignet für biomarkerabgestimmte klinische Studien eingestuft, was verdeutlicht, wie detaillierte molekulare Daten den Zugang zu Studien eröffnen können, die für Menschen mit einer extrem seltenen Erkrankung sonst schwer zugänglich wären.
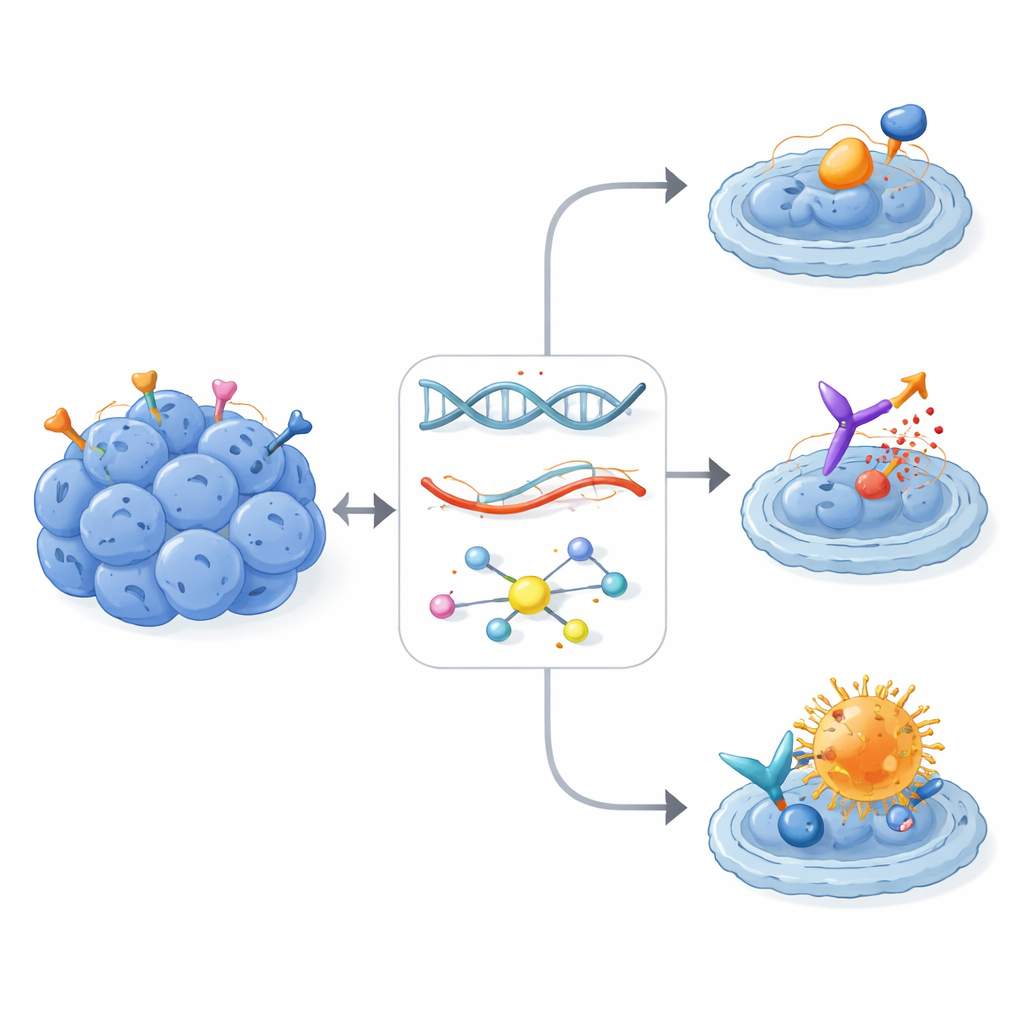
Reale Wirkung bei stark vorbehandelten Patientinnen und Patienten
Von allen empfohlenen personalisierten Therapien wurden 16 tatsächlich bei 13 Patientinnen bzw. Patienten angewendet, alle geleitet von RNA-Signalen und teils verfeinert durch Phosphoprotein-Daten. Obwohl diese Personen bereits mehrere Zyklen Chemotherapie und lokale Behandlungen durchlaufen hatten, erreichten acht der 13 eine Krankheitskontrolle — fünf mit teilweiser Tumorverkleinerung und drei mit stabiler Erkrankung. Multi-Target-Tyrosinkinase-Inhibitoren, am häufigsten Pazopanib, brachten bei mehreren Patientinnen bzw. Patienten einen bedeutsamen und teils langanhaltenden Nutzen, besonders wenn die bekannten Ziele des Wirkstoffs im Tumor deutlich überaktiv waren. Besonders bemerkenswert waren zwei Patientinnen bzw. Patienten mit hoher ERBB2-Expression, die das Antikörper–Wirkstoff-Konjugat Trastuzumab Deruxtecan (T-DXd) erhielten. Beide zeigten anhaltende Ansprechen über bis zu zwei Jahre oder länger, obwohl sie viele vorherige Therapielinien ausgeschöpft hatten und obwohl der ERBB2-Rezeptor nicht das starke Aktivierungsmuster zeigte, das typischerweise für klassische ERBB2-blockierende Medikamente verlangt wird.
Was das für Patientinnen und Patienten und die zukünftige Versorgung bedeutet
Für Menschen mit DSRCT liefert die Studie eine verhalten optimistische Botschaft. Obwohl dieser Krebs wenige offensichtliche DNA-Mutationen bietet, die sich ausnutzen lassen, kann ein Blick über mehrere molekulare Ebenen sowohl Fehldiagnosen korrigieren als auch verwertbare Schwachstellen aufdecken, die Standardtests verborgen bleiben. Die Arbeit zeigt, dass selbst bei einer seltenen und aggressiven Erkrankung ein biologiebasierter Ansatz echten klinischen Nutzen bringen kann, einschließlich dauerhafter Ansprechen auf Wirkstoffe wie Pazopanib und Trastuzumab Deruxtecan. Breiter gedacht plädiert sie dafür, Patientinnen und Patienten mit DSRCT — und übertragbar auf andere ultrarelle Krebserkrankungen — routinemäßigen Zugang zu umfassendem molekularem Profiling und fachlicher Begutachtung zu gewähren, was den Weg für künftige Studien ebnet, in denen Therapien nicht allein nach Tumortyp, sondern nach den einzigartigen molekularen Fingerabdrücken des jeweiligen Tumors ausgewählt werden.
Zitation: Renner, M., Oleś, M., Paramasivam, N. et al. Multi-layered molecular profiling informs the diagnosis and targeted therapy of desmoplastic small round cell tumor. Nat Commun 17, 3397 (2026). https://doi.org/10.1038/s41467-026-71636-0
Schlüsselwörter: desmoplastischer kleinrunder Zelltumor, Präzisionsonkologie, Multi-Omics-Profiling, gezielte Therapie, Antikörper-Wirkstoff-Konjugate