Clear Sky Science · de
Wechselspiel zwischen SLC33A1‑abhängiger und -unabhängiger Golgi‑O‑Acetylierung von Sialinsäure in der CASD1‑Katalyse
Wie winzige Zucker‑Modifikationen Gesundheit und Krankheit prägen können
Unsere Zellen sind mit komplexen Zuckerketten überzogen, die wie molekulare Ausweise wirken und Immunität, Entwicklung und sogar die Anheftung von Viren steuern. Diese Studie untersucht eine subtile, aber wirkungsvolle Modifikation dieser Zucker — das Anfügen kleiner chemischer „Kappen“, sogenannter Acetylgruppen, an eine terminale Zuckerstruktur namens Sialinsäure — und enthüllt eine überraschende zweiteilige molekulare Maschine, die diesen Prozess im Golgi‑Apparat der Zelle steuert. Das Verständnis dieses verborgenen Systems hilft, bestimmte schwere neurologische Erkrankungen zu erklären, und liefert Hinweise darauf, wie Zellen ihre Oberflächen in Gesundheit und Krankheit feinabstimmen. 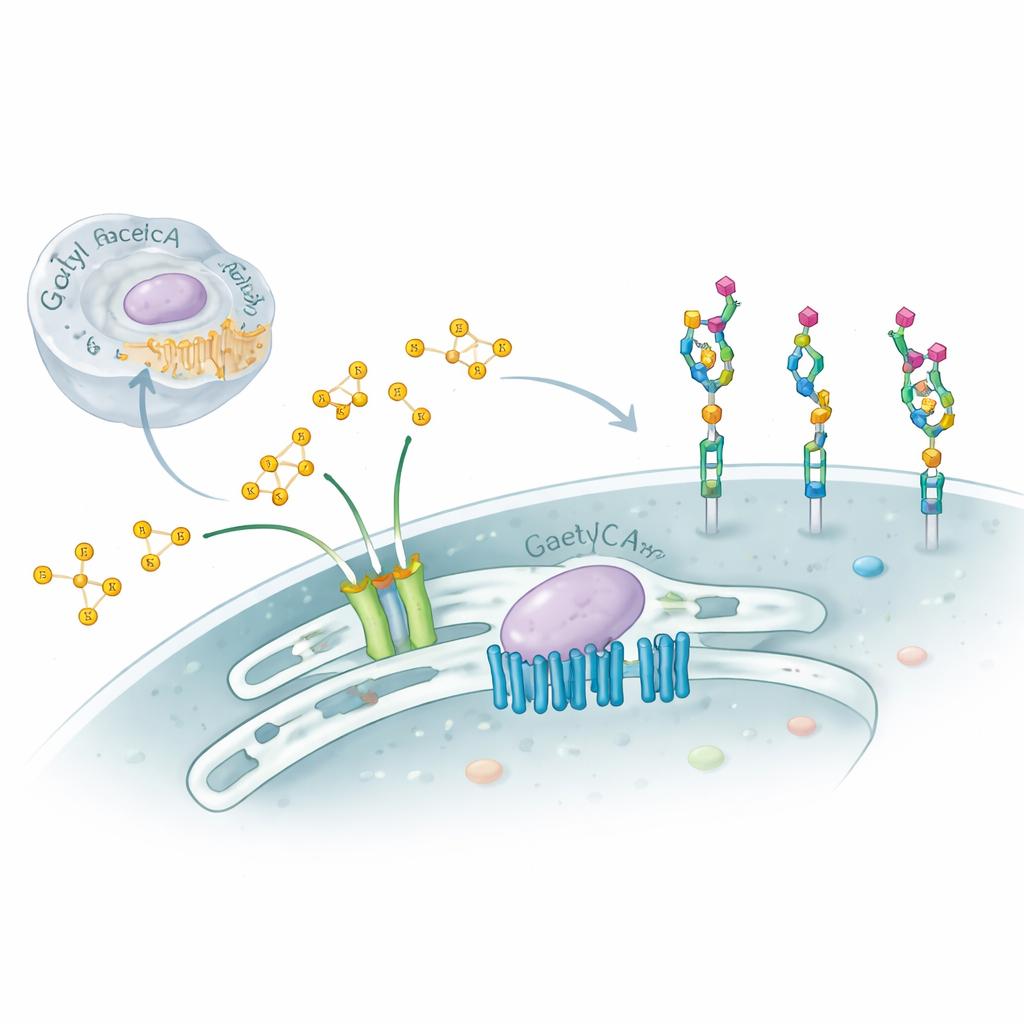
Die besonderen Zucker auf der Zelloberfläche
Sialinsäuren sitzen an den äußeren Enden vieler zelloberflächlicher Zuckerketten auf Proteinen und Lipiden, insbesondere auf den im Gehirn vorkommenden Molekülen, den Gangliosiden. Durch geringe Veränderungen an Sialinsäuren — etwa das Anhängen einer oder zweier Acetylgruppen an spezifischen Positionen — können Zellen bestehende Erkennungsstellen überdecken oder neue schaffen. Viren wie Influenza C und einige Coronaviren suchen gezielt nach diesen modifizierten Zuckern, und acetylierte Ganglioside können beeinflussen, ob Nervenzellen überleben oder absterben sowie wie Tumoren wachsen. Trotz ihrer Bedeutung waren die inneren Mechanismen der zellulären Maschinerie, die diese Acetylgruppen im Golgi anbringt, lange schlecht verstanden.
Ein Transporter und ein Enzym arbeiten Hand in Hand
Die Forschenden konzentrierten sich auf zwei Proteine, die im oder am Golgi sitzen: SLC33A1, ein Transporter, der Acetyl‑CoA (den Hauptacetylspender der Zelle) über Membranen befördert, und CASD1, ein Enzym, das dafür bekannt ist, Acetylgruppen auf Sialinsäuren zu übertragen. Mithilfe von Geneditierung in menschlichen und Hamster‑Zelllinien entfernten sie SLC33A1 und beobachteten, was mit bestimmten Gangliosiden geschah. Zellen ohne SLC33A1 konnten weiterhin die Grundganglioside GD3 und GD2 herstellen, verloren jedoch vollständig ihre 9‑O‑acetylierten Formen — eine charakteristische Modifikation, die mit Krebs und neuronaler Funktion in Verbindung steht. Die Wiedereinführung humanen SLC33A1 stellte diese acetylierten Ganglioside wieder her und zeigte damit, dass SLC33A1 ein entscheidender Lieferant von Acetyl‑CoA für diesen Weg ist. 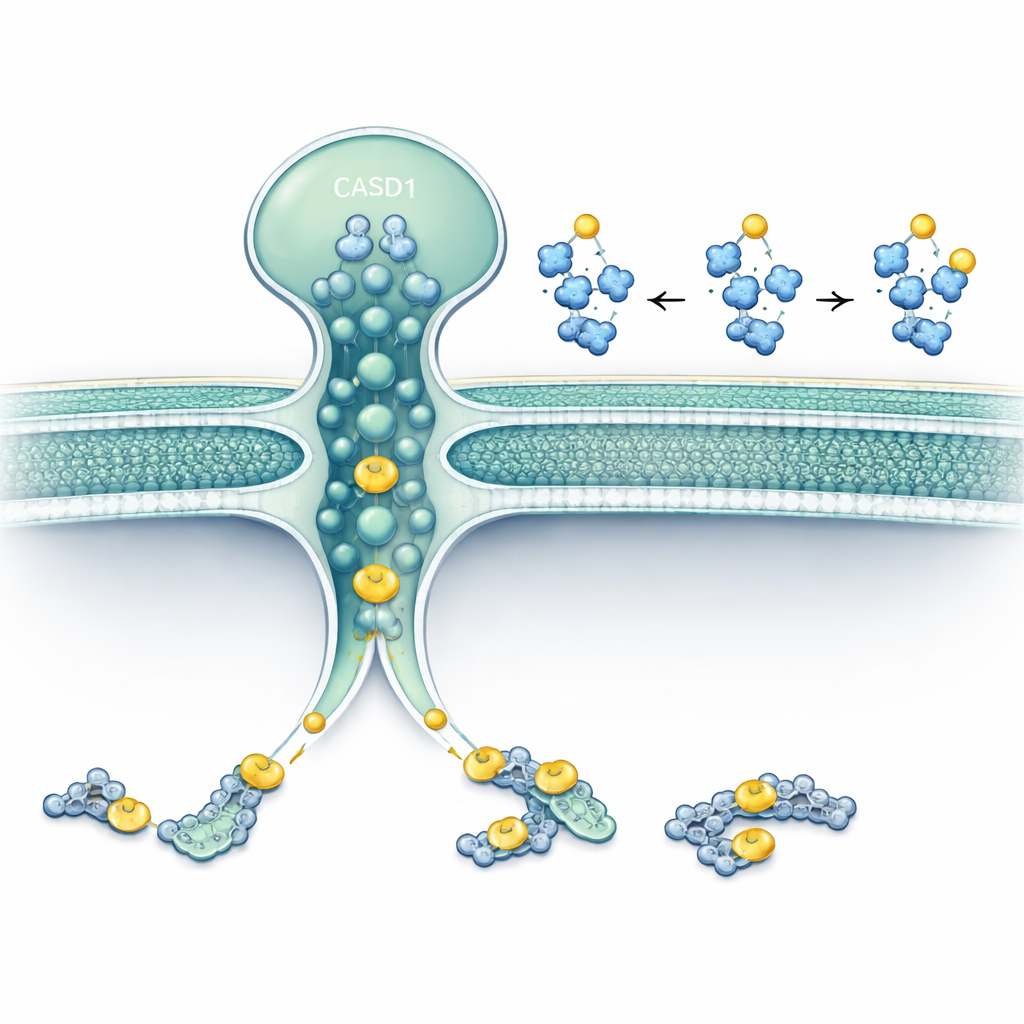
Patientenmutationen offenbaren medizinische Relevanz
SLC33A1 wurde mit mehreren seltenen neurologischen Erkrankungen in Verbindung gebracht, darunter eine schwere Kindheitserkrankung (Huppke–Brendel‑Syndrom), eine Form der hereditären spastischen Paraplegie und eine spät einsetzende zerebelläre Ataxie. Das Team rekonstruierte vier patientenstammende SLC33A1‑Varianten in Zellen, denen der normale Transporter fehlte, und prüfte, ob diese veränderten Proteine die Gangliosidacetylierung wiederherstellen konnten. Alle vier zeigten reduzierte Funktion, und die schwersten, im Kindesalter auftretenden Mutationen stellten kaum noch Acetylierung her. Anhand einer kürzlich gelösten dreidimensionalen Struktur von SLC33A1 setzten die Autorinnen und Autoren diese Mutationen in das Protein und zeigten, wie sie wahrscheinlich dessen Architektur oder die Fähigkeit zur Bindung von Acetyl‑CoA stören. Das legt nahe, dass beeinträchtigte Gangliosidacetylierung zu den neurologischen Symptomen bei betroffenen Patientinnen und Patienten beiträgt.
Eine verborgene zweite aktiven Stelle in CASD1
Die Arbeit förderte außerdem eine unerwartete Wendung zutage: CASD1 scheint selbst ein doppelfunktionales Enzym zu sein. Sein bekannter Anteil im Golgi‑Lumen nutzt Acetyl‑CoA, das von SLC33A1 geliefert wird. Wenn SLC33A1 jedoch ausgeschaltet war, gelang es den Zellen unter bestimmten Bedingungen dennoch, eine einzelne Acetylgruppe an bestimmte Sialinsäuren anzubringen, während die Hinzufügung der zweiten Acetylgruppe für komplexere Muster ausblieb. Mithilfe fortgeschrittener Strukturvorhersage und molekularer Simulationen zeigten die Autorinnen und Autoren, dass der membranüberspannende Teil von CASD1 einem bekannten transmembranen Acetyltransferase‑Protein aus Lysosomen stark ähnelt. Sie identifizierten Schlüsselaminosäuren in diesem Bereich, die Acetyl‑CoA auf der zytosolischen Seite binden und dessen Acetylgruppe direkt durch die Membran an die Sialinsäure weiterreichen. Bei Mutation dieser Rückstände verlor CASD1 diese zweite Aktivität sowohl in In‑vitro‑Assays als auch in lebenden Zellen.
Zwei Wege, ein fein abgestimmter Zuckercode
Zusammen stützen die Daten ein Modell mit „zwei katalytischen Stellen“. Der eine Weg hängt davon ab, dass SLC33A1 Acetyl‑CoA in das Golgi‑Lumen bringt, wo die luminale Domäne von CASD1 eine Acetylgruppe auf Sialinsäure anbringt und so sowohl einfache als auch doppelte Acetylierungsmuster ermöglicht. Der andere Weg ist im membranüberspannenden Kern von CASD1 angelegt, der direkt auf zytosolisches Acetyl‑CoA zugreift und selbst dann noch ein Basisniveau an Acetylierung durchführen kann, wenn SLC33A1 fehlt. Für Laien bedeutet das: Ein einziges Enzym, gespeist aus zwei verschiedenen Acetylquellen, schreibt feine „Satzzeichen“ auf die zelloberflächlichen Zucker. Wenn der Transporter oder ein Teil des Enzyms ausfällt, sind diese Markierungen fehlplatziert oder fehlen — das könnte bestimmte neuro‑entwicklungsbedingte und neurodegenerative Erkrankungen erklären und zeigt eine neue Ebene der Regulation, wie Zellen ihre äußere Identität formen.
Zitation: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
Schlüsselwörter: Sialinsäure, Golgi‑Acetylierung, Ganglioside, SLC33A1, CASD1