Clear Sky Science · de
Das ribosom‑assoziierte N‑terminal‑Acetyltransferase B koordiniert die globale Proteostase und Autophagie in Pflanzen durch Erzeugung von Ac/N‑Degrons
Wie Pflanzen ihre Proteine im Gleichgewicht halten
Jede Zelle einer Pflanze ist vollgepackt mit Proteinen, die ständig neu hergestellt, repariert und entfernt werden müssen. Wenn dieses Gleichgewicht gestört ist, verlangsamt sich das Wachstum und Stress kann tödlich werden. Diese Studie zeigt, wie ein winziger chemischer Aufsatz am Anfang vieler Proteine Pflanzen dabei hilft zu entscheiden, welche Proteine schnell recycelt werden sollen und wie stark ein interner Reinigungsprozess namens Autophagie aktiviert wird. Das Verständnis dieses Kontrollsystems erklärt, wie Pflanzen lange Perioden ohne Licht oder Nährstoffe überstehen, und könnte eines Tages helfen, Kulturpflanzen zu züchten, die härtere Bedingungen besser ertragen.
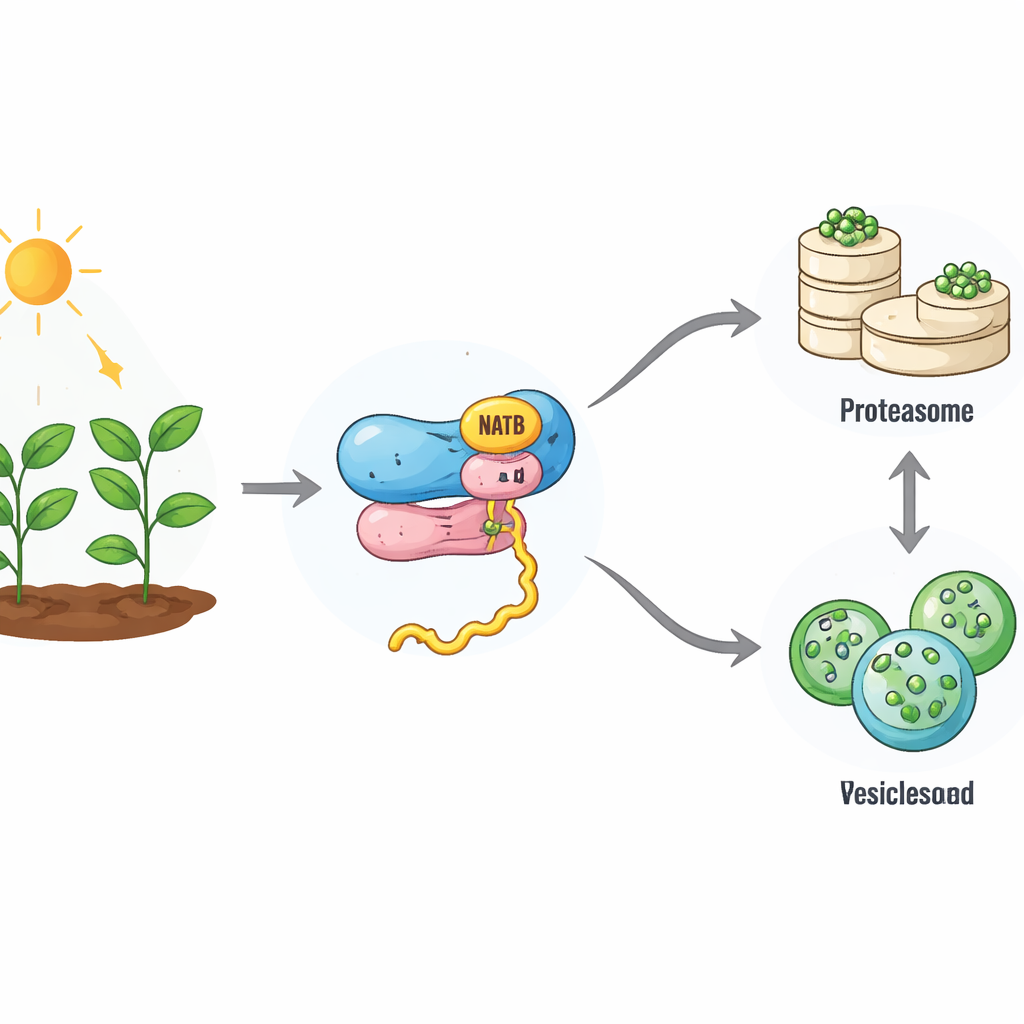
Ein kleiner Aufsatz mit großen Folgen
Wenn neue Proteine an Ribosomen entstehen, können sie an ihrem Anfang durch eine chemische Gruppe „abgedeckt“ werden. Bei Pflanzen fügt ein ribosom‑gebundenes Enzymkomplex namens NatB diesen Aufsatz bei etwa einem Fünftel aller Proteine an. Bislang war nicht vollständig geklärt, was diese weitverbreitete Markierung für das Schicksal dieser Proteine bedeutet. Mithilfe von CRISPR‑Geneditierung, um den katalytischen Teil von NatB in Arabidopsis auszuschalten, erzeugten die Autoren Pflanzen, denen diese Modifikation an den üblichen NatB‑Zielen weitgehend fehlt. Überraschenderweise waren diese Pflanzen verkümmert, überlebten aber, im Gegensatz zu NatB‑defizienten Tieren, was darauf hindeutet, dass Pflanzenzellen den Verlust teilweise kompensieren können. Dennoch waren viele Proteine, die normalerweise das NatB‑Tag tragen, nur teilweise oder gar nicht modifiziert, wodurch sich ein Einblick in die Funktionsweise dieses Systems ergibt.
Langsamere Proteinumsatzraten und eine Verschiebung im zellulären Recycling
Als das Team maß, wie schnell Proteine abgebaut werden, stellten sie fest, dass NatB‑defiziente Pflanzen eine verlangsamte zelluläre Recyclingmaschinerie aufweisen. Der Hauptweg des Proteinabbaus, das Ubiquitin‑Proteasom‑System, arbeitete weniger effizient: seine Aktivität nahm ab und Proteine, die auf diesem Weg abgebaut werden sollten, trugen weniger der üblichen „vernichte mich“‑Markierungen. Gleichzeitig sank auch die Gesamtgeschwindigkeit der neuen Proteinproduktion. Detaillierte Proteomstudien zeigten, dass viele NatB‑abhängige Proteine nun stabiler waren und sich in der Zelle anhäuften, was darauf hindeutet, dass das NatB‑Tag normalerweise hilft, bestimmte Proteine kurzlebig zu machen. Doch nicht alle NatB‑Ziele verhielten sich so — das deutet auf einen selektiveren Effekt hin, der von der Sequenz und dem Kontext jedes Proteins geprägt ist.
Autophagie springt als Backup ein
Die Studie zeigte, dass, wenn der Proteasom‑Weg langsamer wird, ein anderer Recyclingweg hochfährt. Dieses zweite System, die Autophagie, umschließt zelluläre Abschnitte in Membranenblasen, die zu einem Kompartiment geliefert werden, in dem die Inhalte abgebaut und wiederverwendet werden. NatB‑defiziente Pflanzen wiesen höhere Spiegel von Kernproteinen der Autophagie und einen stärkeren Fluss von Material durch diesen Weg auf, besonders in der Dunkelheit, wenn Energie knapp ist. Pflanzen ohne NatB überlebten deutlich länger unter lang anhaltender Dunkelheit oder bei Stickstoff‑ und Schwefelmangel als normale Pflanzen, doch dieser Vorteil verschwand, wenn Autophagie‑Gene ausgeschaltet wurden. Das deutet darauf hin, dass die verstärkte Autophagie hilft, das geschwächte Proteasom‑System zu kompensieren und die Proteinökonomie der Zelle vor dem Zusammenbruch zu bewahren.
Ein zentraler Energiesensor im Zentrum des Umschaltens
Um zu verstehen, was das Gleichgewicht von der Nutzung des Proteasoms hin zur Autophagie kippt, konzentrierten sich die Autoren auf einen Energie‑sensorischen Proteinkomplex namens SnRK1. Zwei eng verwandte Untereinheiten, KIN10 und KIN11, beginnen mit Sequenzen, die sie zu wahrscheinlichen NatB‑Substraten machen. Die Forscher zeigten, dass NatB diese Proteine in Test‑Röhrchen‑Assays direkt markieren kann. In Pflanzen ohne NatB sammelte sich nur KIN11 stark an, und seine aktive, phosphorylierte Form war häufiger vorhanden. Sorgfältige Verfolgung des Proteinabbaus ergab, dass KIN11, wenn es das NatB‑Tag trägt, eher für die Zerstörung durch das Proteasom markiert wird, während unmarkiertes KIN11 bestehen bleibt. Pflanzen, denen sowohl NatB als auch KIN11 fehlten, verloren ihre zusätzliche Dunkelheits‑Stressresistenz, während Pflanzen, die so verändert wurden, dass sie nur KIN11 überproduzieren, toleranter gegenüber langer Dunkelheit wurden. Diese Ergebnisse machen KIN11 zu einem entscheidenden Botenstoff, der, wenn er stabilisiert ist, die Zelle dazu bringt, Autophagie und Energiesparen zu bevorzugen.
Was das für das Überleben von Pflanzen bedeutet
Kurz gesagt: NatB schreibt ein entfernbares „Benutzen‑und‑Wegwerfen“‑Kennzeichen auf spezifische Proteine, einschließlich des Energiesensors KIN11. Wenn NatB aktiv ist, wird KIN11 in Schach gehalten, der Proteinumsatz über das Proteasom ist flott, und Pflanzen wachsen unter guten Bedingungen schnell. Wenn die NatB‑Aktivität verloren geht oder reduziert wird, bleibt KIN11 von schneller Zerstörung verschont, die Autophagie wird hochgefahren, und Pflanzen schalten in einen Überlebensmodus um, der Ressourcen spart und besser mit langen Perioden von Dunkelheit oder Nährstoffmangel zurechtkommt. Diese Arbeit enthüllt NatB als zentralen Koordinator zwischen zwei wichtigen Recycling‑Systemen in Pflanzenzellen und erklärt, wie ein feiner chemischer Aufsatz am Beginn eines Proteins das Gleichgewicht zwischen Wachstum und Ausdauer verschieben kann.
Zitation: Gong, X., Pożoga, M., Boyer, JB. et al. The ribosome-associated N-terminal acetyltransferase B coordinates global proteostasis and autophagy in plants by creating Ac/N-degrons. Nat Commun 17, 3116 (2026). https://doi.org/10.1038/s41467-026-71208-2
Schlüsselwörter: Protein‑Qualitätskontrolle, Autophagie, Pflanzenstress‑Toleranz, posttranslationale Modifikation, Proteinabbau