Clear Sky Science · de
Strukturelle Dynamik des Midnolin‑Proteasoms während des ubiquitinunabhängigen Substratabbaus
Wie Zellen den Abfall schnell loswerden
In jeder Zelle werden Proteine ständig hergestellt und wieder abgebaut. Viele werden vor dem Einlass in die zelluläre Hauptrecyclingmaschine, das Proteasom, mit kleinen Molekülen namens Ubiquitin markiert. Manche nukleären Proteine müssen jedoch so schnell entfernt werden, dass keine Zeit für eine Markierung bleibt. Diese Studie zeigt, wie ein wenig bekanntes Helferprotein, Midnolin, direkt an das Proteasom andockt, um diese dringenden Zielproteine zu entfernen, und liefert damit Hinweise darauf, wie Zellen die Genaktivität schnell und präzise regulieren.
Eine Abkürzung zum zellulären Schredder
Das 26S‑Proteasom ist ein tonnenförmiger Komplex, der Proteine in kleine Stücke zerkleinert. Klassisch erkennt es Ziele, indem es an ihnen aneinander gereihte Ubiquitinmoleküle abliest. Jüngere Arbeiten haben jedoch einen alternativen Weg aufgezeigt: eine „Abkürzung“, bei der Midnolin bestimmte nukleäre Proteine — vor allem Produkte sofort‑früher Gene, die Gene rasch an‑ und ausschalten — direkt ohne Ubiquitinanhang zum Proteasom geleitet. Solche Proteine, etwa Transkriptionsfaktoren für Stressreaktionen und Entzündungen, müssen innerhalb von Minuten erscheinen und wieder verschwinden. Das neue Papier kombiniert hochaufgelöste Kryo‑Elektronenmikroskopie mit biochemischen Experimenten, um nahezu Bild‑für‑Bild zu kartieren, wie Midnolin am Proteasom andockt und seine Ladung zur Zerstörung positioniert.
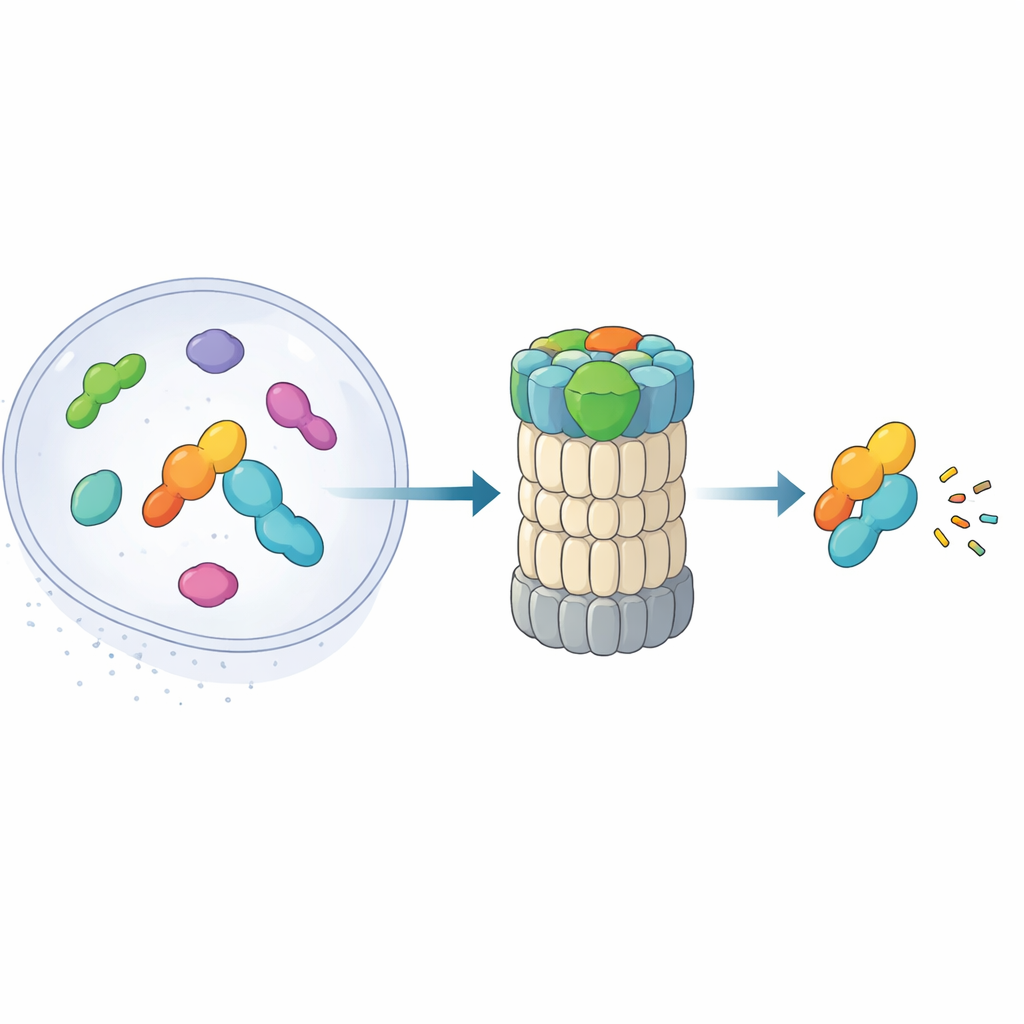
Der dreiteilige Helfer, der Ziele greift und ausrichtet
Midnolin funktioniert wie ein Multitool mit drei Schlüsselmodulen. Ein Ende, eine C‑terminale Helix, steckt in einer Andockstelle einer Proteasomkomponente namens RPN1 und verankert Midnolin an der Recyclingmaschine. Eine zentrale „Catch“-Region erkennt und greift ein spezifisches strangartiges Merkmal (ein Degron) in den Zielproteinen. Am gegenüberliegenden Ende befindet sich eine ubiquitinähnliche Domäne. Überraschenderweise dient diese Domäne hier nicht primär der Proteasombindung, wie es bei ähnlichen Shuttle‑Proteinen der Fall ist. Stattdessen legen die Autoren dar, dass sie an RPN11 anliegt, ein Enzym, das normalerweise Ubiquitin von Substraten abschneidet. Hier wirkt RPN11 eher wie ein Gerüst: Indem es Midnolins ubiquitinähnlichen Abschnitt umschließt, hilft es dabei, die Catch‑Region und ihre gebundene Ladung direkt über dem engen Eintrittspore des Proteasoms zu positionieren.
Das Protein in den Mahlkern führen
Sobald Midnolin andockt, übernimmt der energiehungrige Motor des Proteasoms — ein AAA+‑ATPase‑Ring — die Arbeit. Dieser Ring sitzt direkt unter der Eintrittspore und zieht entfaltetete Proteinketten schrittweise in das Innere. Die Kryo‑EM‑Schnappschüsse zeigen eine Reihe von „Spiral‑Treppen“-Positionen, die die sechs Untereinheiten des Motors einnehmen, während sie das Substrat greifen und durch den zentralen Kanal weiterreichen. Die Autoren haben vier aufeinanderfolgende Stadien dieses Zyklus eingefangen, alle mit Midnolin‑gebundenem Material, das durch die Pore gefädelt ist, und beobachteten sogar, wie die Freisetzung eines Magnesiumions in einer Untereinheit mit einer Abwärtsbewegung des gesamten Rings zusammenfällt. Das legt nahe, dass koordinierter ATP‑Verbrauch und Magnesiumfreisetzung das Protein stufenweise tiefer in die Kammer ratchetieren, in der die Schnittstellen liegen.
Warum Positionierung und Koexpression wichtig sind
Das Team untersuchte, wie jedes Midnolin‑Modul zur Effizienz beiträgt. Die verankernde Helix allein kann RPN1 binden, erhöht aber die Proteasomaktivität nicht wesentlich. Das Entfernen der Catch‑Domäne lässt viele Proteasome in einem untätigen, substratfreien Zustand verharren, obwohl Midnolin weiterhin anheften kann; das Ersetzen der Catch‑Region durch ein dauerhaft angefügtes Substrat stellt die volle Aktivität ebenfalls nicht wieder her. Diese Befunde deuten darauf hin, dass Catch mehr tut als nur das Ziel zu greifen — sie muss das Protein auch präzise am Poreingang ausrichten. Biochemische Daten und Tumor‑Transkriptomdaten zeigen zudem, dass Midnolin häufig zusammen mit seinen Substraten produziert wird. Bei Koexpression faltet Midnolin besser und bildet stabile Komplexe, wodurch ein fertiges „Abbaue mich“-Paket entsteht, das bei Bedarf rasch an das Proteasom geliefert werden kann, wenn die Zelle die Genexpression zurücksetzen muss.
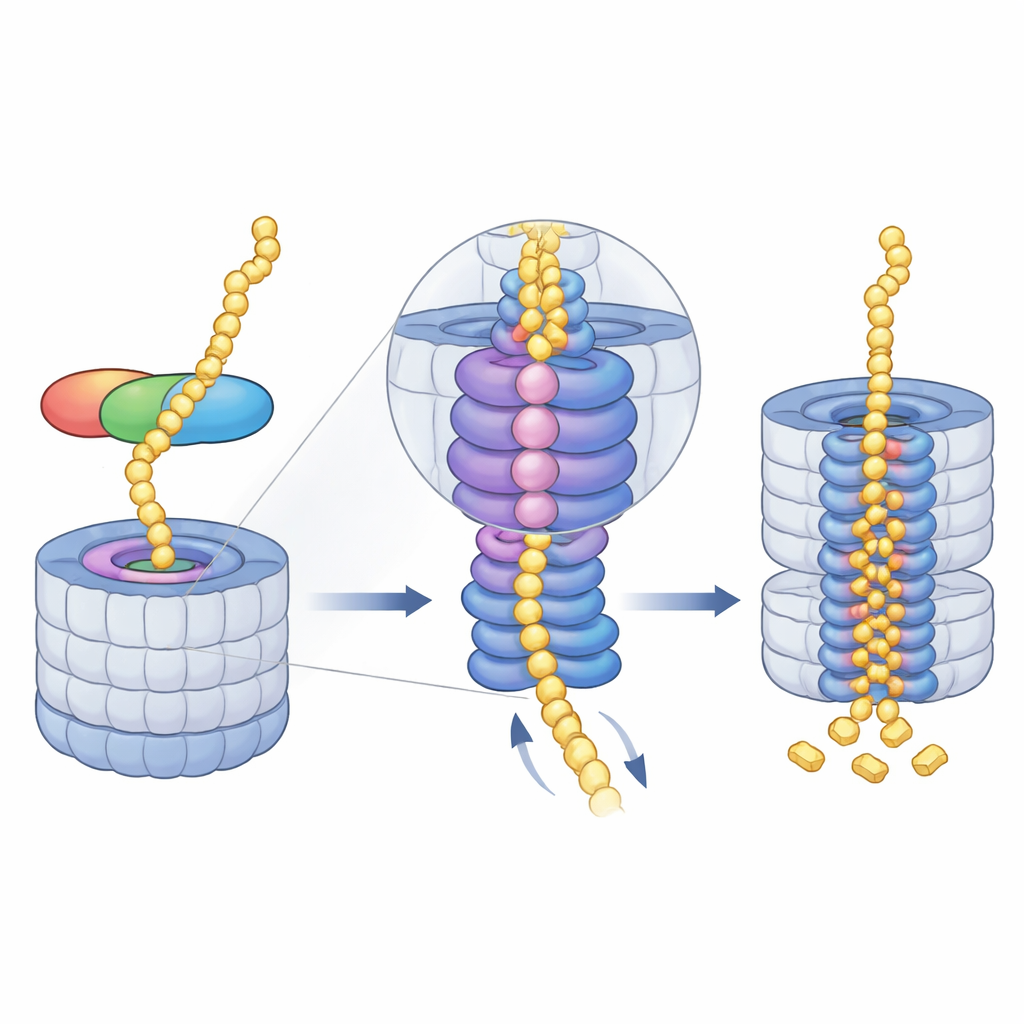
Selbstreinigung und mögliche medizinische Perspektiven
Nachdem das Zielprotein hineingezogen und zerkleinert wurde, bleibt Midnolin selbst nicht verschont. Seine eigenen ungeordneten Regionen können in den Motor eingefädelt und in dieselbe Zerstörungskammer geführt werden, wodurch verhindert wird, dass der Helfer sich unnötig anreichert. Indem diese ubiquitinfreie Route zum Proteasom beleuchtet wird, erweitert die Studie unser Verständnis dafür, wie Zellen Proteinlebensdauern unter sehr engen Zeitvorgaben steuern. Sie deutet auch auf neue therapeutische Strategien hin: Durch das Konstruieren von Midnolin‑basierten Molekülen, die krankheitsverursachende nukleäre Proteine direkt ans Proteasom binden, könnten Forscher eines Tages „unbehandelbare“ Ziele, einschließlich bestimmter Krebsfaktoren, schneller und selektiver eliminieren.»
Zitation: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
Schlüsselwörter: Proteasom, Midnolin, Proteinabbau, ubiquitinunabhängiger Weg, Sofort‑früh‑Gene