Clear Sky Science · de
Transkriptionelle Kompetenz bestimmt das heterochromatische Nukleationspotenzial isolierter MSR‑Einheiten
Verborgene Schalter in unserer DNA
Unsere Genome sind im Zellkern in zwei Hauptzuständen verpackt: aktive Regionen, die Gene beherbergen, und dicht gepackte Abschnitte, die lange Zeit als genetische „Dunkelmaterie“ betrachtet wurden. Diese Studie stellt eine trügerisch einfache Frage: Was veranlasst einen DNA‑Abschnitt, zunächst dieses eng gepackte, gen‑stille Material – bekannt als Heterochromatin – zu werden? Durch die Untersuchung einer spezifischen Klasse repetitiver DNA in Mäusen zeigen die Autorinnen und Autoren, dass nicht alle Wiederholungen gleich sind: Nur diejenigen, die eine besondere Form der Transkription unterstützen, können den Schalter umlegen, der solche stillen DNA‑Nachbarschaften aufbaut und erhält.
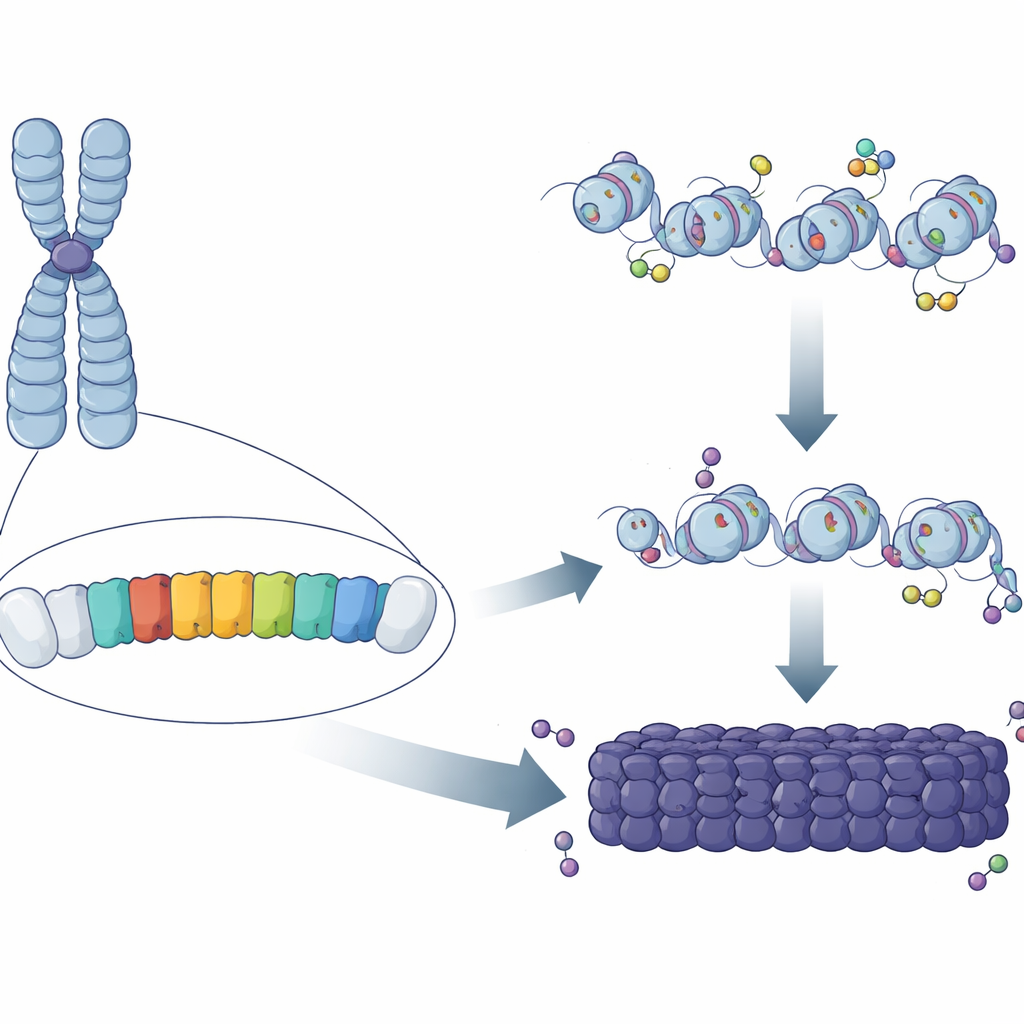
Wiederkehrende Muster im Genom
Fast die Hälfte der DNA von Säugetieren besteht aus wiederholten Sequenzen, viele davon in Regionen um das Chromosomenzentrum gehäuft. Bei Mäusen ist ein Hauptbestandteil dieser Regionen das „major satellite repeat“ (MSR), eine kurze AT‑reiche DNA‑Sequenz, die hunderttausendfach kopiert vorkommt. Klassische Arbeiten zeigten, dass diese Regionen mit chemischen Markierungen und Proteinen überzogen sind, die die DNA in einen kompakten, schützenden Zustand sperren. Dennoch blieb rätselhaft, warum einige MSR‑Kopien vollständig heterochromatisch werden, während andere, an anderen Stellen im Genom verteilt, das nicht tun. Die Autorinnen und Autoren vermuteten, dass kleine Unterschiede in Sequenz oder Verhalten einzelner MSR‑Einheiten darüber entscheiden könnten, ob sie ein Stück Heterochromatin aussäen oder „nukleieren“ können.
Einen Testplatz im Genom bauen
Um diese Idee sauber zu prüfen, erzeugte das Team Maus‑embryonale Stammzellen mit einer künstlichen Einfügestelle in einem stillen Abschnitt von Chromosom 2 – einer Region ohne nahegelegene Gene oder Wiederholungen und ohne nachweisbare Aktivität. In diesen neutralen Ort setzten sie unterschiedliche DNA‑Fragmente ein: intakte MSR‑Einheiten, stark verschlüsselte MSR‑Varianten und Kontrollelemente wie virale Promotoren oder Abschnitte mobiler Elemente. So konnten sie Einheit für Einheit fragen, welche Sequenzen die typischen Merkmale von Heterochromatin anziehen: eine spezifische chemische Markierung an Histonproteinen (H3K9me3), Bindung von HP1‑Proteinen und Einbau des Linker‑Histons H1, die zusammen das lokale Chromatin verdichten und stabilisieren.
Nur transkriptionsfähige Wiederholungen bilden stilles Chromatin
Die Ergebnisse waren überraschend selektiv. Eine einzelne intakte MSR‑Einheit am Testort reichte nicht aus, um das Chromatin zu verändern. Drei oder mehr tandemartige Kopien der intakten MSR‑Sequenz verwandelten dagegen die Umgebung in eine Heterochromatin‑„Insel“ mit starker H3K9me3‑Markierung, HP1‑ und Histon‑H1‑Bindung. Dagegen vermochten gleich lange Abschnitte verschlüsselter MSR‑Sequenzen oder eines anderen Wiederholungstyps (LINE‑1 5'‑untranslatierter Bereich) dies nicht, obwohl sie starke Transkription antreiben konnten. Der entscheidende Unterschied war, dass multi‑kopierte intakte MSR‑Einheiten eine mäßige, bidirektionale Transkription unterstützten, die kurze, nichtstandardmäßige RNA‑Moleküle erzeugte, die eng mit dem Chromatin assoziiert blieben. Dieses Muster, nicht eine hohe, genähnliche Transkriptionsrate, korrelierte mit der Fähigkeit zur Nukleation von Heterochromatin.
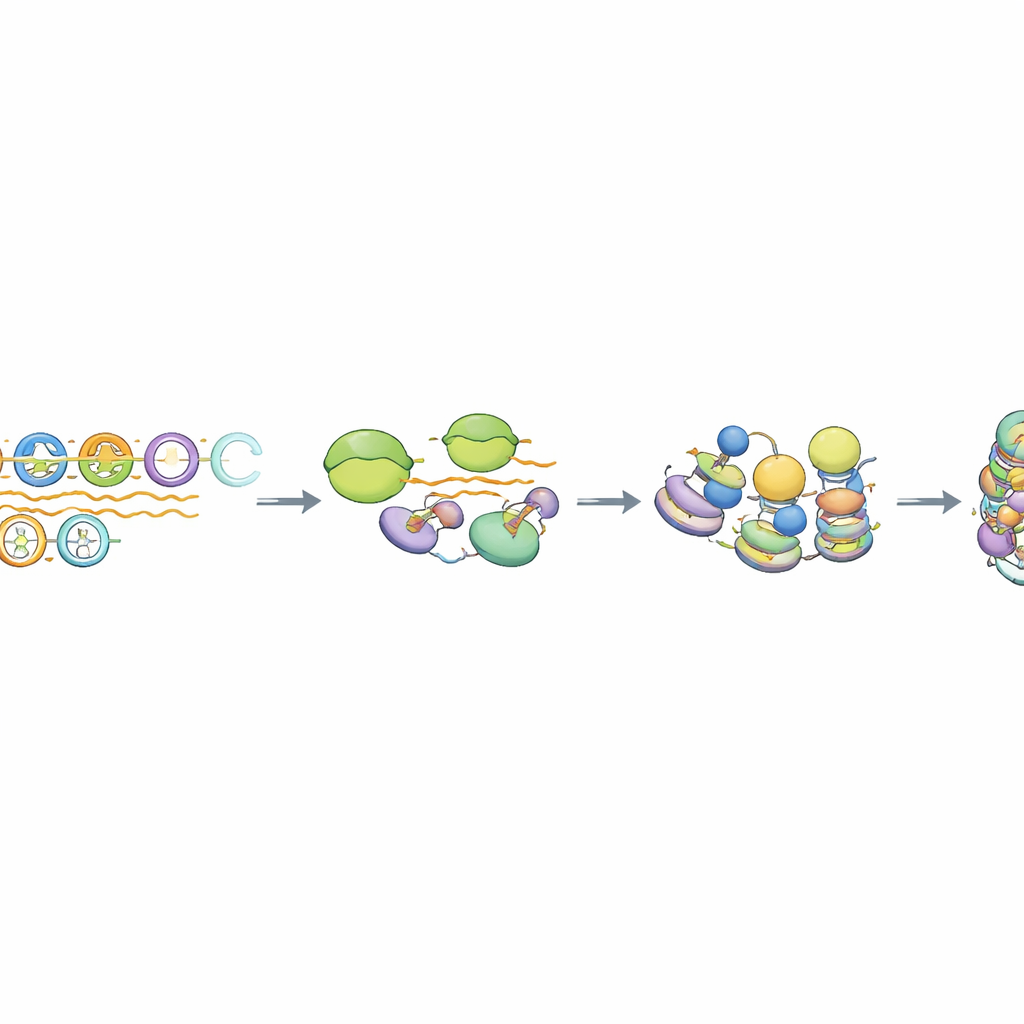
Eine spezielle Form der Transkription und RNA‑Verarbeitung
Bei genauerer Untersuchung fanden die Forschenden, dass die RNA‑Polymerase II, das Enzym, das normalerweise Boten‑RNA herstellt, kurz an die MSR‑Arrays bindet, aber nicht effizient in lange Transkripte übergeht. Die resultierenden RNAs fehlen typische mRNA‑Kennzeichen wie eine schützende 5'‑Cap und lange Poly‑A‑Schwänze und bleiben in der Nähe der sie produzierenden DNA. Ein Proteinkomplex namens Integrator, bekannt für das Trimmen und Terminiertwerden bestimmter nichtkodierender RNAs, war spezifisch an intakten MSR‑Einheiten angereichert. Wenn die Schneideaktivität des Integrators reduziert wurde, stiegen die MSR‑abgeleiteten RNA‑Spiegel deutlich an, doch die wesentliche repressive Histonmarke blieb bestehen, während die HP1‑Bindung sich subtil veränderte. Genomeweite Analysen zeigten, dass nur die intaktesten ~10–15 % der MSR‑Kopien sich so verhalten, was eine Untergruppe „kompetenter“ Wiederholungen hervorhebt, die für diesen transkriptionsgekoppelten Stilllegungsweg verdrahtet sind.
Aufgewickelte DNA als Promotor‑Imitat
Das Team untersuchte auch, wie die MSR‑DNA selbst diese ungewöhnliche Transkription begünstigt. Multi‑kopierte MSR‑Arrays, nicht aber Einzel‑ oder Doppelkopien, zeigten klare Anzeichen lokal aufgewickelter DNA und RNA:DNA‑Hybride – strukturelle Merkmale, die oft in der Nähe aktiver Promotoren und Pausenstellen vorkommen. Diese Konfigurationen wurden verstärkt, wenn Topoisomerase‑Enzyme gehemmt wurden, und sie fielen mit stärkerer MSR‑Transkription und ausgeprägteren Heterochromatin‑Merkmalen zusammen. Die Autorinnen und Autoren schlagen vor, dass drei oder mehr tandemartige MSR‑Einheiten eine physikalische DNA‑Topologie erzeugen, die einen Promotor nachahmt, wodurch Polymerase und Transkriptionsfaktoren gerade genug angezogen werden, um kurze RNAs zu erzeugen, die zusammen mit spezifischen Proteinen eine kompakte Chromatinarchitektur verstärken.
Warum das für die Gesundheit des Genoms wichtig ist
Für den Laien zeigt diese Arbeit, dass Teile unserer „Junk‑DNA“ als fein abgestimmte Schalter wirken, die mithilfe einer Mischung aus DNA‑Form, niedrigem Transkriptionsniveau und RNA‑Verarbeitung die schützende Hülle des Genoms aufbauen. Nur MSR‑Einheiten, die diese kontrollierte, nicht‑mRNA‑artige Transkription tragen können, können neues Heterochromatin entfachen; verschlüsselte oder übermäßig aktive Elemente können das nicht. Diese DNA/RNA‑basierte Logik hilft zu erklären, wie Zellen Regionen unterscheiden, die still gehalten werden sollen, von solchen, die Gene beherbergen dürfen, und warum fehlregulierte Satelliten‑RNAs mit Krebs und Entwicklungsstörungen in Verbindung gebracht werden. Im Kern zeigt die Studie, dass der repetitive „Hintergrund“ des Genoms kein passives Füllmaterial ist, sondern ein aktiver Gestalter nuklearer Architektur und Stabilität.
Zitation: Lo, YH., Shukeir, N., Erikson, G. et al. Transcriptional competence defines the heterochromatin nucleating potential of isolated MSR units. Nat Commun 17, 2653 (2026). https://doi.org/10.1038/s41467-026-70991-2
Schlüsselwörter: Heterochromatin, Satelliten‑DNA, nichtkodierende RNA, Chromatinstruktur, Genomstabilität