Clear Sky Science · de
Substituent-induzierte Redox-Molekülgrenzfläche für die fotoelektrochemische Synthese von Wasserstoffperoxid an Grenzflächen
Eine schlauere Methode zur Herstellung eines vertrauten Desinfektionsmittels
Wasserstoffperoxid ist ein gängiges Haushaltsdesinfektionsmittel, doch seine Produktion in Fabriken erfordert meist energieintensive Verfahren und gefährliche Chemikalien. Diese Studie stellt ein neues Feststoffmaterial vor, das Wasserstoffperoxid direkt aus Luft und Wasser mithilfe von Sonnenlicht und schonenden Vibrationen herstellen kann und zugleich hilft, giftige Metallverunreinigungen im Wasser zu beseitigen. Durch die gezielte Anordnung der reaktiven Stellen im Material auf der Ebene einzelner Moleküle zeigen die Forschenden, wie wir die Eleganz der natürlichen Photosynthese nachahmen könnten, um grüneren Chemieprozessen und einer effizienteren Abwasserbehandlung Vorschub zu leisten.
Warum herkömmliche Katalysatoren nicht ausreichen
Die meisten industriellen Katalysatoren beruhen auf einer einzigen Art aktiver Stelle – einem Ort an der Oberfläche, an dem Moleküle haften, reagieren und wieder freigesetzt werden. Das funktioniert für einfache Reaktionen, aber viele reale Prozesse, etwa die Wasserspaltung oder die Umwandlung von Sauerstoff in nützliche Chemikalien, bestehen aus mehreren Schritten, die besser verlaufen, wenn verschiedene Aufgaben an unterschiedlichen Orten stattfinden. Die Natur nutzt diesen Trick bereits: in der Photosynthese und in Enzymen arbeiten mehrere spezialisierte Stellen zusammen, um Elektronen und Protonen in präziser Reihenfolge zu verschieben. Konventionelle technische Katalysatoren hingegen packen ihre aktiven Stellen oft ungeordnet zusammen, was zu Energieverlusten und unerwünschten Nebenreaktionen führt und die Effizienz mindert.
Entwurf einer zweiseitigen molekularen Werkbank
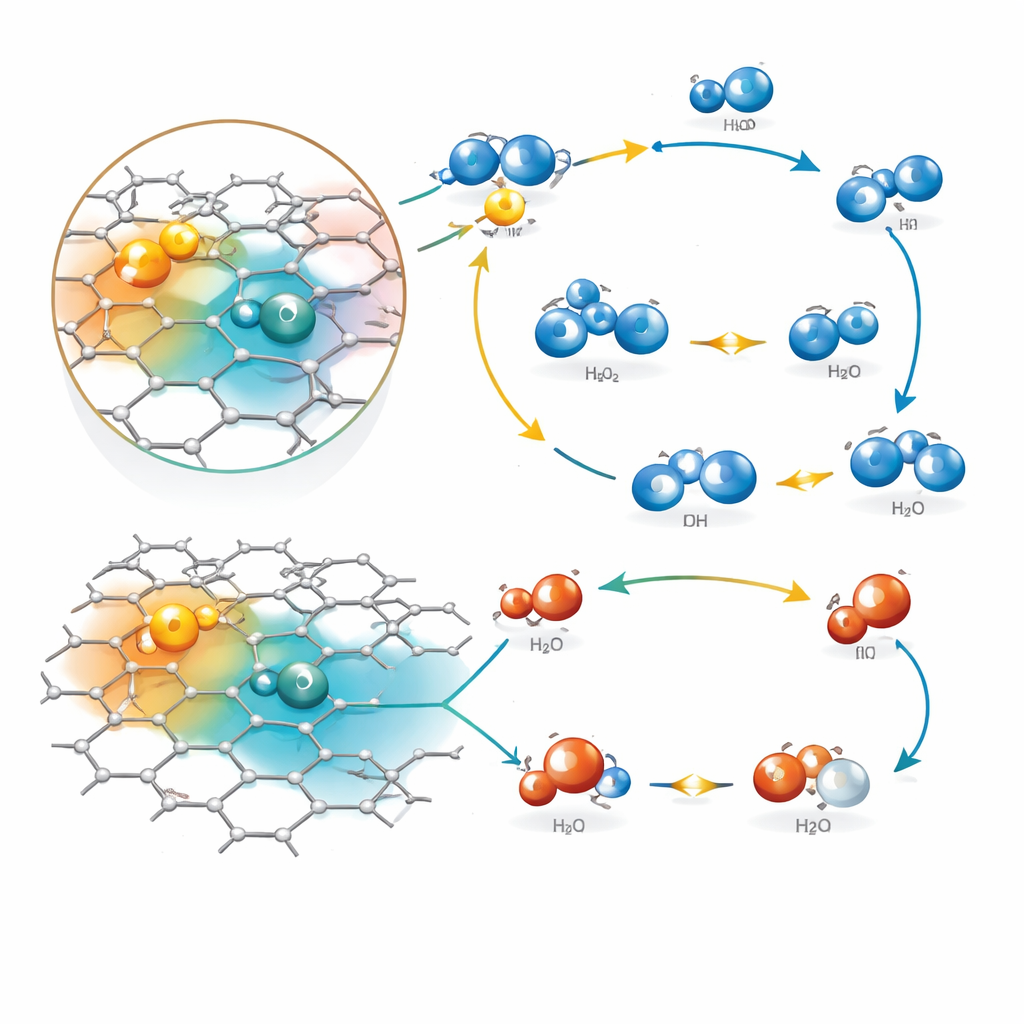
Das Team ging dieses Problem mit einer Familie poröser organischer Feststoffe an, den kovalenten Triazin‑Gerüsten. Dabei handelt es sich um starre Netzwerke aus Kohlenstoff‑ und Stickstoffringen, verbunden durch Benzolbausteine, die blattartige Strukturen mit vielen inneren Kanälen bilden. Durch den Austausch einiger Benzol‑Linker gegen fluorierte Varianten konnten sie die Verteilung der Elektronen innerhalb des Gerüsts feinjustieren. Detaillierte Computersimulationen zeigten, dass bei einem bestimmten Fluoranteil – dem Material CTF‑TF‑0.5 – die elektronische Struktur sich natürlich in zwei verschiedene Bereiche aufspaltet. Ein Bereich neigt dazu, positiv geladene "Löcher" zu halten und fungiert als Oxidationszone, während der andere Bereich zusätzliche Elektronen konzentriert und als Reduktionszone dient. Effektiv wird das Material so zu einer eingebauten molekularen Grenzfläche mit getrennten "Seiten", die dafür zuständig sind, Elektronen entweder aufzunehmen oder abzugeben.
Luft und Wasser in Peroxid verwandeln
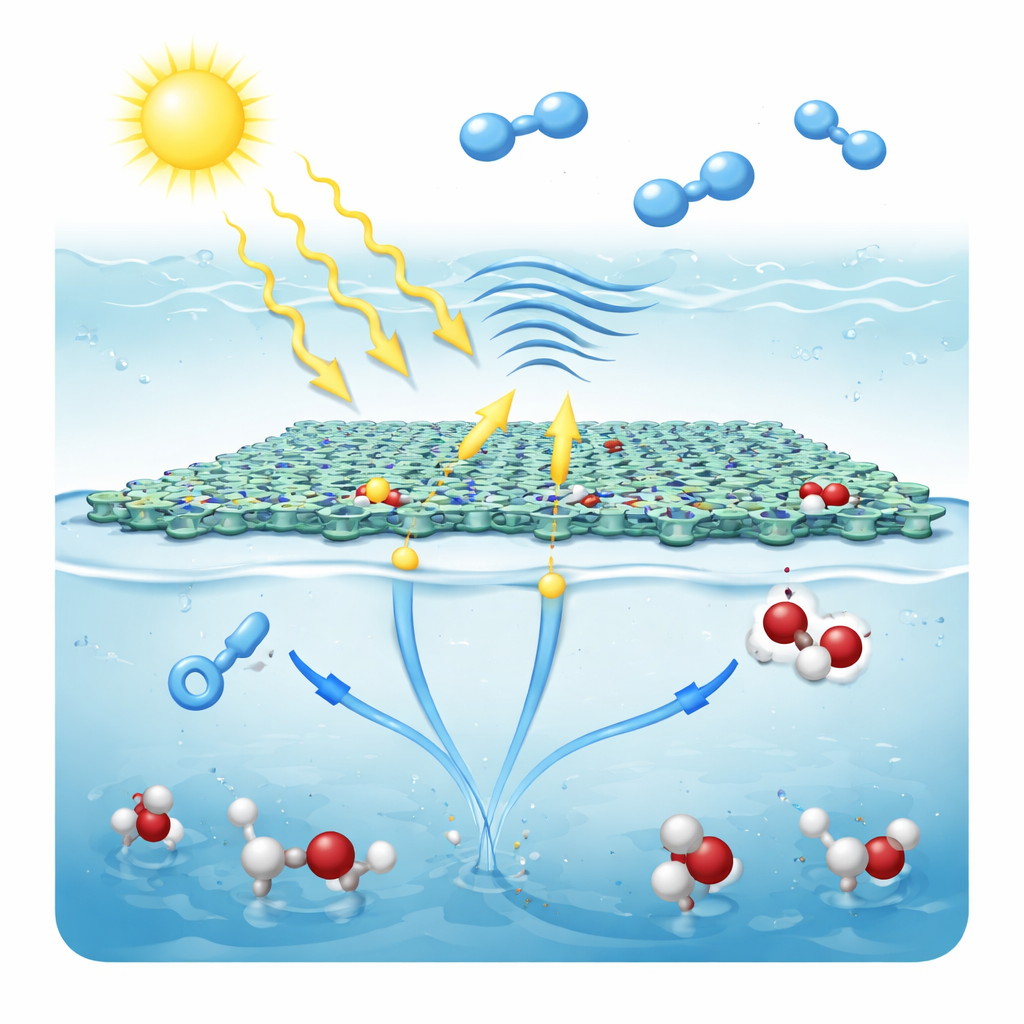
Im Betrieb schweben dünne Flocken von CTF‑TF‑0.5 an der Grenze zwischen Luft und Wasser und bilden eine dreiphasige Grenzfläche aus Gas, Flüssigkeit und Feststoff. Sonnenlicht regt Elektronen im Gerüst an, und gleichzeitig verstärken Ultraschallvibrationen die piezoelektrische Antwort des Materials, was die Ladungstrennung noch effizienter macht. Elektronen wandern durch die Struktur zu den Reduktionszonen, wo sie mit dem aus der Luft unmittelbar über der Wasseroberfläche verfügbaren Sauerstoff reagieren. Dieser schrittweise Prozess wandelt Sauerstoff über reaktive Zwischenstufen in Wasserstoffperoxid um. In den Oxidationszonen entziehen die positiv geladenen Löcher Elektronen aus Wassermolekülen und erzeugen kurzlebige Radikale, die ebenfalls zur Bildung von Wasserstoffperoxid koppeln. Da Oxidation und Reduktion an getrennten, aber verbundenen Stellen stattfinden, wird unerwünschte Ladungsrekombination unterdrückt und beide Halbreaktionen verlaufen entlang Pfaden, die die Bildung von Wasserstoffperoxid begünstigen, anstatt Sauerstoff vollständig zu Wasser zu reduzieren.
Leistungssteigerung durch Struktur und mechanische Einwirkung
Die Forschenden setzten eine Reihe von Techniken ein – Spektroskopie, Mikroskopie und Druckmessungen – um zu zeigen, wie die besondere Anordnung der Stellen das Verhalten beeinflusst. Im Vergleich zu verwandten Materialien ohne klare Funktionsaufteilung weist CTF‑TF‑0.5 eine stärkere Ladungstrennung, höhere Oberflächenpotenziale unter Lichteinfall und eine ausgeprägtere mechanische Reaktion bei Druck oder Vibration auf; all dies fördert die schnellere Elektronenmigration. Unter kombiniertem Licht‑ und Ultraschalleinfluss bei Raumtemperatur erreicht der schwimmende Katalysator eine Wasserstoffperoxid‑Produktionsrate von etwa 4,7 Millimol pro Gramm und Stunde und übertrifft damit viele zuvor berichtete organische Photokatalysatoren und piezoelektrische Materialien. Die Anordnung funktioniert nicht nur in reinem Wasser, sondern auch in Leitungswasser, Meerwasser, Flusswasser, Regenwasser und Krankenhausabwasser und behält trotz Verunreinigungen eine beträchtliche Aktivität bei.
Entfernung giftiger Metalle aus realem Abwasser
Über die bloße Erzeugung von Wasserstoffperoxid hinaus demonstrierte das Team eine praktische Umweltanwendung: die Entfernung von Arsen aus saurem Bergbaubetriebswasser. Bei dieser Form der Verschmutzung liegt Arsen überwiegend als As(III) vor, das sehr giftig und schwer zu binden ist. Während der Behandlung mit CTF‑TF‑0.5 unter Licht und Ultraschall oxidiert das in situ gebildete Wasserstoffperoxid As(III) zu As(V), einer weniger toxischen Form, die stärker an das Gerüst bindet und so herausgefiltert werden kann. In Labortests wandelte das Material über 95 % des vorhandenen As(III) innerhalb weniger Stunden zu As(V) um und adsorbierte das entstehende As(V) effizient, selbst in authentischem Grubenabwässern mit niedrigem pH‑Wert wie unter realen Bedingungen.
Was das für den Alltag bedeutet
Indem ein Katalysator entwickelt wurde, dessen molekulare Architektur explizit trennt, wo Elektronen entzogen und wo sie zugeführt werden, zeigt diese Arbeit einen Weg zu effizienteren, selektiveren chemischen Prozessen, die nur von Licht und sanfter mechanischer Energie angetrieben werden. Das neue Material kann auf Wasser schwimmen, Sauerstoff aus der Luft aufnehmen und kontinuierlich Wasserstoffperoxid ohne Zusatzchemikalien produzieren, während es gleichzeitig hilft, gefährliche Metalle wie Arsen zu binden und zu entfernen. Für den Laien lautet die Quintessenz: Durch sorgfältige Kontrolle der Struktur auf winzigster Skala lassen sich sauberere und sicherere Wege finden, bekannte Verbindungen herzustellen und verschmutztes Wasser zu behandeln – ein Schritt, der die technische Chemie näher an die Eleganz biologischer Systeme bringt.
Zitation: Li, Z., An, L., Guan, L. et al. Substituent-induced oxidation-reduction molecular organic junction for interfacial hydrogen peroxide photosynthesis. Nat Commun 17, 2794 (2026). https://doi.org/10.1038/s41467-026-70959-2
Schlüsselwörter: Wasserstoffperoxid, Photokatalysator, kovalentes Triazin-Gerüst, Wasseraufbereitung, Arsenentfernung