Clear Sky Science · de
TONSL unterdrückt polymerase-theta-abhängige Tandemduplikationen durch chromatingeführte Reparatur
Wenn die DNA gefährliche Extra-Kopien erzeugt
Jede Zelle muss ihre DNA mit erstaunlicher Genauigkeit kopieren, dennoch ist unser Genom ständig Beschädigungen ausgesetzt, die Chromosomen umgestalten können. Eine besonders wichtige Veränderung ist die „Tandemduplikation“, bei der ein DNA-Abschnitt kopiert und direkt neben seinem Original eingefügt wird. Solche zusätzlichen Kopien können der Evolution nützlich sein, indem sie neues genetisches Material bereitstellen, in Krebs jedoch oft unkontrolliertes Wachstum antreiben. Diese Studie enthüllt, wie ein Protein namens TONSL Zellen dabei hilft, diese riskanten Duplikationen zu vermeiden, und zeigt eine verborgene Schutzfunktion, die offenbar bei Tieren und Pflanzen geteilt wird. 
Extra-Kopien: Für die Evolution nützlich, für die Gesundheit riskant
Große, hintereinandergereihte DNA-Wiederholungen, bekannt als Tandemduplikationen, gehören zu den häufigsten Strukturveränderungen in komplexen Genomen. Sie können ganze Gene verdoppeln und so über lange Zeiträume neue Funktionen ermöglichen. Wenn Forscher jedoch gesunde Gewebe untersuchen, finden sie nur sehr wenige neue Tandemduplikationen, was darauf hindeutet, dass Zellen aktiv deren Entstehung verhindern. In vielen Krebsarten sind diese Duplikationen jedoch zahlreich und formen das Genom in großem Maßstab um. Das Rätsel bestand darin, wie normale Zellen DNA-Brüche normalerweise so reparieren, dass sie nicht versehentlich solche großen kopierten Segmente erzeugen.
Auf der Spur eines verborgenen Genomwächters
Um natürliche Schutzfaktoren gegen diese Duplikationsereignisse zu finden, wandten sich die Forschenden dem winzigen Fadenwurm Caenorhabditis elegans zu, der in großer Zahl gezüchtet und sequenziert werden kann. Durch die Reanalyse einer Sammlung von etwa 2.000 mutagenisierten Wurmstämmen identifizierten sie einige wenige, die unerwartet viele Tandemduplikationen aufwiesen. Ein gemeinsamer Nenner dieser Stämme war die Schädigung eines einzelnen Gens, tnsl-1, das das Protein TONSL kodiert. Als das Team dieses Gen gezielt entfernte und die Würmer über viele Generationen hin weiterzog, sammelten sich in ihren Genomen stetig Tandemduplikationen an – grob eine pro Generation – verteilt über alle Chromosomen. Überraschenderweise blieben die Tiere weitgehend gesund, was zeigt, dass ein Genom viele große Duplikationen stillschweigend anhäufen kann, ohne sofort zusammenzubrechen.
Schnelle Zellen erzeugen kleine Duplikationen, langsame Zellen große
Genauere Untersuchungen zeigten, dass die neuen Duplikationen zwei Hauptgrößen aufwiesen: eine Gruppe um einige Zehntausend DNA-Basen und eine andere um einige Hunderttausend. Das Team vermutete, dass das Tempo der Zellteilung beeinflusst, wie groß eine Duplikation wird. Wurm-Embryonen teilen sich sehr schnell, mit Zellzyklen von etwa 20 Minuten, während Keimzellen, die Eier und Spermien bilden, viel langsamer teilen. Mithilfe sorgfältig gestalteter genetischer Kreuzungen und kompletter Genomsequenzierung der Nachkommen konnten die Forschenden den Zeitpunkt der Entstehung der Duplikationen eingrenzen. Sie fanden heraus, dass kleine Duplikationen während der schnellen frühen Embryonalteilungen entstanden, während große im späteren, langsam teilenden Keimkreis auftraten. Das deutet auf ein Modell hin, in dem die verfügbare Zeit für DNA-Reparatur und -Synthese bestimmt, wie weit ein bruchgetriebener Kopiervorgang laufen kann, bevor er abgeschlossen wird. 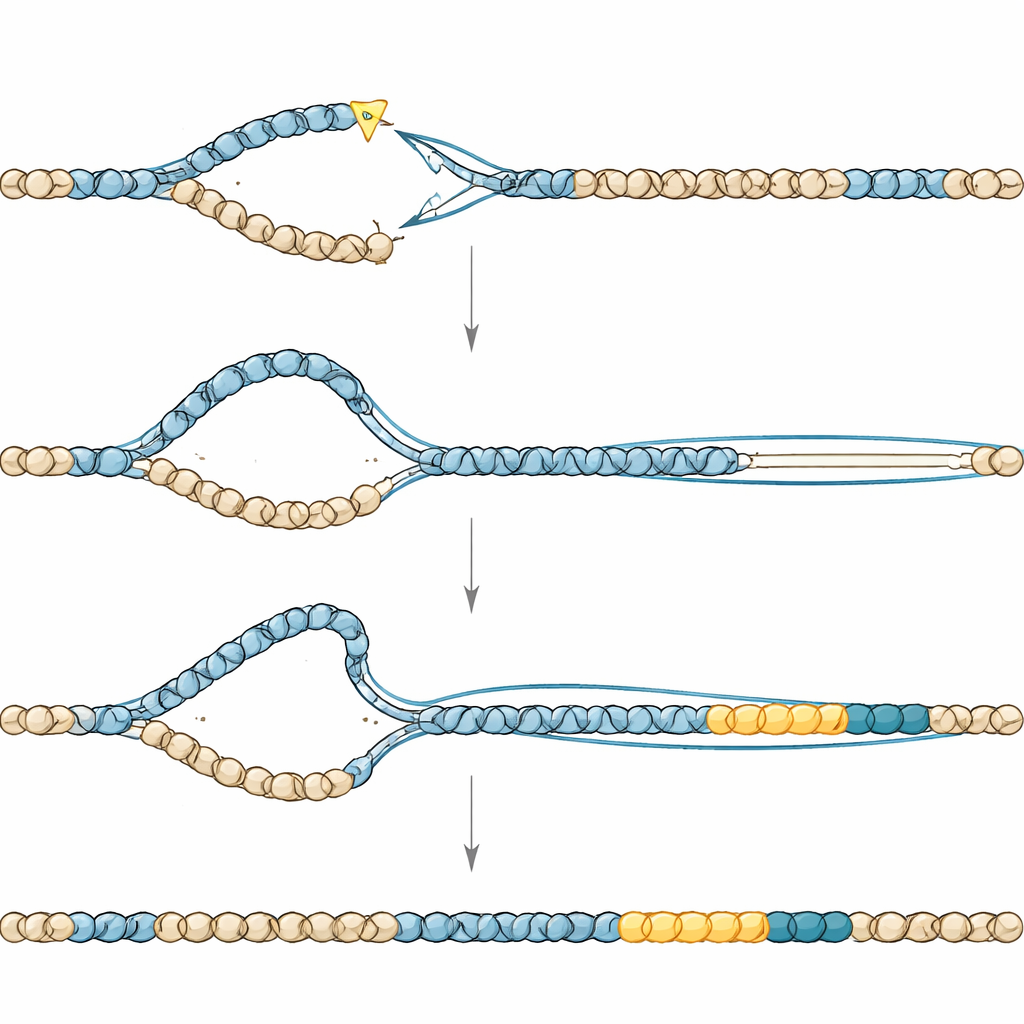
Wie fehlerhafte Reparaturmaschinen Duplikationen erzeugen
Die Verbindungsstellen, an denen die duplizierten Segmente mit der Original-DNA verbunden waren, trugen die Handschrift eines spezialisierten, fehleranfälligen Reparaturwegs, der polymerase-theta-vermittelten End-Joining genannt wird. Als das Schlüsselelement dieses Wegs deaktiviert wurde, verschwanden die Duplikationen nahezu vollständig, doch die Würmer zahlten einen hohen Preis in Form verminderter Fruchtbarkeit. Das legt nahe, dass derselbe Weg auch nötig ist, um gebrochene Chromosomen zu retten, wenn TONSL fehlt. Weitere Experimente deuteten auf einen zweiten Akteur hin: einen Prozess, der einem „break-induced replication“ ähnelt, bei dem ein gebrochenes DNA-Ende eine intakte Vorlage nutzt, um große Sequenzabschnitte zu kopieren. Die Entfernung einer Helikase, die solch langreichende Kopien fördert, verringerte die Größe der Duplikationen, stoppte sie aber nicht vollständig und unterstützte somit die Idee, dass ausgedehnte, schlecht kontrollierte DNA-Synthese diesen Ereignissen zugrunde liegt.
Chromatin als stiller Regisseur der Reparatur
Es ist bekannt, dass TONSL an bestimmte chemische Markierungen auf neu replizierten DNA-Verpackungsproteinen bindet, was darauf hindeutet, dass es hilft, das Chromatin—die Struktur, die DNA umhüllt und organisiert—direkt nach der Replikation wiederaufzubauen. Die Autorinnen und Autoren erzeugten eine subtile Veränderung im Wurmprotein, die diese Chromatinbindung abschwächt. Würmer mit diesem einzelnen Aminosäureaustausch bildeten weiterhin Duplikationen, aber weniger und kleinere, was darauf hinweist, dass TONSLs Haftung an frischem Chromatin direkt ausufernde DNA-Synthese an Reparaturstellen begrenzt. In dessen Abwesenheit können Reparaturzwischenprodukte zu weit auslaufen, bevor sie schließlich durch den fehleranfälligen Verknüpfungsweg zusammengenäht werden, sodass ein dupliziertes Blockfragment anstelle einer sauberen Reparatur zurückbleibt.
Eine gemeinsame Verteidigung von Würmern bis zu Pflanzen
Um zu prüfen, ob diese Schutzfunktion in anderen Arten erhalten ist, untersuchten die Forschenden ein Mutant der Modellpflanze Arabidopsis thaliana, dem das verwandte Protein TONSOKU fehlt. Nach nur wenigen Generationen sammelten diese Pflanzen eine auffällige Anzahl großer Tandemduplikationen an, was zu einem Zuwachs der Genomgröße von etwa einem Prozent pro Generation führte—eine enorme Veränderung auf evolutionären Zeitskalen. Auch hier trugen die DNA-Verbindungsstellen die charakteristischen kurzen Überlappungen und Einschlüsse, die mit demselben fehleranfälligen Reparaturweg assoziiert werden, was darauf hindeutet, dass Würmer und Pflanzen ein tief konserviertes chromatingeführtes System nutzen, um replikationsassoziierte Brüche von duplikationsanfälligen Ergebnissen wegzulenken.
Was das für Krebs und Genomstabilität bedeutet
Einfach gesagt zeigt diese Arbeit, dass TONSL und sein Pflanzenverwandter als Qualitätskontrolleure fungieren, die an der Schnittstelle von DNA-Replikation und -Reparatur sitzen. Indem sie helfen, das Chromatin nach einem Bruch korrekt wiederaufzubauen, halten sie Reparaturvorgänge kurz und ordentlich und verhindern, dass lange DNA-Abschnitte doppelt hintereinander kopiert werden. Ohne diese Kontrolle reparieren Zellen Brüche zwar weiterhin, tun dies aber durch Überdehnen und anschließendes grobes Wiederzusammenfügen der DNA, wobei Tandemduplikationen zurückbleiben. Da ähnliche Duplikationsmuster in mehreren menschlichen Krebsarten beobachtet werden, einschließlich Tumoren mit Defekten in replikationsassoziierten Faktoren, könnte das Verständnis von TONSLs Rolle schließlich helfen zu erklären, warum bestimmte Tumoren so stark umgestaltete Genome erwerben, und neue Ansätze nahelegen, vorherzusagen oder zu beeinflussen, wie sich ihre DNA unter Therapie verändert.
Zitation: van Schendel, R., Romeijn, R., Kralemann, L.E.M. et al. TONSL suppresses polymerase theta-dependent tandem duplications through chromatin-guided repair. Nat Commun 17, 2875 (2026). https://doi.org/10.1038/s41467-026-70905-2
Schlüsselwörter: Genomstabilität, Tandemduplikationen, DNA-Reparatur, Chromatin, TONSL