Clear Sky Science · de
Timosaponin AIII steigert die Wirksamkeit von CAR‑T‑Zellen und verhindert Rückfälle durch Beeinträchtigung von CAR‑Tregs
Die Bremse des Immunsystems lösen, um die Krebsbehandlung zu stärken
Für Menschen mit aggressiven Blutkrebserkrankungen kann die CAR‑T‑Zelltherapie lebensverändernd sein: Die körpereigenen Immunzellen der Patient:innen werden so umprogrammiert, dass sie Tumorzellen aufspüren. Dennoch kommt es bei vielen Patient:innen zu Rückfällen, wenn diese gentechnisch veränderten Zellen an Wirksamkeit verlieren. In dieser Studie wird ein pflanzliches Molekül, Timosaponin AIII, untersucht, das CAR‑T‑Zellen länger aktiv hält, indem es selektiv eine zentrale Bremsfunktion des Immunsystems stört — womit diese Therapien potenziell dauerhafter und wirkungsvoller werden.
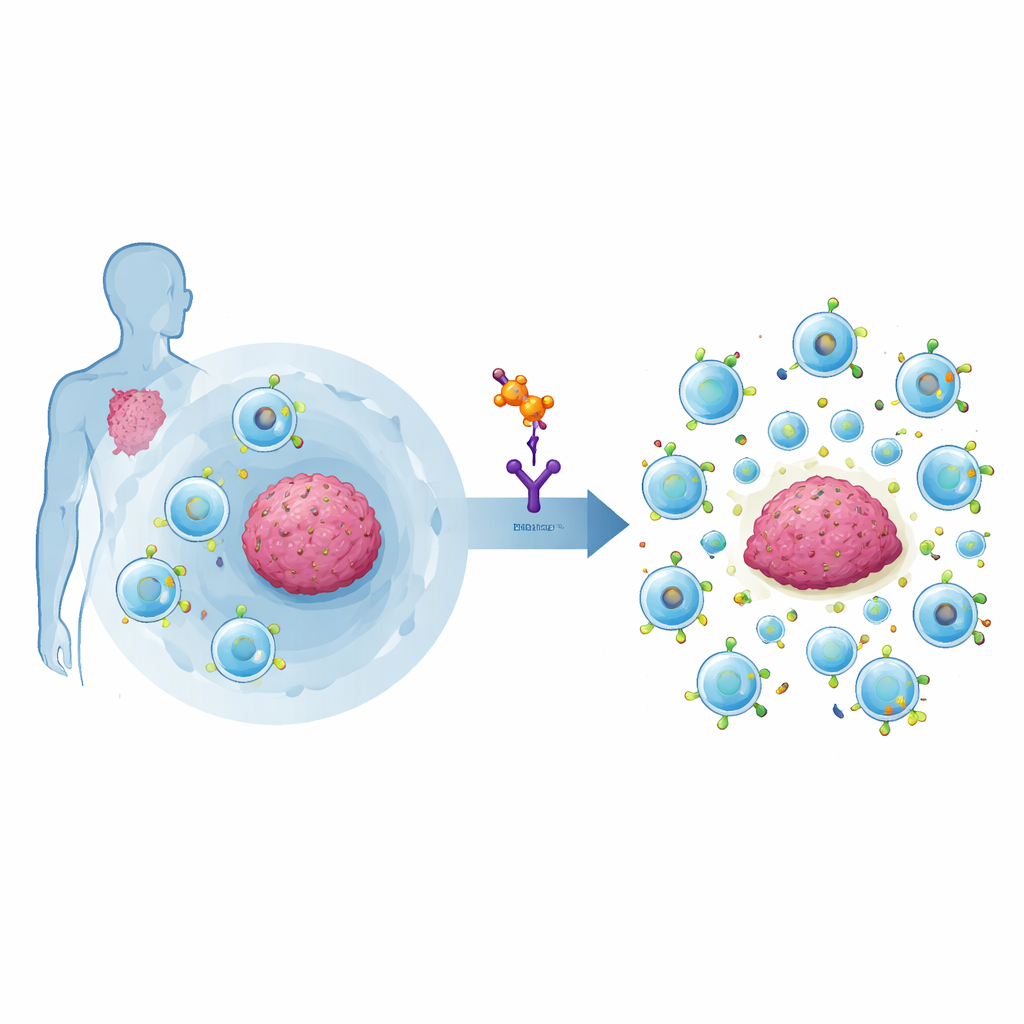
Warum starke Krebsbekämpfer manchmal ins Stocken geraten
CAR‑T‑Zellen sind maßgeschneiderte Immunzellen, die einen künstlichen Sensor tragen, um Krebsziele wie CD19 auf malignen B‑Zellen zu erkennen. In echten Patient:innen erleben jedoch nur etwa die Hälfte dauerhafte Remissionen. Ein Hauptgrund ist eine spezielle Untergruppe von Immunzellen, die regulatorischen T‑Zellen oder Tregs. Diese Zellen verhindern normalerweise, dass das Immunsystem gesundes Gewebe angreift, können aber bei Krebs die anti‑tumoralen Antworten unterdrücken — auch die von CAR‑T‑Zellen. Kürzliche klinische Studien zeigten, dass CAR‑T‑Produkte mit einem hohen Anteil an Tregs mit größerer Wahrscheinlichkeit wirkungslos bleiben oder Rückfälle verursachen. Leider sind derzeit verfügbare Medikamente zur Verringerung von Tregs oft grobe Werkzeuge, die hilfreiche Immunzellen ebenso schädigen wie die schädlichen.
Ein sanfter Helfer aus einer Heilpflanze
Die Forschenden entwickelten ein Screening‑System, das anzeigt, wenn ein zentraler Treg‑Kontrollschalter, das Protein FoxP3, die Immunaktivierung herunterfährt. Sie testeten mehr als 3.000 natürliche und zugelassene Verbindungen und identifizierten solche, die FoxP3 lockern konnten, ohne Zellen zu töten. Ein Kandidat fiel besonders auf: Timosaponin AIII (TAIII), ein steroidähnliches Molekül aus der traditionellen chinesischen Heilpflanze Anemarrhena asphodeloides, das bereits klinisch als topisches entzündungshemmendes Hautmittel getestet wird. In humanen T‑Zellen, die unter Bedingungen gezüchtet wurden, die normalerweise ihre Umwandlung in Tregs fördern, verringerte TAIII deutlich die Bildung und Aktivität dieser unterdrückenden Zellen, während andere T‑Zelltypen weitgehend erhalten blieben. Das deutete darauf hin, dass TAIII das Immunsystem weg von Unterdrückung und hin zur Angriffslust lenken kann.
Wie ein kleines Molekül CAR‑T‑Zellen befreit
Bei der Untersuchung des Wirkmechanismus nutzte das Team chemische Sonden, Proteinbindungstests und Computermodelle und fand heraus, dass TAIII an den Adenosin‑A2A‑Rezeptor (A2AR) bindet, einen bekannten „Aus‑Schalter“ des Immunsystems, der auf hohe Adenosinspiegel in Tumoren reagiert. Anstatt die Hauptbindestelle zu blockieren, schiebt sich TAIII in eine cholesterin‑sensible Region des Rezeptors in der Zellmembran und wirkt so als allosterischer Inhibitor. Durch die Verdrängung cholesterinähnlicher Lipide und die Abschwächung einer Signalkette, die im Protein CREB endet, senkt TAIII die FoxP3‑Produktion und untergräbt das Treg‑Programm. Entfernte man A2AR aus T‑Zellen oder CAR‑T‑Zellen, verlor TAIII seine Wirkung, was bestätigt, dass dieser Rezeptor das kritische Ziel ist.
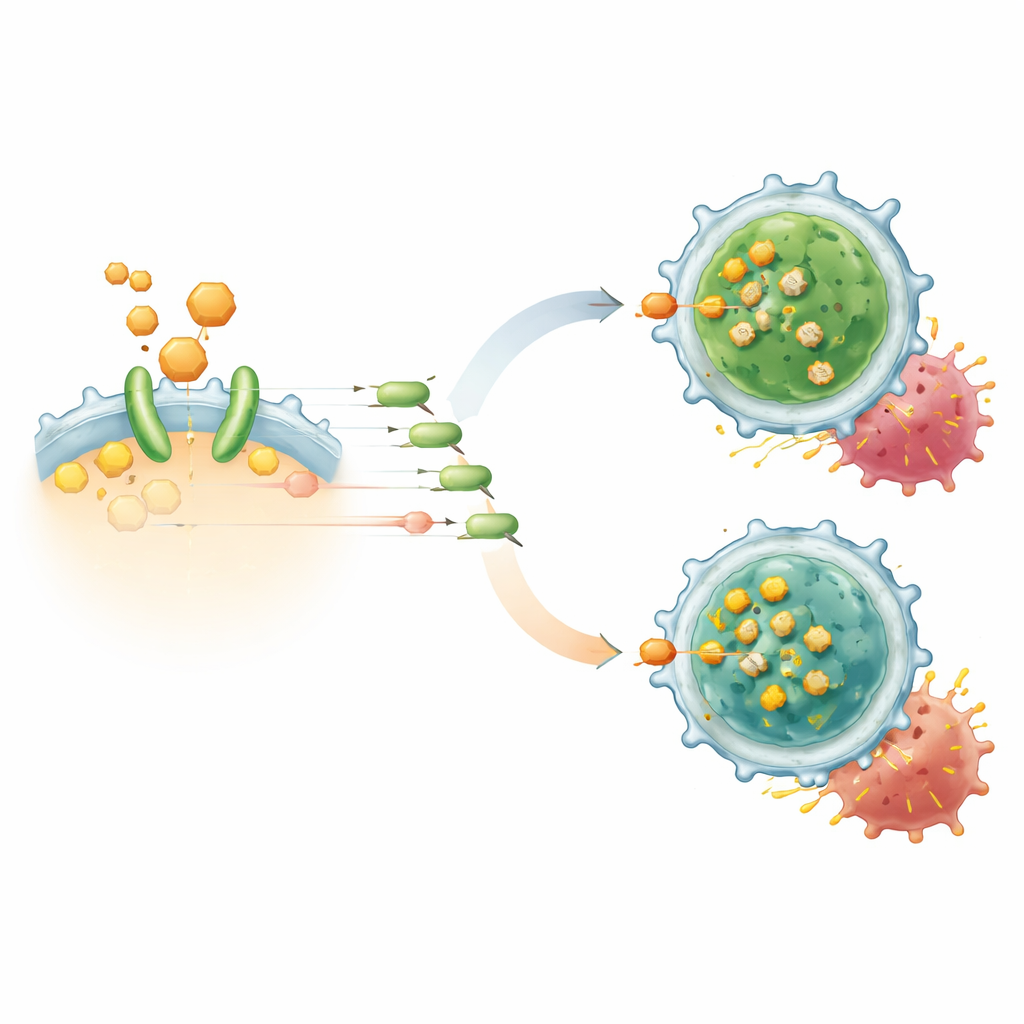
Stärkere, länger anhaltende CAR‑T‑Antworten in Modellen
In Labor‑Co‑Kultur‑Experimenten erhöhte die Zugabe von TAIII zu humanen CD19 CAR‑T‑Zellen deren Fähigkeit, Lymphomzellen zu töten, und steigerte die Freisetzung von Angriffsmediatoren wie Interferon‑gamma und IL‑2. Gleichzeitig verringerte sich der Anteil der CAR‑T‑Zellen mit Treg‑ähnlichen Merkmalen, und es wurden vermehrt zentrale Memory‑T‑Zellen gefördert — eine Untergruppe, die mit anhaltendem Schutz verbunden ist. Einzelzell‑RNA‑Sequenzierungen zeigten, dass TAIII‑behandelte CAR‑T‑Populationen weniger FoxP3‑reiche regulatorische Zellen und mehr aktive Killer‑T‑Zellen enthielten. In mehreren Mausmodellen von Blutkrebserkrankungen und soliden Tumoren verlangsamte die Kombination von TAIII mit CAR‑T‑Therapie das Tumorwachstum, vertiefte die Response und verringerte spät auftretende Rückfälle deutlich. Wurden CAR‑T‑Produkte experimentell von Tregs befreit, brachte TAIII keinen zusätzlichen Nutzen, was unterstreicht, dass seine Hauptfunktion darin besteht, diese unterdrückende Untergruppe zu zerschlagen und nicht, alle T‑Zellen allgemein zu überstimulieren.
Über CAR‑T hinaus: Das tumoriale Immunumfeld umlenken
Die Effekte von TAIII beschränkten sich nicht auf gentechnisch veränderte Zellen. Bei immunkompetenten Mäusen mit soliden Tumoren verringerte tägliche TAIII‑Gabe die Zahl der Tregs im Tumor, erhöhte die Infiltration durch CD8‑„Killer“‑T‑Zellen und steigerte die Spiegel antitumoraler Zytokine — alles ohne offensichtliche Toxizität oder Gewichtsverlust. In Kombination mit einer Anti‑PD‑1‑Checkpoint‑Therapie — einer weiteren weit verbreiteten Form der Immuntherapie — verstärkte TAIII die Tumorkontrolle und erweiterte nützliche memory‑ähnliche T‑Zellen. Wichtig ist, dass TAIII in stark immundefizienten Mäusen ohne funktionelle T‑Zellen kaum Wirkung zeigte, was darauf hinweist, dass seine anti‑tumorale Aktivität davon abhängt, die Immunantwort umzugestalten und nicht direkt Krebszellen zu vergiften.
Was das für die künftige Krebsbehandlung bedeuten könnte
Für Laien lautet die Botschaft, dass die Autor:innen einen Weg gefunden haben, eine spezifische interne Bremse des Immunsystems zu lockern, ohne die Energiezufuhr zu kappen oder das Gaspedal voll durchzutreten. Indem regulatorische T‑Zellen über eine präzise Interaktion mit dem A2A‑Rezeptor gedrosselt werden, hilft Timosaponin AIII CAR‑T‑Zellen, aktiv zu bleiben, langlebigere Gedächtnispopulationen zu bilden und nicht vom Tumormikroumfeld zum Schweigen gebracht zu werden. In präklinischen Studien und Tests mit patientenabgeleiteten CAR‑T‑Zellen übersetzte sich dies in stärkere Tumorvernichtung und weniger Rückfälle. Klinische Studien werden nötig sein, um Sicherheit und Wirksamkeit beim Menschen zu bestätigen, doch TAIII tritt als vielversprechende, pflanzenbasierte Ergänzung hervor, die moderne Immuntherapien sowohl langlebiger als auch insgesamt erfolgreicher machen könnte.
Zitation: Hou, M., Zhang, W., Qi, Z. et al. Timosaponin AIII enhances CAR-T cell potency and prevents relapse through impairing CAR-Tregs. Nat Commun 17, 3045 (2026). https://doi.org/10.1038/s41467-026-70867-5
Schlüsselwörter: CAR‑T‑Zelltherapie, regulatorische T‑Zellen, Adenosin‑A2A‑Rezeptor, Timosaponin AIII, Krebsimmuntherapie