Clear Sky Science · de
Räumliche Heterogenität von MDSCs, vermittelt durch ANXA1-FPRs‑Signalgebung, treibt die Immunsuppression beim Fortschreiten von OSCC voran
Warum die körpereigenen Abwehrkräfte bei manchen Mundkrebsarten versagen
Das Plattenepithelkarzinom der Mundhöhle, eine häufige Form von Mundkrebs, ist oft resistent gegenüber den aktuell vielversprechenden Krebsbehandlungen: Immuntherapien, die die körpereigene Abwehr entfesseln. Die Studie stellt eine grundsätzliche, aber entscheidende Frage: Warum versagen mächtige Immunzellen, die Krebs erkennen und zerstören sollten, so häufig bei diesen Tumoren? Durch das Kartieren der Position verschiedener Zellen im Tumor und ihrer Kommunikationswege enthüllen die Forschenden ein sich wandelndes „Katz‑und‑Maus“-Spiel zwischen Krebszellen, immunsuppressiven Zellen und CD8‑Killerzellen, das das Versagen der Behandlung erklärt — und einen Weg aufzeigt, es zu beheben. 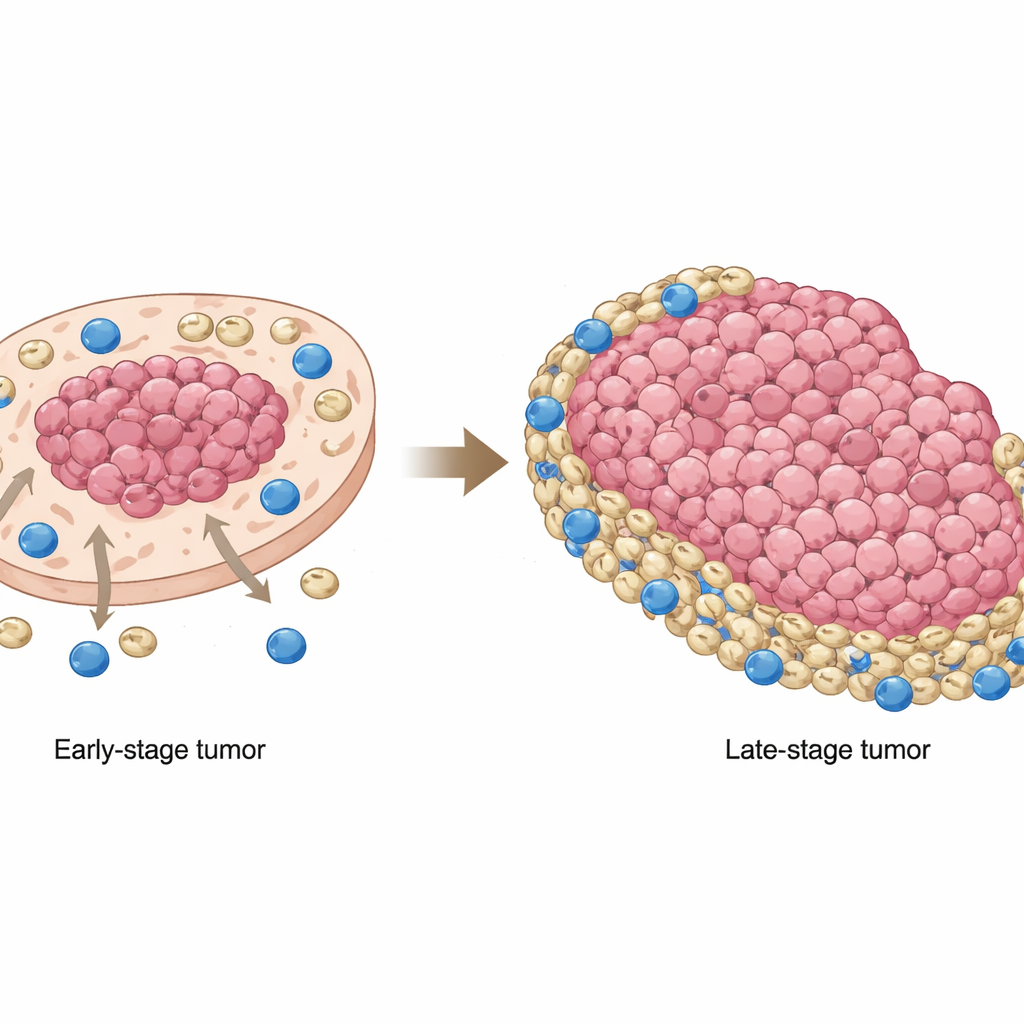
Die verborgene Landschaft im Inneren eines Tumors
Die Autorinnen und Autoren kombinierten zwei hochmoderne Methoden: Einzelzell‑RNA‑Sequenzierung, die die Aktivität einzelner Zellen erfasst, und räumliche Transkriptomik, die zeigt, wo diese Zellen in tatsächlichen Tumorschnitten lokalisiert sind. Bei der Analyse von Tumoren aus frühen und fortgeschrittenen Stadien des Mundkrebses identifizierten sie die wichtigsten Zellakteure: krebsartige epitheliale Zellen, CD8‑„Killer“‑T‑Zellen, weitere T‑ und B‑Zellen, Fibroblasten als strukturelle Stütze sowie spezialisierte Immunzellen, sogenannte myeloid‑abgeleitete Suppressorzellen (MDSCs). Während frühere Tumoren mehr aktive CD8‑T‑Zellen enthielten, zeigten Tumoren im Spätstadium schwächere T‑Zell‑Signalübertragung und stärkere immundämpfende Signale von myeloiden Zellen — ein Hinweis auf eine zunehmend feindlichere Umgebung für die krebsbekämpfende Immunität.
Wandernde Suppressorzellen
Eines der auffälligsten Ergebnisse war, wie sich die Position der MDSCs mit dem Tumorfortschreiten veränderte. In frühen Stadien neigten diese Suppressorzellen dazu, in tumorzellreichen Regionen zu clustern, nahe dem Tumorkern. In späteren Stadien verschoben sie sich nach außen und sammelten sich in tumorarmen Bereichen und an den Rändern, wo CD8‑T‑Zellen häufiger vorkamen. Das bedeutete, dass in fortgeschrittenen Tumoren die Killer‑T‑Zellen größtenteils an die Ränder gedrängt wurden und dort auf einen Gürtel aus MDSCs trafen, der ihre Fähigkeit, Krebszellen anzugreifen, dämpfte. Proben von Patientinnen und Patienten sowie Mausmodelle bestätigten, dass diese Umverteilung keine bloße Kuriosität war: Wenn MDSCs weniger mit Krebszellen überlappten und stattdessen in nicht‑tumoralen Regionen lagerten, war das mit einer schlechteren Gesamtüberlebenszeit verbunden. 
Ein Signalwechsel zwischen Krebs- und Suppressorzellen
Die Studie fokussierte eine molekulare „Unterhaltung“ zwischen Krebszellen und MDSCs, die ein Protein namens Annexin A1 (ANXA1) auf Tumorzellen und eine Familie von Rezeptoren namens FPRs auf myeloiden Zellen betrifft. In frühen Krankheitsstadien band ANXA1 auf Krebszellen stark an FPR1 und FPR3, insbesondere auf MDSCs und tumorassoziierten Makrophagen, und trug so zur Rekrutierung und zum Verbleib dieser Suppressorzellen im Tumorkern bei. Mit dem Fortschreiten des Krebses sanken die ANXA1‑Spiegel auf Tumorzellen und diese ursprünglichen Verbindungen schwächten sich. Gleichzeitig begannen mehr MDSCs, einen anderen Rezeptor, FPR2, zu exprimieren, und ANXA1–FPR2‑Signalgebung trat als kompensierender Weg auf, um MDSCs weiterhin zu binden. Eine spezifische Untergruppe von Tumorzellen mit hohem ANXA1, die auch stamzellähnliche Merkmale zeigte, schien als „Köder“ zu wirken und zog MDSCs früh an; fiel ANXA1 ab, waren MDSCs nicht mehr im Kern verankert und wanderten stattdessen in Regionen mit vielen CD8‑T‑Zellen.
Den Schutzschild ausschalten, damit Immuntherapie wirken kann
Um zu testen, ob das Unterbrechen dieser Kommunikation die Therapie verbessern könnte, verwendeten die Forschenden ein Mausmodell von Mundkrebs und blockierten FPR2 mit einem kleinen Molekülinhibitor namens WRW4. Allein führte die FPR2‑Hemmung zu einer Reduktion der MDSCs und zu mehr CD8‑T‑Zellen in der Tumorumgebung, verlangsamte aber das Tumorwachstum nicht ausreichend. Ebenso brachte eine alleinige Behandlung mit einem Anti‑PD‑1‑Checkpoint‑Antikörper nur mäßige Vorteile, weil MDSCs weiterhin eine suppressive Barriere bildeten. Als beide Wirkstoffe kombiniert wurden, wurde das Tumorwachstum jedoch deutlich zurückgedrängt und die Mäuse lebten länger. In diesen Tieren ging die MDSC‑Infiltration stark zurück, während CD8‑T‑Zellen tiefer in tumorzellreiche Regionen eindrangen — ein Hinweis darauf, dass die Blockade von FPR2 einen wichtigen Schutzschild entfernt, der Krebszellen normalerweise vor Immunangriffen schützt.
Was das für die zukünftige Krebsbehandlung bedeutet
Zusammengefasst zeigt die Arbeit, dass nicht nur die Zelltypen, sondern auch ihre räumliche Anordnung und Signalpartnerschaften darüber entscheiden, ob Immuntherapien beim oralen Krebs erfolgreich sein können. Mit dem Tumorfortschreiten wandern MDSCs vom Zentrum an die Ränder, wo sie Killer‑T‑Zellen abfangen, und die ANXA1–FPR2‑Signalgebung hilft, diese suppressive Anordnung aufrechtzuerhalten. Durch die Störung dieses Weges — besonders in Kombination mit bereits zugelassenen Checkpoint‑Medikamenten — könnten Ärztinnen und Ärzte die Tumorumgebung so umlenken, dass die körpereigenen Immunzellen Krebs wieder erkennen und zerstören. Dies legt eine konkrete Strategie nahe: Die Kombination von FPR2‑Blockern mit Immuntherapie könnte die Aussichten für Patientinnen und Patienten verbessern, deren Mundkrebserkrankungen derzeit gegen die besten verfügbaren Behandlungen resistent sind.
Zitation: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
Schlüsselwörter: Plattenepithelkarzinom der Mundhöhle, Tumormikroumgebung, myeloid‑abgeleitete Suppressorzellen, räumliche Transkriptomik, Krebsimmuntherapie