Clear Sky Science · de
FGFR-Signalgebung etabliert räumliche Gradienten sekretorischer Zellidentitäten entlang der proximal-distalen Achse der Atemwege
Wie unsere Atemwege still und leise die Luft sortieren und schützen, die wir atmen
Jeder Atemzug strömt über Millionen von Zellen, die unsere Luftröhre und Lungen auskleiden. Diese Zellen sind weit mehr als eine passive Oberfläche: sie entgiften Schadstoffe, bekämpfen Keime und helfen, kleine Lufthäute vor dem Kollaps zu bewahren. Diese Studie zeigt, dass sekretorische Zellen in der Maus-Atemwege nicht alle gleich sind. Vielmehr sind sie in sanften Gradienten vom Rachen (proximal) bis in die tiefen Lungenregionen (distal) angeordnet, und ein zentrales Signalnetzwerk, genannt FGFR2b, trägt dazu bei, diese allmählichen Verschiebungen in Zellidentität und Funktion aufzubauen und zu erhalten. Das Verständnis dieser verborgenen Ordnung liefert Einsichten, wie die Lunge gesund bleibt und was bei chronischen Lungenerkrankungen schiefgehen kann.
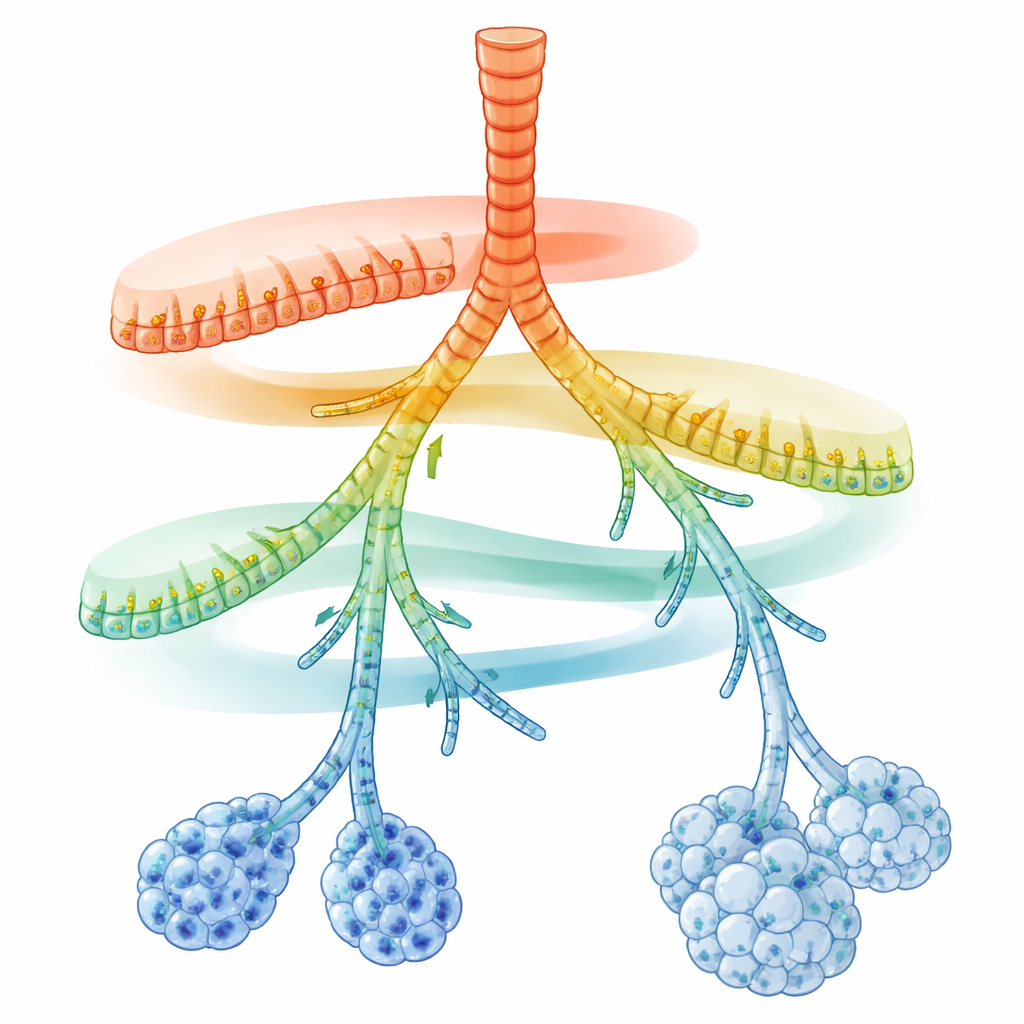
Eine verborgene Karte entlang der Atemröhren
Die Forschenden konzentrierten sich auf sekretorische Zellen, die die Atemwege auskleiden und Schleim, antimikrobielle Peptide sowie Surfactant absondern. Mithilfe von Einzelzell-RNA-Sequenzierung bestimmten sie die aktiven Gene in Tausenden einzelner Zellen aus erwachsenen Mauslungen. Als sie diese Zellen in eine Karte molekularer Ähnlichkeit projizierten, fielen sekretorische Zellen nicht in ein paar starre Typen. Stattdessen bildeten sie eine kontinuierliche Kette von Zuständen, die große Atemwege mit den winzigen Lungenbläschen verbindet. Auf einem gemeinsamen Kernprogramm zur Entgiftung eingeatmeter Chemikalien lagen zwei entgegengesetzte Genaktivitätsgradienten: in der Nähe der größeren Atemwege waren Gene für schnelle, angeborene Immunabwehr am höchsten; in Richtung der entferntesten Verzweigungen und Alveolen dominierten Gene für Lipidverarbeitung, Surfactantproduktion und Antigenpräsentation.
Aus einem Ausgangspunkt viele spezialisierte Zellzustände
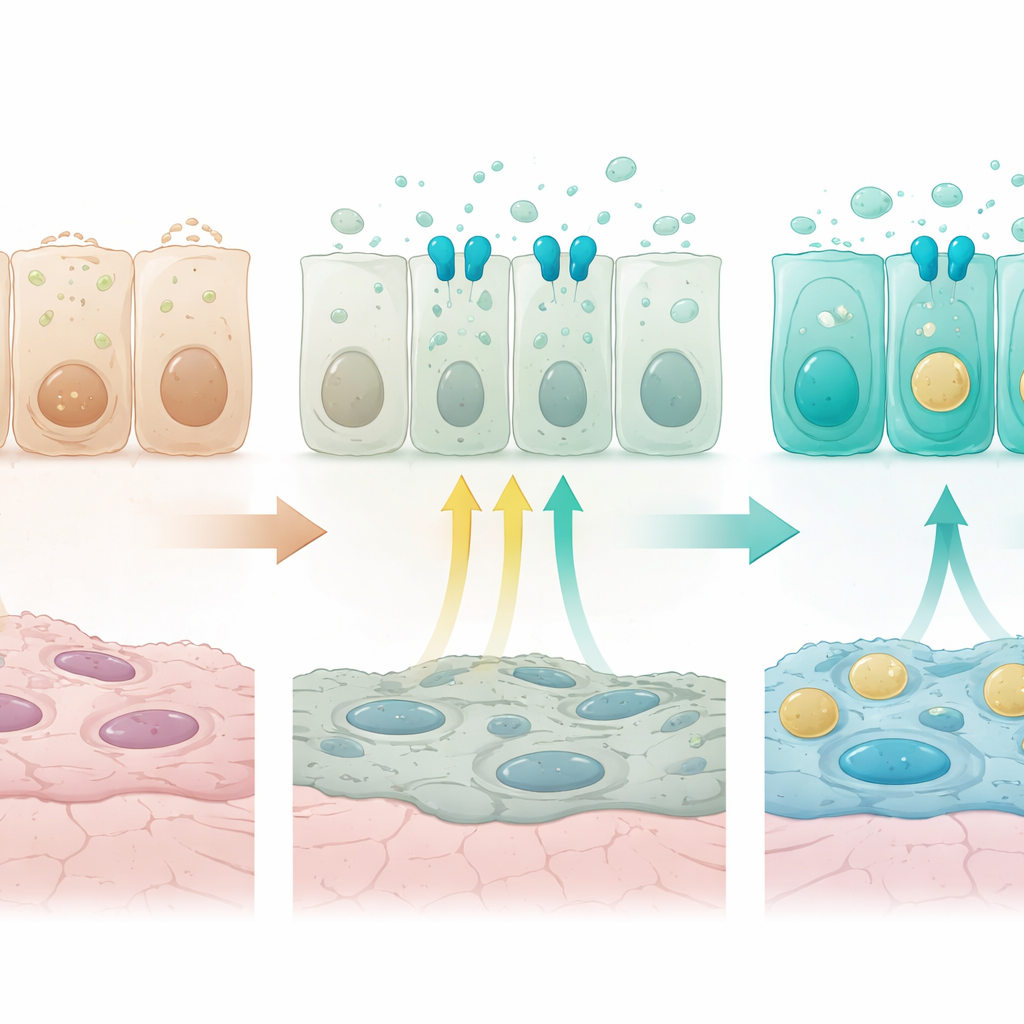
Um zu verstehen, wie dieses Muster entsteht, markierte das Team sekretorische Vorläuferzellen in der späten Fetalphase und verfolgte ihre Nachkommen über die frühe Lebenszeit mittels Linienverfolgung und Einzelzellanalyse. Diese markierten Zellen bildeten zunächst einen unreifen Pool mit starker Proteinproduktionsmaschinerie und Genen, die mit Gewebebildung verknüpft sind. Nach der Geburt, als Atmung und Kontakt mit der Außenwelt einsetzten, diversifizierten sich diese Zellen allmählich in mehrere reife Gruppen: proximale sekretorische Zellen, reich an Genen der angeborenen Abwehr; zentralere Zellen mit Entwicklungs- und Regulationssignaturen; doppelt-positive Zellen, die Atemwegs- und Alveolaridentitäten überbrücken; und alveoläre Typ-2-Zellen, spezialisiert auf Surfactant. Das Entgiftungsprogramm schaltete früh und breit ein, während Programme für angeborene Immunität und Antigenpräsentation später und in definierten Regionen aktiv wurden, was darauf hinweist, dass Merkmale sekretorischer Zellen in einer festgelegten zeitlichen Reihenfolge erworben werden.
Wie ein Wachstumsignal die distale Atemwegsidentität formt
Ein wichtiger Hinweis darauf, was diese Gradienten antreibt, stammt von einem Rezeptor namens FGFR2b, Teil eines Wachstumsfaktor-Signalwegs, der bereits als essentiell für alveoläre Typ-2-Zellen bekannt ist. FGFR2b und seine Zielgene waren in distalen Atemwegs- und Alveolarzellen stärker aktiv als in proximalen Zellen. Wenn die Forschenden FGFR2b gezielt in sekretorischen Zellen kurz nach der Geburt ausschalteten, versagte das normale distale Programm. Gene, die für Surfactantproduktion und Vesikeltransport nötig sind, gingen zurück, während Gene, die typisch für flache alveoläre Typ-1-Zellen, mitochondriale Komponenten, Ionenkanäle und Stressüberlebensfaktoren sind, zunahmen. Einige intermediäre Atemwegszellen exprimierten nun moderat sowohl proximale Abwehrmarker als auch distale Marker, wodurch das normale räumliche Muster verwischte. In Organoidkulturen aus Atemwegszellen unterdrückte die Zugabe von FGFR-Liganden proximale Abwehrmarker und stärkte Surfactant-bezogene Gene in einer Weise, die zu den in vivo-Befunden passte, und bestätigte damit, dass die Aktivierung von FGFR2b ausreichend ist, um Zellen in Richtung einer distalen sekretorischen Identität zu treiben.
Feinabstimmung durch Wechselwirkung mit anderen Signalen
Das Team untersuchte außerdem, wie FGFR2b-Signalgebung mit einem anderen Weg interagiert, der durch VEGFA getrieben wird und vor allem für die Ausbildung von Blutgefäßen bekannt ist. In Organoiden konnte VEGFA allein einige Abwehrgene abschwächen, und die Blockade seines Rezeptors veränderte bestimmte distale Marker, doch es konnte FGFR2b nicht vollständig ersetzen. Tatsächlich reduzierte der Verlust von FGFR2b in vivo die Vegfa-Expression, und kombinierte Stimulierung beider Wege führte zu einer Rückkopplung, die FGFR2b-Level senkte, was auf eine komplexe Kreuzkommunikation zwischen diesen Signalsystemen hinweist. Bei erwachsenen Mäusen veränderte das Abschalten von FGFR2b die Gradienten der angeborenen Immunität nicht mehr dramatisch, doch es war weiterhin nötig, die Expression wichtiger distaler Marker wie des Surfactant-Gens Sftpb und des klassischen sekretorischen Markers Scgb1a1 zu erhalten und hybride Atemwegs–Alveolarzellen zu bewahren.
Warum diese Gradienten für die Lungengesundheit wichtig sind
Das Bild, das sich abzeichnet, ist das einer fein abgestuften Landschaft der Atemwegsauskleidung statt eines Flickwerks isolierter Zonen. Proximale Regionen sind auf schnelle, schleimbasierte Abwehr ausgerichtet, während distale Regionen Surfactantproduktion mit spezialisierterer Immunkommunikation verbinden. Die FGFR2b-Signalgebung hilft, dieses Gefüge vor allem in den distalen Kompartimenten aufzubauen und aufrechtzuerhalten, indem sie Lipid- und Vesikelprogramme fördert und unpassende proximale Merkmale zurückhält. Das Stören dieser Gradienten, sei es durch genetische Ursachen, Umweltfaktoren oder Krankheit, könnte das Gleichgewicht zwischen Abwehr, Entgiftung und Unterstützung des Gasaustauschs verschieben und zu Zuständen beitragen, in denen distale Atemwege mehr proximale Eigenschaften annehmen. Dieser Rahmen bietet eine neue Perspektive auf Lungenerkrankungen, die den Atembaum „ummustern“, und könnte künftige Strategien zur Wiederherstellung einer richtigen zellulären Organisation leiten.
Zitation: Sountoulidis, A., Theelke, J., Liontos, A. et al. FGFR signaling establishes spatial gradients of secretory cell identities along the airway proximal-distal axis. Nat Commun 17, 2651 (2026). https://doi.org/10.1038/s41467-026-70842-0
Schlüsselwörter: Atemwegsepithelium, sekretorische Zellen, FGFR2b-Signalgebung, Lungenentwicklung, räumliche Gradienten