Clear Sky Science · de
Protonenkanäle steuern die vesikuläre Karbonatchemie in mineralisierenden Zellen eines marinen Kalkbildners
Wie winzige Baumeister unseren Planeten formen
Ein großer Teil der Kalksteinfelsen und Korallenriffe der Erde wird von mikroskopischen Baumeistern geschaffen, die gelöste Bestandteile aus dem Meerwasser entnehmen und in festen Stein verwandeln. Diese Studie blickt in einen solchen Baumeister – die Larvenphase eines Seeigels – und stellt eine überraschend grundlegende Frage: Wie kontrollieren seine Zellen den Säuregrad, während sie ein Skelett aus Calciumcarbonat aufbauen? Die Antwort offenbart einen eleganten elektrischen Trick, der möglicherweise auch erklärt, warum marine Schalenbildner gegenüber einem saurer werdenden Ozean so empfindlich sind.
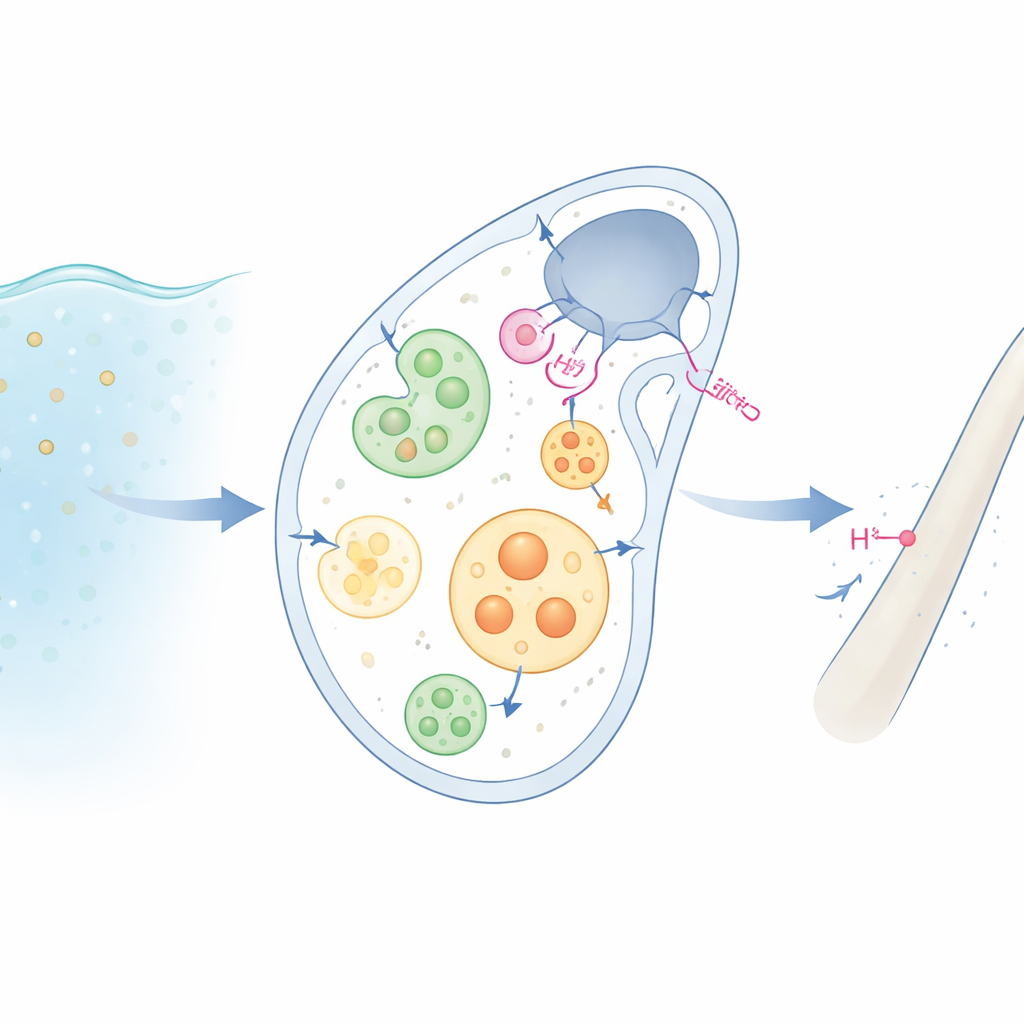
Vom Meerwasser zum Skelett
Seeigel-Larven verhärten ihren Körper mit winzigen Calcitstäbchen aus Calciumcarbonat. Dazu nehmen spezialisierte „mineralisierende“ Zellen zunächst Meerwasser auf und verpacken es in kleine innere Tröpfchen, sogenannte Vesikel. In diesen Tröpfchen werden die Baustoffe für das Mineral – Calcium, Karbonat und andere Ionen – zu einem amorphen, glasigen Vorläufer konzentriert, der später zu kristallinem Material aushärtet. Doch bei jeder Bildung von Calciumcarbonat entsteht zusätzliche Säure (Protonen). Würde diese Säure sich ansammeln, würde sie das Mineral, das die Zellen zu bilden versuchen, wieder auflösen. Wie die Zellen diese Selbstzerstörung verhindern, war ein lange offenes Rätsel.
Den Säuregrad in bewegten Tröpfchen messen
Die Forschenden nutzten Live‑Imaging und pH‑sensitive Fluoreszenzfarbstoffe, um die Chemie innerhalb dieser Vesikel in Echtzeit zu verfolgen. Sie stellten fest, dass fast die Hälfte der Vesikel stark alkalisch war – basischer als normales Meerwasser –, während der Rest neutral oder leicht sauer war. Als sie kurzzeitig den pH‑Wert des umgebenden Meerwassers veränderten, reagierten sowohl das Zellinnere als auch die Vesikel, was zeigt, dass Protonen relativ frei über diese Membranen wandern können. Die Vesikel waren jedoch teilweise abgeschirmt gegenüber dem Zellinneren: Ihre Reaktion war langsamer und weniger ausgeprägt, was auf eine kontrollierte „Leckigkeit“ hindeutet, die hilft, günstige Bedingungen für die Mineralbildung aufrechtzuerhalten.
Elektrische Lecks, die Säure entfernen
Um herauszufinden, was diese Leckigkeit erzeugt, konzentrierte sich das Team auf ein Protonenkanalprotein namens Otop2l, das zuvor mit dem Skelettwachstum von Seeigeln in Verbindung gebracht worden war. Mit Antikörpern beobachteten sie, dass Otop2l nicht nur in der äußeren Membran der mineralisierenden Zellen sitzt, sondern auch auf den Membranen großer interner Vesikel. Wenn sie Otop2l mit einem gezielten genetischen Blocker reduzierte, wurden sowohl die Zellen als auch ihre Vesikel weniger reaktionsfähig gegenüber Änderungen des äußeren pH‑Werts, was darauf hindeutet, dass dieser Kanal eine Hauptroute für den Protonenabfluss darstellt. Elektrische Aufnahmen in Froscheiern und in menschlichen Zellen, die so verändert wurden, dass sie Otop2l produzieren, zeigten, dass der Kanal sich bei alkalischen Bedingungen und in Anwesenheit von Calcium und Magnesium weit öffnet – genau die Situation in kalzifizierenden Vesikeln. Im Wesentlichen nutzen die Zellen ihren natürlichen Spannungsunterschied über die Membran zusammen mit Otop2l, um Säure hinauszutreiben, ohne viel metabolische Energie aufzuwenden.
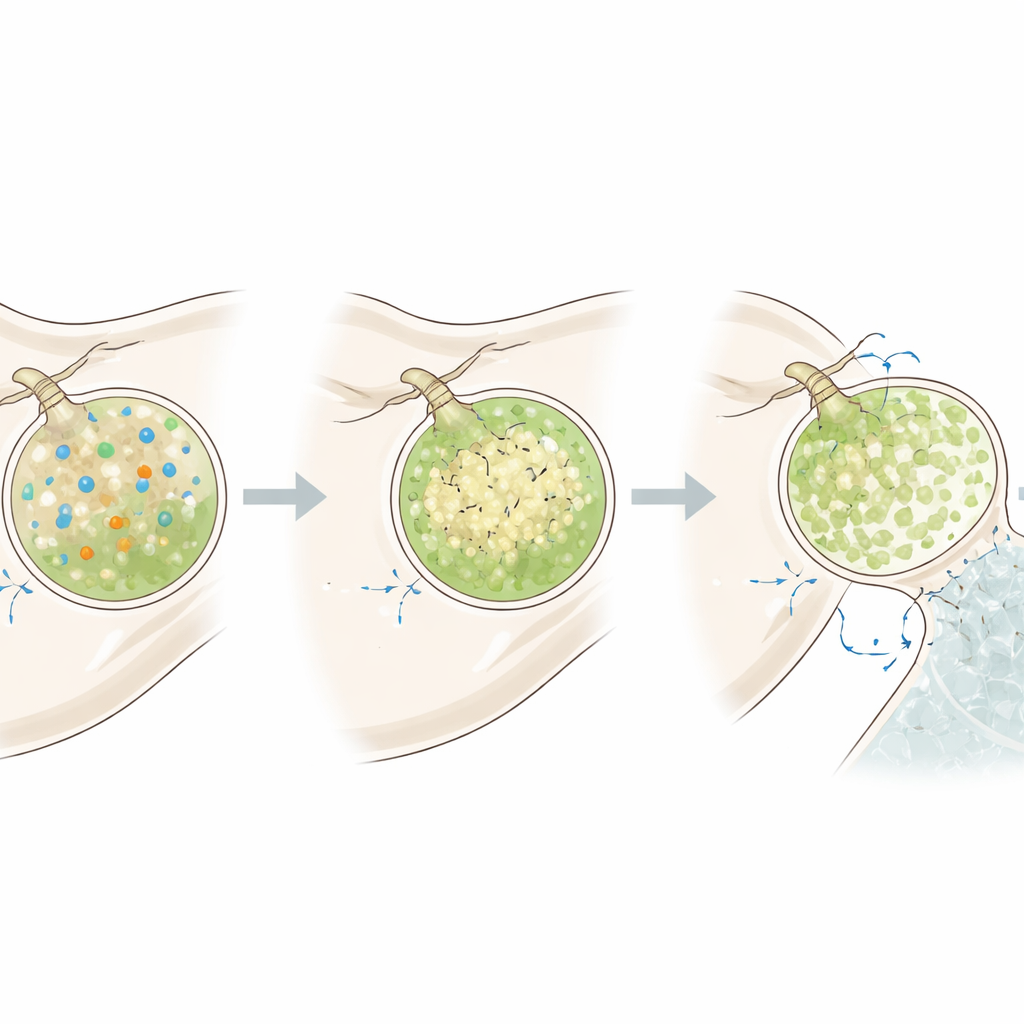
Vesikel schalten hoch für die Reparatur
Das Team untersuchte dann, was passiert, wenn die Larven ihr Skelett nach einer Beschädigung wieder aufbauen müssen. Sie lösten die Larvenskelette, indem sie sie kurzzeitig niedrigem pH‑Wert aussetzten, setzten sie dann wieder normalem Wasser aus und verfolgten die Vesikel während des Nachwachsens. In dieser Phase hoher Nachfrage produzierten die mineralisierenden Zellen insgesamt mehr Vesikel, mit einem starken Anstieg alkalischer, calciumreicher Vesikel. Diese Vesikel konnten ihren hohen pH‑Wert nach einem Säurepuls schneller wiederherstellen, und auch das Zellinnere wurde alkalischer. Dennoch blieb das elektrische Potenzial der Zellen ähnlich, was darauf hindeutet, dass sie sich hauptsächlich anpassen, indem sie die Karbonatzufuhr und die Protonenleitfähigkeit erhöhen, statt ihren elektrischen Zustand grundlegend zu ändern.
Warum Ozeanversauerung relevant ist
Insgesamt stützen die Ergebnisse ein Modell, in dem die mineralisierenden Zellen von Seeigeln ein „offenes“ System betreiben: Sie nehmen kontinuierlich Meerwasser über Endozytose auf, pumpen Kohlenstoff in Vesikel und verlassen sich auf Protonenkanäle und Membranspannung, um überschüssige Säure zurück ins umgebende Meer abzugeben. Dieses System ist effizient, solange der externe pH‑Wert innerhalb des engen, stabilen Bereichs bleibt, der einen großen Teil der jüngeren Erdgeschichte charakterisiert hat. Wird das Meerwasser jedoch saurer – wie es heute bei steigendem Kohlendioxid der Fall ist –, kann dieser Ausstrom von Protonen abgeschwächt oder sogar umgekehrt werden. Die Arbeit liefert daher mechanische Einsichten, warum viele marine Kalkbildner unter Ozeanversauerung zu kämpfen haben: Gerade die Kanäle, die einst die Biomineralisation kostengünstig und robust machten, können in einem sich rasch verändernden Meer zu einer Belastung werden.
Zitation: Jonusaite, S., Przibylla-Diop, C., Musinszki, M. et al. Proton channels govern vesicular carbonate chemistry in mineralizing cells of a marine calcifier. Nat Commun 17, 2578 (2026). https://doi.org/10.1038/s41467-026-70837-x
Schlüsselwörter: Biomineralisation, Seeigel-Larven, Protonenkanäle, Ozeanversauerung, Calciumcarbonat