Clear Sky Science · de
SMART: räumliche Multi-Omic-Aggregation mithilfe graphneuraler Netze und Metric Learning
Gewebe als Nachbarschaftskarten sehen
Unser Körper besteht aus pulsierenden zellulären Nachbarschaften, in denen Gene, Proteine und die Verpackung der DNA an genau definierten Orten zusammenwirken. Neue Mikroskope und Sequenzierverfahren können inzwischen viele dieser molekularen Ebenen direkt in dünnen Gewebeschnitten erfassen, doch aus dieser Flut mehrschichtiger, räumlicher Daten klare Bilder darüber zu gewinnen, wie Organe organisiert sind, ist eine große rechnerische Herausforderung. Diese Studie stellt SMART vor, eine Methode, die Forschenden hilft, diese komplexen Signale zu einem detaillierten Lageplan zusammenzuführen, wo verschiedene Zellgemeinschaften vorkommen und wie sie angeordnet sind.
Warum das Kartieren zellulärer Nachbarschaften schwierig ist
Moderne „räumliche Multi-Omics“-Technologien messen mehrere Arten molekularer Information gleichzeitig – etwa RNA, Oberflächenproteine und wie offen oder geschlossen die DNA ist – und behalten dabei die genaue Position jeder Messung in einem Gewebeschnitt bei. Jede Omic-Perspektive liefert einen anderen Blick auf Zellverhalten, ist aber rauschbehaftet, hochdimensional und nicht von vornherein aufeinander abstimmbar. Darüber hinaus sind Zellen desselben Typs nicht immer zusammengeclustert; sie können als verstreute Inseln im Organ auftreten. Bestehende Softwarewerkzeuge vernachlässigen oft die räumliche Anordnung, vereinfachen die Beziehungen zwischen den Omics zu stark oder haben Schwierigkeiten, mit den sehr großen Datensätzen klarzukommen, die neue Instrumente erzeugen können.
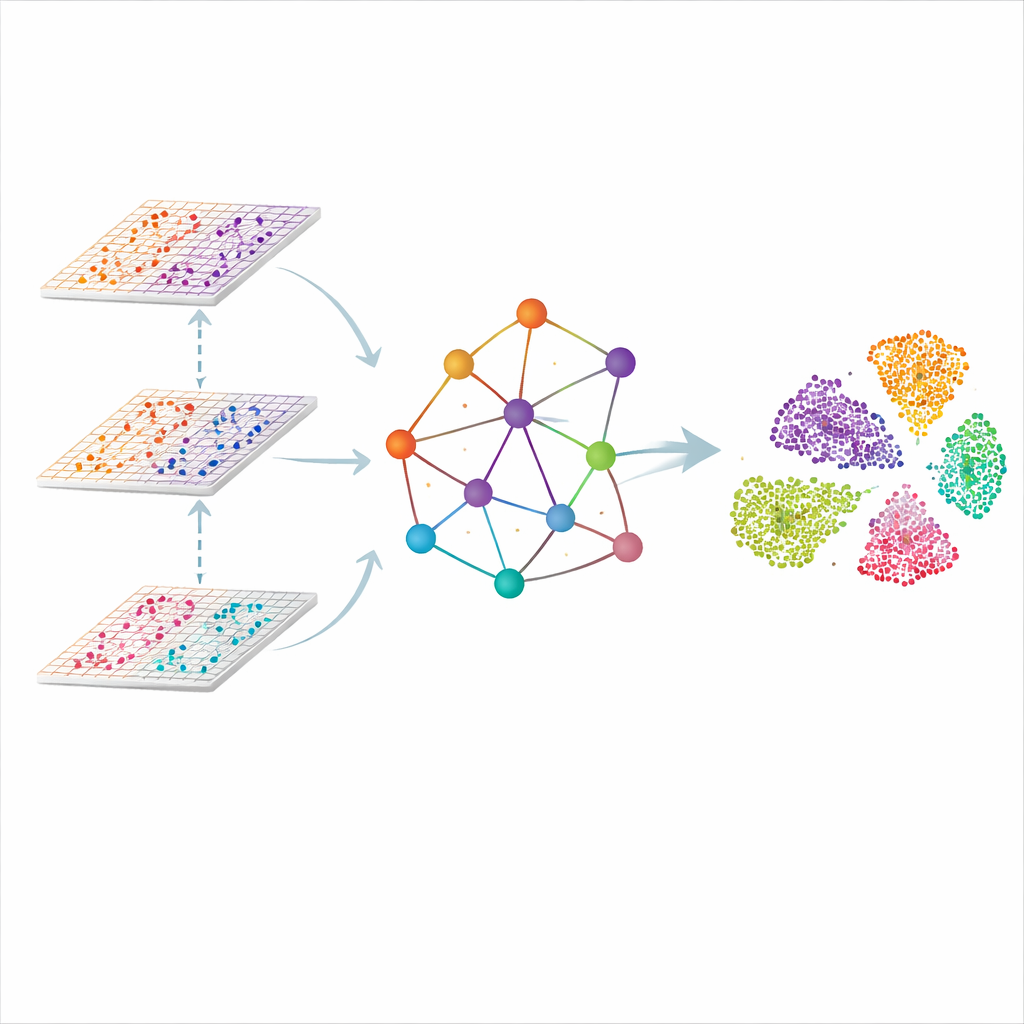
Ein Graph des Gewebes, nicht nur eine Liste von Zellen
SMART geht das Problem an, indem jede Messstelle im Gewebe als Knoten in einem Netzwerk betrachtet wird. Nahegelegene Punkte werden zu einem räumlichen Graphen verbunden, und die molekularen Messwerte jeder Omic-Ebene werden zunächst in eine kleinere Menge koordinierter Merkmale komprimiert, die Gesamtmuster besser erfassen als einzelne Gene. Eine Form neuronaler Netze, die für Graphen entworfen ist, leitet dann Informationen entlang der Kanten weiter, sodass jeder Punkt von seinen Nachbarn „hört“, dabei aber verfolgt wird, wie jede Omic-Ebene beiträgt. Das Ergebnis ist eine gemeinsame, niedrigdimensionale Darstellung, in der ähnliche Regionen im Gewebe – etwa verschiedene Schichten des Gehirns oder Bereiche eines Lymphknotens – sich von selbst gruppieren.
Dem Modell beibringen, was ähnlich sein sollte
Allein den physischen Nachbarn zu folgen reicht nicht aus, weil Zellen gleichen Typs weit auseinanderliegen können. SMART ergänzt das durch eine zweite Zutat aus der Gesichtserkennung: Metric Learning mit Triplets. Für jeden Punkt findet die Methode automatisch einen anderen Punkt mit sehr ähnlichen molekularen Mustern (ein „Positiver“) und einen, der deutlich anders ist (ein „Negativer“). Dann passt sie die interne Repräsentation so an, dass Positive näher zusammengezogen und Negative weiter auseinandergeschoben werden, selbst wenn sie auf dem Gewebeschnitt räumlich weit entfernt sind. Dieses Ziehen und Schieben läuft parallel zu einem Rekonstruktionsschritt, der SMART dazu zwingt, die wesentlichen Details jeder Omic-Ebene zu bewahren und so räumliche Kontinuität mit molekularer Spezifität auszugleichen.
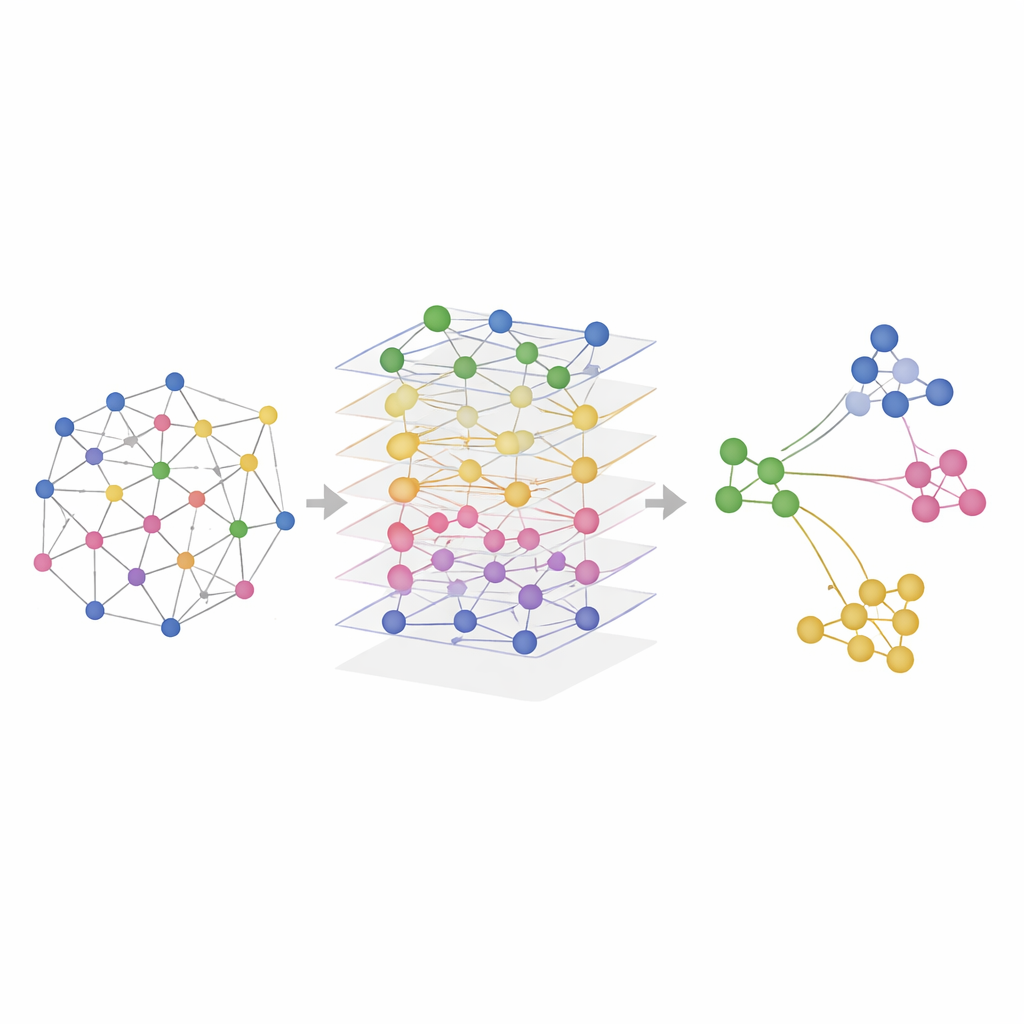
SMART in echten Geweben auf die Probe gestellt
Die Forschenden testeten SMART sowohl an simulierten Daten als auch an realen Experimenten, die Kombinationen aus RNA-, Protein- und Chromatin-Accessibility-Messungen in Mausgehirnen, Maussplenien, menschlichen Lymphknoten und Tonsillen erfassten. In kontrollierten Simulationen, in denen die wahren räumlichen Regionen bekannt waren, erholte SMART die tatsächlichen Muster am zuverlässigsten und bewahrte die Beziehungen in jeder Omic-Ebene. Bei realen Datensätzen identifizierte SMART konsistent feine anatomische Strukturen – etwa spezifische Hirnregionen oder Immunzonen in lymphatischen Organen – klarer als konkurrierende Methoden und hielt gleichzeitig die Rechenanforderungen niedrig. Eine verwandte Variante, SMART‑MS, überträgt dieselben Ideen auf mehrere Gewebeschnitte, richtet Schnitte desselben Organs aus und korrigiert technische Unterschiede zwischen Experimenten.
Schnelle Karten für die nächste Welle der räumlichen Biologie
Einfach gesagt ist SMART eine Karten-Engine für die nächste Generation molekularer Atlanten. Indem es netzwerkartige Modellierung der Gewebeanordnung mit einem eingebauten Verständnis dafür kombiniert, was als „ähnlich“ gelten sollte, kann es riesige, unordentliche Sammlungen räumlicher Multi-Omics-Messungen in kohärente Nachbarschaftskarten von Organen verwandeln. Das ermöglicht Forschenden, leichter zu erkennen, wo bestimmte Zelltypen und Mikro‑Umgebungen liegen, wie sie sich während Entwicklung oder Krankheit verändern und wie neue experimentelle Technologien zusammenpassen. Da räumliche Daten weiter an Größe und Komplexität zunehmen, werden Werkzeuge wie SMART und SMART‑MS entscheidend sein, um Rohmessungen in biologische Einsichten zu verwandeln.
Zitation: Du, Z., Chen, Q., Huang, W. et al. SMART: spatial multi-omic aggregation using graph neural networks and metric learning. Nat Commun 17, 2876 (2026). https://doi.org/10.1038/s41467-026-70821-5
Schlüsselwörter: räumliche Multi-Omics, graphneuronale Netze, Gewebe-Mikroumgebung, Datenintegration, Einzelzellbiologie