Clear Sky Science · de
Ein einzelner Cluster von RNA-Polymerase-II-Molekülen ist stabil mit aktiven Genen assoziiert
Wie Zellen Gene in kraftvollen Schüben einschalten
Jede Zelle in Ihrem Körper muss entscheiden, welche Gene sie nutzt und wann — oft schaltet sie sie in kurzen, intensiven Schüben an. Jahrzehntelang vermuteten Forscher, dass die Enzyme, die DNA ablesen, sich in winzigen "Hotspots" im Zellkern sammeln, um diesen Prozess zu verstärken, doch wie diese Cluster funktionieren, war umstritten. Diese Studie blickt mit fortschrittlichen Mikroskopen in lebende Fruchtfliegen-Embryonen und zeigt, dass jedes aktive Gen mit genau einem stabilen Cluster des Enzyms verbunden ist, das DNA in RNA umschreibt, und dass sich diese Cluster eher wie belebte Arbeitsplätze verhalten als wie exotische Tröpfchen zellulären "phasenseparierten" Materials.
Kleine Maschinen, die das Genom lesen
Das Enzym im Zentrum dieser Geschichte ist die RNA-Polymerase II, eine molekulare Maschine, die entlang der DNA gleitet und Gene in RNA kopiert — der erste Schritt auf dem Weg zu Proteinen. Frühere Arbeiten lieferten widersprüchliche Bilder: Manche Experimente legten nahe, dass Polymerase-Moleküle in großen, langlebigen "Fabriken" zusammenkommen, die viele Gene gleichzeitig bedienen, während andere nur flüchtige Ansammlungen weniger Moleküle beobachteten. Die Autoren konzentrierten sich auf einen dramatischen Moment in der frühen Entwicklung der Fruchtfliege, die zygotische Genomaktivierung, in der ein zuvor ruhender Embryo plötzlich tausende seiner eigenen Gene einschaltet. Diese natürliche Aktivitätswelle bot ein kraftvolles Testfeld, um in Echtzeit zu beobachten, wie sich Polymerase-Moleküle bewegen, zusammentreffen und mit Genen interagieren.
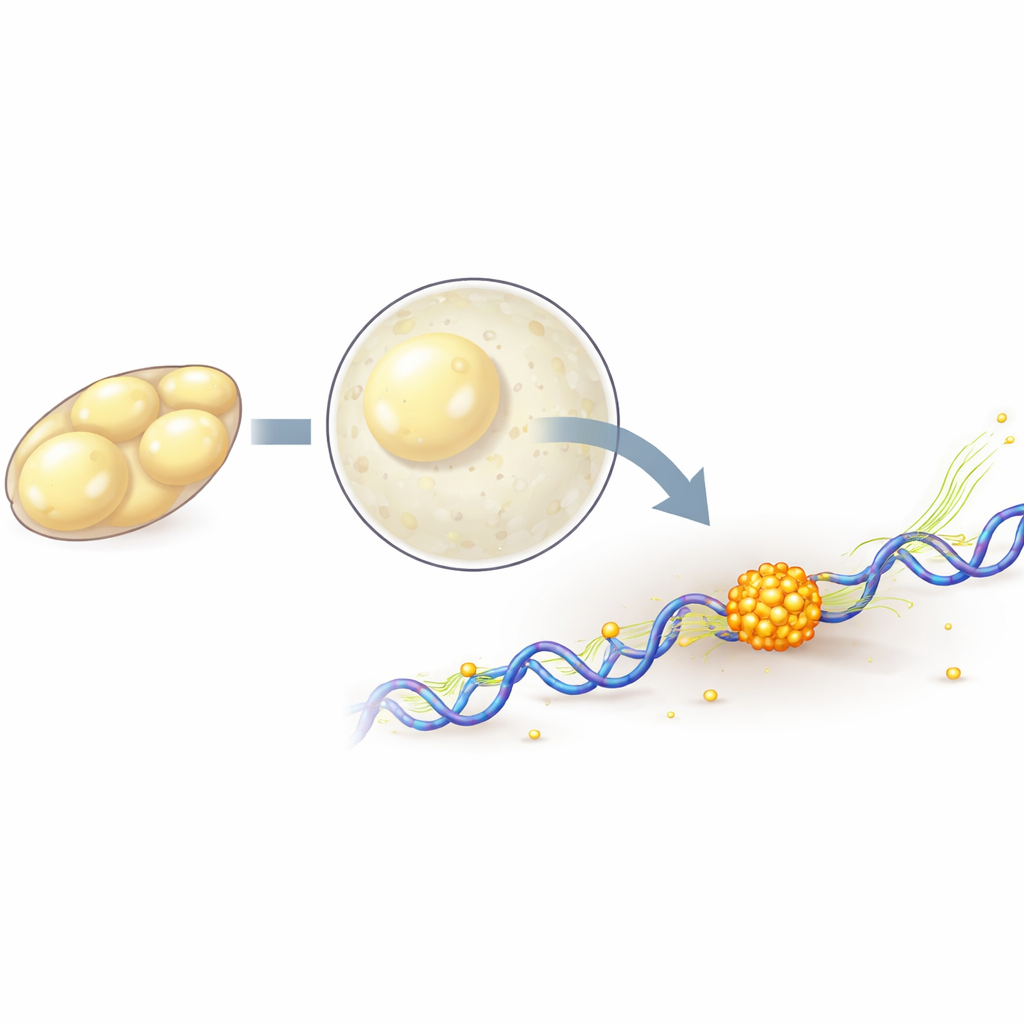
Einzelne Moleküle in einem lebenden Embryo beobachten
Um einzelnen Polymerase-Molekülen zu folgen, markierte das Team genetisch eine ihrer Kernkomponenten mit fluoreszierenden Proteinen und nutzte dann Lattice-Light-Sheet-Mikroskopie sowie Einzelmolekül-Tracking, um ihre Bewegung dreidimensional, schnell und mit schonender Beleuchtung aufzuzeichnen. Sie fanden heraus, dass beim Eintritt des Embryos in die große Aktivierungsphase mehr Polymerase-Moleküle fest an die DNA gebunden sind, was mit einer erhöhten Genaktivität übereinstimmt. Durch kurzes Blockieren unterschiedlicher Schritte des Transkriptionszyklus mit Wirkstoffen konnten sie Moleküle unterscheiden, die gerade an einem Gen zu starten beginnen, von solchen, die aktiv entlang des Gens elongieren. Diese Analyse zeigte, dass die Clusterbildung von den sehr frühen Schritten des Geneinschaltens abhängt, während aktives Kopieren entlang des Gens die Cluster tendenziell abschwächt und verkürzt.
Cluster, die sich im Verlauf der Entwicklung verändern
Die Bildgebung ganzer Zellkerne über die Zeit zeigte Dutzende kleiner Polymerase-Cluster lange bevor die genomweite Aktivierungswelle einsetzte, deren Zahl und Abstand sich änderten, während sich die Kernteilungen verlangsamten. Früh in der Entwicklung halten viele Cluster nahezu so lange an wie die Lücke zwischen Zellteilungen, was darauf hindeutet, dass sie von Polymerasen in einem frühen, "vorgespielten" Zustand dominiert werden, der häufig keine vollständigen RNA-Moleküle produziert. Später, wenn die Transkription anzieht, werden die Cluster dynamischer: ihre Lebensdauern folgen nicht mehr einfach dem Zellzyklus, und ihre interne Zusammensetzung verschiebt sich zugunsten von Polymerasen, die tatsächlich entlang der Gene elongieren. Weitere Messungen der Molekülbewegung innerhalb und außerhalb der Cluster deuten darauf hin, dass Polymerase-Moleküle in der Nähe aktiver Gene stärker eingeengt sind und wahrscheinlich häufiger an dieselben Stellen zurückstoßen — ein Befund, der eher für eine lokal geschäftige Arbeitszone als für einen lockeren, flüssigen Tropfen spricht.
Ein Cluster, ein Gen während eines Bursts
Um Cluster direkt mit Genoutput zu verknüpfen, beobachteten die Forscher spezifische Reporter-Gene, die dort aufleuchten, wo neue RNA entsteht, während sie gleichzeitig Polymerase verfolgten. Für mehrere verschiedene Gene sahen sie konsequent nur einen Polymerase-Cluster an jeder aktiven Genkopie während eines Transkriptionsbursts. Die Intensität des Clusters stieg und fiel synchron mit der Menge an entstehender (naszierender) RNA, und wenn sich duplizierte Schwesterkopien eines Gens auflösen ließen, trug jede ihre eigene, separate Ansammlung statt einer gemeinsamen. Computersimulationen, auf die Bildgebungsbedingungen abgestimmt, zeigten, dass Gene mit starker Polymerase-Beladung sichtbare Cluster bilden, während schwächere Gene möglicherweise weiterhin Polymerase rekrutieren, aber zu schwach leuchten, um erkannt zu werden — was erklärt, warum nur eine Minderheit aktiver Gene im Mikroskop klare Cluster zeigt.
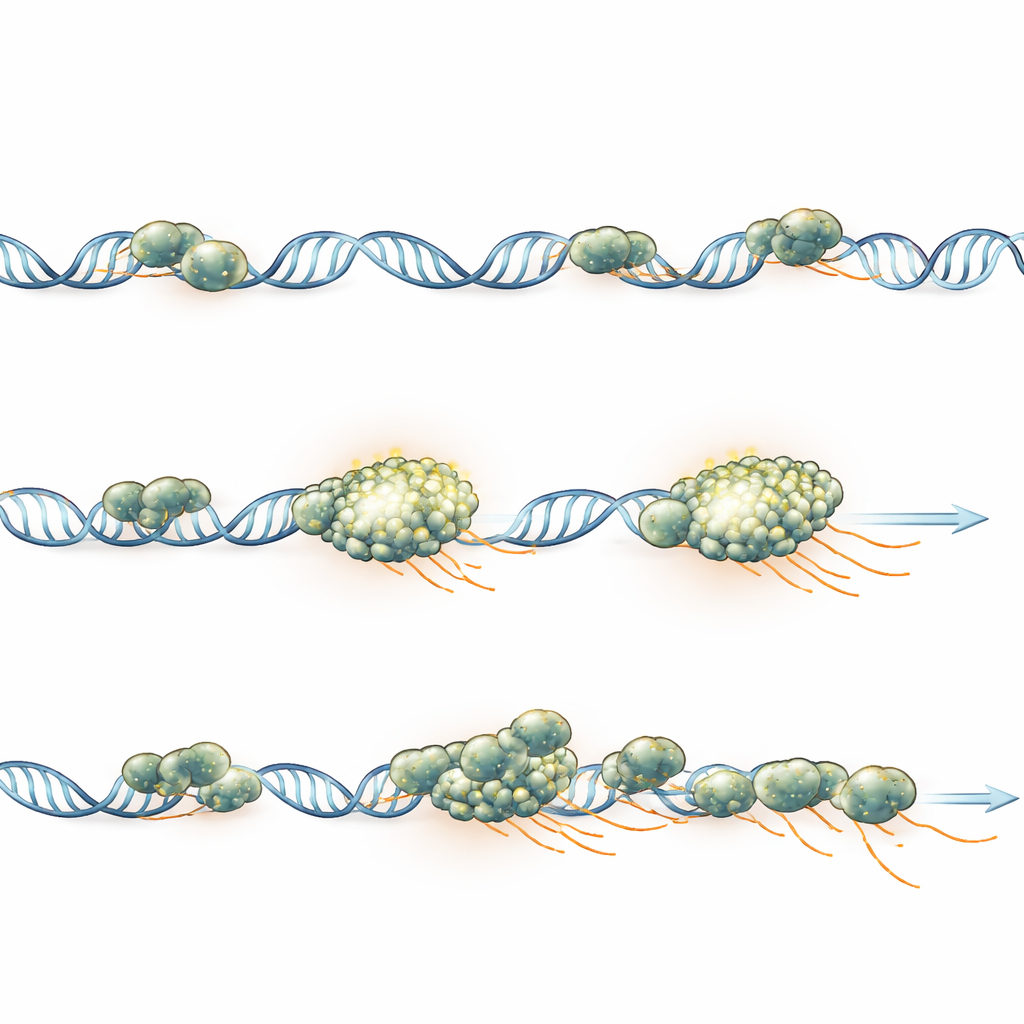
Was das für die Genkontrolle bedeutet
Diese Arbeit legt nahe, dass Cluster in diesen Embryonen hauptsächlich widerspiegeln, wie viele Enzyme an ein einzelnes Gen aktiv gebunden sind, und nicht eine separate "Fabrik" oder einen speziellen Tropfen, der erst entstehen müsste, damit Transkription möglich ist. Ein Cluster erscheint, wenn viele Polymerasen in schneller Folge geladen werden, bleibt während eines Aktivitätsbursts stabil mit genau diesem Gen assoziiert und löst sich allmählich auf, wenn Polymerasen das Kopieren beenden und abwandern. Für nichtfachliche Leser lautet die Kernaussage: Das Umschalten von Genen ist organisiert durch fokussierte, genbezogene Aktivitätshubs — jedes aktive Gen sammelt vorübergehend sein eigenes Team von Kopiermaschinen, und Größe sowie Lebensdauer dieses Teams spiegeln direkt wider, wie stark das Gen eingeschaltet ist.
Zitation: Mukherjee, A., Kapoor, M., Shankta, K. et al. A single cluster of RNA Polymerase II molecules is stably associated with active genes. Nat Commun 17, 2580 (2026). https://doi.org/10.1038/s41467-026-70775-8
Schlüsselwörter: Clustering der RNA-Polymerase II, zygotische Genomaktivierung, Transkriptions-Bursts, Genregulation in Embryonen, Einzelmolekül-Bildgebung