Clear Sky Science · de
Synthetische Aptamer-Mechanorezeptoren ermöglichen zellspezifische Kraftmessung und zeitliche Steuerung über DNA-Schaltkreise
Zellen zuhören durch sanfte Ziehkräfte
Unser Körper ist voller Zellen, die ständig an ihrer Umgebung ziehen und drücken und mit winzigen Kräften entscheiden, wann sie wachsen, sich bewegen oder sich verändern. Diese Studie beschreibt eine neue Methode, um diesen Kräften mit DNA-basierten Geräten nachzuspionieren, die auf bestimmte Zelltypen einstellbar sind und zeitlich ein- und ausgeschaltet werden können. Solche Technologien könnten eines Tages Ingenieuren helfen, Gewebeformation zu steuern, das Verhalten von Tumoren zu verstehen oder intelligente Materialien zu entwickeln, die in Echtzeit auf lebende Zellen reagieren.
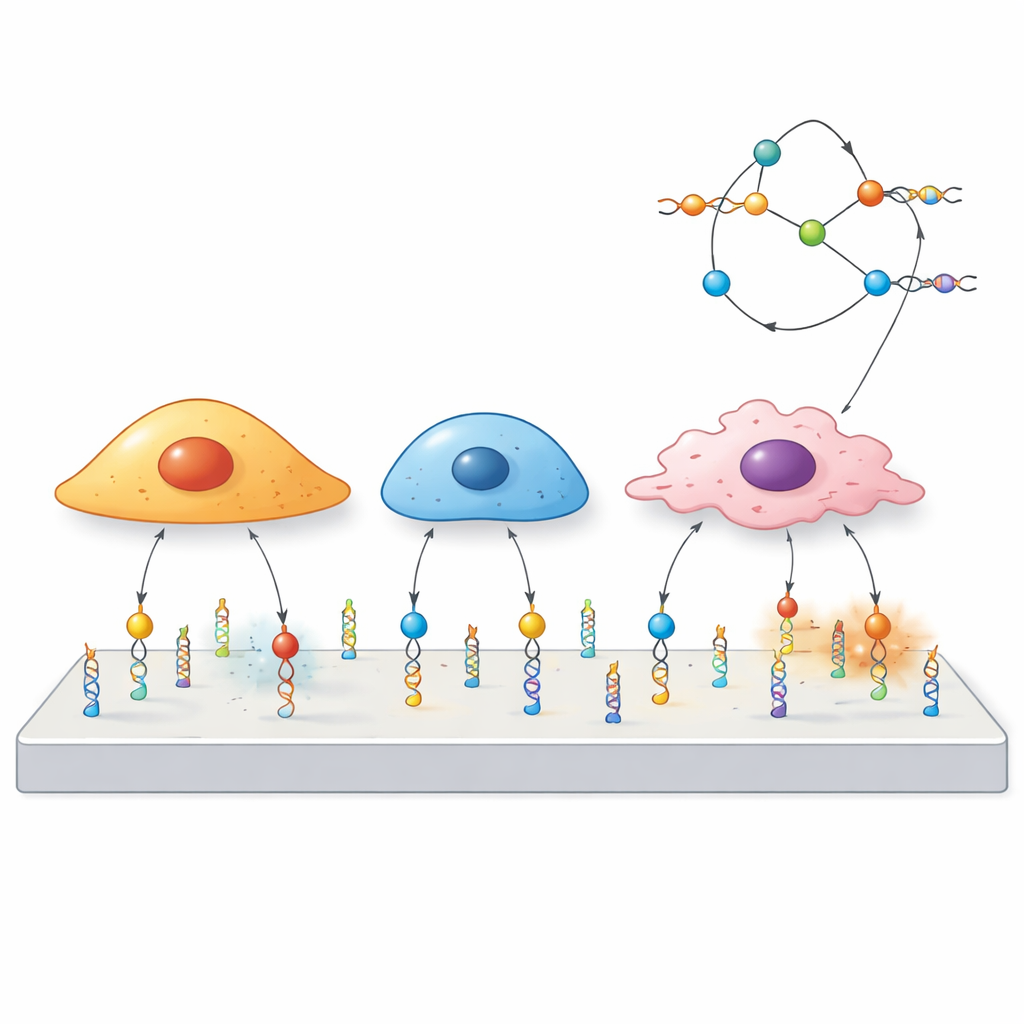
DNA als winziger mechanischer Schalter
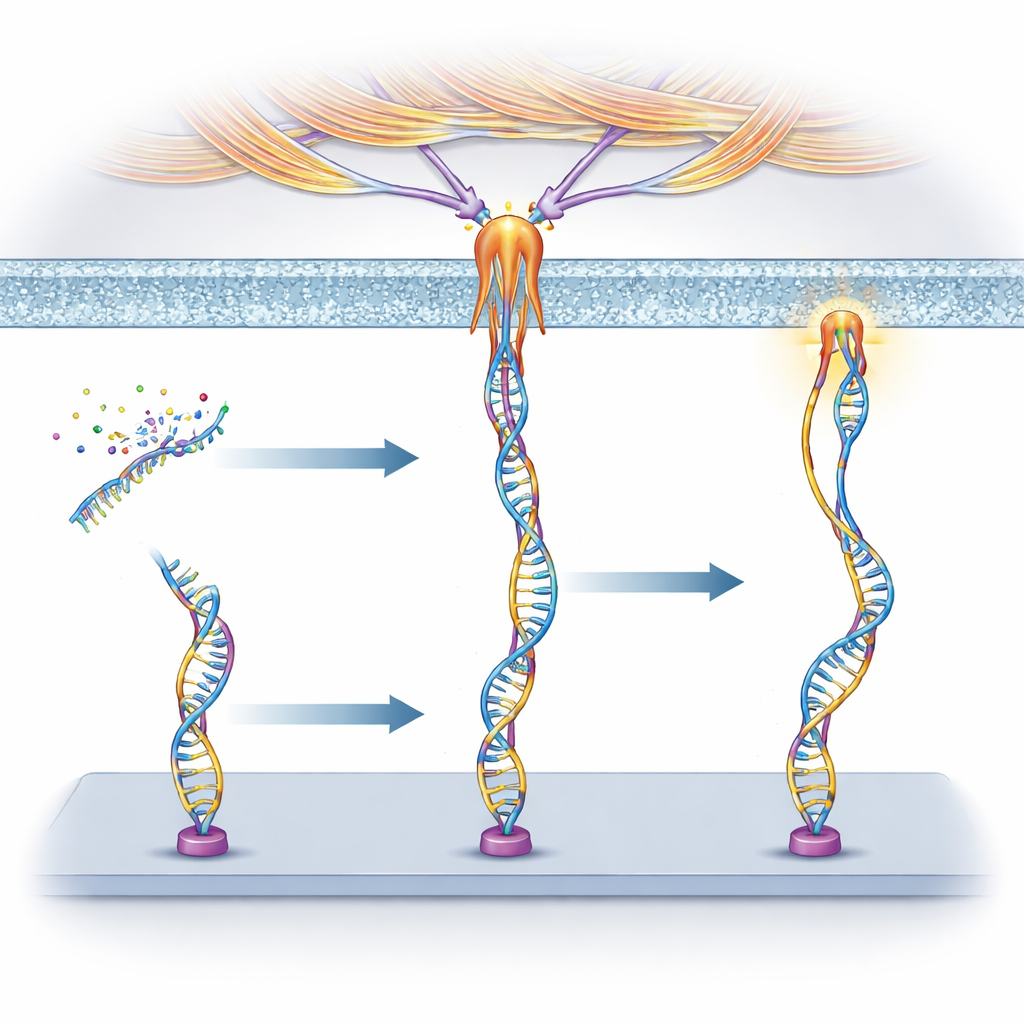
Die Forscher bauten "Mechanosonden" aus DNA, demselben Molekül, das genetische Information trägt. Jede Sonde hat drei Teile: eine kurze DNA-Sequenz, das Aptamer, das an ein gewähltes Protein auf der Zelloberfläche bindet; ein gepaartes DNA-Segment, das wie eine Feder wirkt und bei einer bestimmten Kraft bricht; und einen fluoreszierenden Farbstoff, der aufleuchtet, wenn diese Feder schnappt. Zieht eine Zelle stark genug an dem vom Aptamer gebundenen Rezeptor, öffnet sich das DNA-Duplex und das Signal schaltet sich ein. Weil verschiedene Aptamere an unterschiedliche Rezeptoren binden, kann das Team im Voraus festlegen, welche Zellen oder Proteine die Sonde auslösen können.
Verborgene Kraftwege auf Zelloberflächen aufspüren
Die meisten vorhandenen Kraftsensoren konzentrieren sich auf Integrine, gut bekannte Proteine, die Zellen helfen, sich zu verankern, aber in vielen Zelltypen vorkommen und daher wenig Selektivität bieten. Hier zielte das Team stattdessen auf "nicht-kanonische" Rezeptoren, die normalerweise nicht als mechanisch angesehen werden. Sie zeigten, dass ein Aptamer namens AS1411, das an ein Protein namens Nucleolin bindet, das bei Krebszellen verbreitet ist, nur dann ein Signal erzeugte, wenn es sein Ziel spezifisch erkennen konnte. Durch die Konstruktion von Sonden, die entweder bei geringeren oder höheren Kräften öffnen mussten, entdeckten sie, dass Nucleolin im Vergleich zu Integrinen nur mäßige Kräfte überträgt und für sich genommen nicht dazu beiträgt, dass Zellen auf einer Oberfläche auseinanderlaufen. Im Gegensatz dazu konnte ein anderes Aptamer, Sgc8, das den Rezeptor PTK7 erkennt, Kräfte melden, selbst wenn die Zellen kaum haften, und zeigte ringförmige Muster, die auf eine andere Quelle der Bewegung hindeuteten.
Herkunft der Kräfte nachzeichnen
Um zu verstehen, was an diesen DNA-Geräten zog, verwendeten die Forscher Wirkstoffe, die gezielt verschiedene Zellprozesse blockieren. Für Nucleolin stellten sie fest, dass dessen Kräfte stark von Myosin abhingen, demselben Motorprotein, das Muskelkontraktion unterstützt, und an Stellen auftraten, an denen die Zelle Fokaladhäsionen bildet—spezielle Kontaktpunkte zum Greifen und Wahrnehmen von Steifigkeit. Das legt nahe, dass Nucleolin indirekt mit der internen Aktin‑Myosin‑Maschinerie der Zelle verbunden ist und deren kontraktile Kräfte teilen kann. Für PTK7 allerdings reduzierte die Blockade eines Prozesses namens Makropinozytose—bei dem Zellen ihre Membran wühlen und Flüssigkeit aufnehmen—die Signale stark. Die Kräfte entstanden hauptsächlich durch frühes Membran‑Ruffling, angetrieben vom Aktinwachstum, nicht durch spätere Schritte beim Vesikelschluss, was einen eigenen mechanischen Pfad offenbart.
Zellselektivität mit molekularer Präzision einstellen
Da jedes Aptamer einen bestimmten Oberflächenrezeptor erkennt, lässt sich dasselbe DNA‑Gerüst einfach neu programmieren, indem man ein Aptamer gegen ein anderes austauscht. Das Team demonstrierte dies mit Sonden für drei verschiedene Ziele—PTK7, Mucin‑1 und EpCAM—über ein Panel von Krebszelllinien mit hohen oder niedrigen Mengen der jeweiligen Proteine. Zellen, die reich an einem bestimmten Rezeptor waren, erzeugten starke Signale, während Zellen mit wenig Rezeptor kaum reagierten, selbst wenn sie zusammen in derselben Schale kultiviert wurden. Auffällig war, dass Zellen mit demselben Rezeptor dennoch unterschiedliche räumliche Kraftmuster zeigen konnten, was unterstreicht, dass der Kraftfluss durch einen Rezeptor nicht nur von seiner Präsenz, sondern auch von der inneren Verschaltung des jeweiligen Zelltyps abhängt.
Programmieren, wann Zellen ziehen dürfen
Indem sie ausnutzen, dass Aptamere aus DNA bestehen, verbanden die Forscher ihre Sonden mit DNA‑Reaktionsnetzwerken, die steuern, ob das Aptamer überhaupt binden kann. Komplementäre "Blocker"‑Stränge können das Aptamer vorübergehend verbergen, und "Aktivator"‑Stränge können später die Blocker durch Strangaustausch entfernen und die Kraftempfindlichkeit wiederherstellen. Sie entwarfen außerdem einen RNA‑basierten Blocker, der von einem Enzym namens RNase H geschnitten werden kann, und verlangsamten dieses Schneiden weiter mit Ködermolekülen, die um das Enzym konkurrieren. Auf diese Weise wandelten sie das Mechano‑Sensing in ein zeitlich gesteuertes Programm: Zellen konnten Signale nur nach einer eingebauten Verzögerung oder innerhalb gewählter Zeitfenster erzeugen.
Warum das für zukünftige lebende Materialien wichtig ist
Vereinfacht gesagt verwandelt diese Arbeit DNA in ein intelligentes mechanisches Schloss, das sich nur für bestimmte Zellen, nur bei bestimmten Kräften und nur zu gewählten Zeiten öffnet. Indem sie zeigen, dass weniger offensichtliche Rezeptoren wie Nucleolin und PTK7 mechanische Informationen über sehr unterschiedliche Wege innerhalb der Zelle übertragen können, erweitern sie unser Bild davon, wie Zellen ihre Umgebung "fühlen". Weil das gesamte System aus Nukleinsäuren aufgebaut ist, lässt es sich direkt in das schnell wachsende Arsenal von DNA‑Schaltkreisen und Nanogeräten einbinden. Das schafft eine Grundlage für Materialien und gentechnisch erzeugte Gewebe, die nicht nur erkennen, wann Zellen drücken oder ziehen, sondern auch mit zeitlich abgestimmten biochemischen Aktionen reagieren—möglicherweise um Heilung, Wachstum oder Krebstherapie auf äußerst programmierbare Weise zu steuern.
Zitation: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
Schlüsselwörter: Mechanotransduktion, DNA-Aptamere, Zellmechanik, Synthetische Biologie, DNA-Reaktionsnetzwerke