Clear Sky Science · de
Ein myoneuraler Aktuator mit entworfener Biophysik für implantierbare biohybride Systeme
Muskeln neu bauen als intelligente lebende Maschinen
Stellen Sie sich vor, Ärztinnen und Ärzte könnten den eigenen Muskel eines Menschen in einen lebenden Motor verwandeln, der nie müde wird, sich von einem Computer steuern lässt und jahrelang sicher neben empfindlichen Organen liegen kann. Diese Studie beschreibt genau einen solchen Ansatz. Die Forschenden entwickeln in Ratten einen „myoneuralen Aktuator“ – einen Muskel, dessen Nervenanbindung gezielt umgebaut wird, sodass er elektronisch angesteuert werden kann, gegen Ermüdung resistent ist und zugleich wie natürliches Gewebe funktioniert. Solche lebenden Aktuatoren könnten eines Tages Bewegung wiederherstellen, geschädigte Organe stützen oder realistische Empfindungen von fortschrittlichen Prothesen liefern.
Warum lebende Muskeln bessere Motoren sind
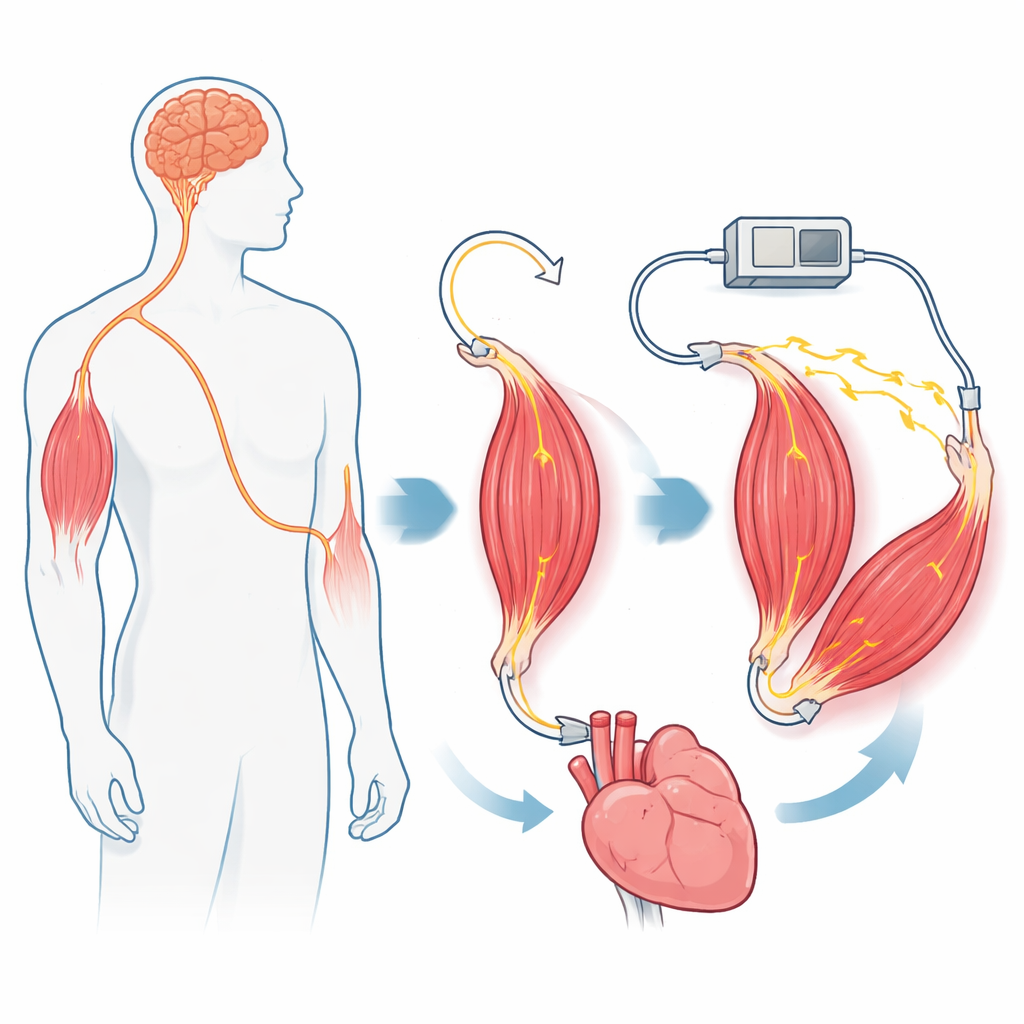
Künstliche Motoren, die mit Strom, Luft oder Flüssigkeiten betrieben werden, sind leistungsstark, aber sie sind schwer, schwierig auf körperfreundliche Größen zu verkleinern und bestehen aus Materialien, die sich schlecht mit lebendem Gewebe vertragen. Im Gegensatz dazu ist Skelettmuskel leicht, energieeffizient, selbstreparierend und bereits dafür ausgelegt, im Körper zu funktionieren. Er kann wachsen, sich anpassen und auf winzige Nervensignale reagieren. Wenn Muskeln jedoch direkt von einem implantierten Gerät mit elektrischen Impulsen gesteuert werden, ermüden sie schnell. Diese Ermüdung entsteht, weil die Standard-Elektrostimulation die größten, schnellsten, aber am wenigsten ausdauernden Fasern zuerst rekrutiert. Um Muskel als verlässlichen, implantierbaren Motor nutzbar zu machen, musste das Team die Organisation und Rekrutierung der Nervenfasern ändern – ohne die natürliche Gesundheit und Nachhaltigkeit des Muskels aufzugeben.
Nervenwege tauschen, um die Steuerung neu zu schreiben
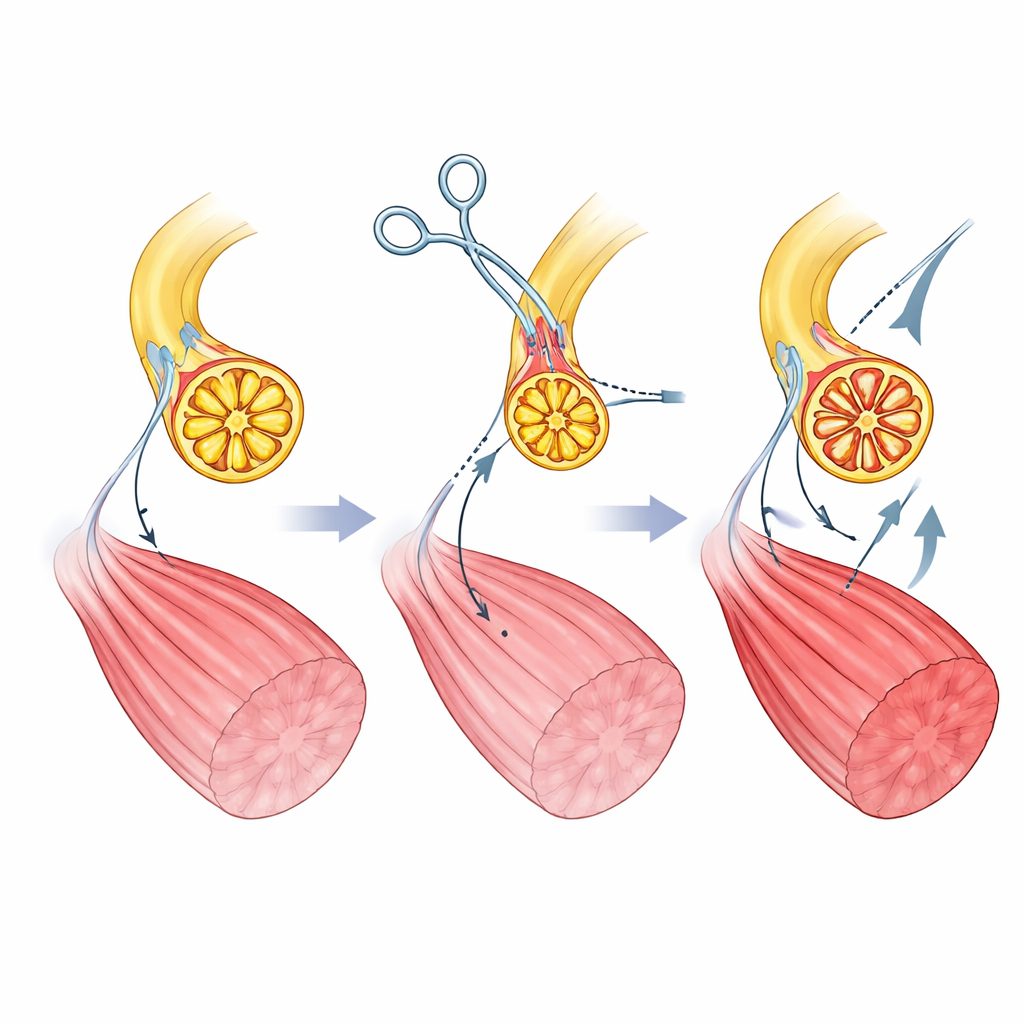
Die Autoren erzeugen ihren myoneuralen Aktuator in Ratten, indem sie chirurgisch einen Beinmuskel umverdrahten. Zunächst durchtrennen sie den normalen motorischen Nerv, der Befehle aus dem Rückenmark überträgt, und verhindern dessen Wiederanwachsen. Dann leiten sie einen anderen Nerv – einen, der normalerweise Berührungs- und Dehnreize von Haut und Gewebe überträgt – direkt in den Muskel. Im Laufe der Zeit regeneriert dieser „sensorische“ Nerv im Muskel und bildet neue Kontaktstellen mit den Muskelfasern. Die Mikroskopie zeigt, dass diese neuen Verbindungsstellen optisch und funktional wie normale motorische Synapsen wirken, und der Muskel gewinnt seine Fähigkeit zur Kontraktion zurück, wenn der sensorische Nerv elektrisch stimuliert wird. Wichtig ist, dass die Axone in diesem sensorischen Nerv gleichmäßiger und kleiner sind als die des ursprünglichen motorischen Nervs, was die Grundlage für eine ausgewogenere Rekrutierung der Muskelfasern unter computerbasierter Steuerung schafft.
Muskeln, die weitermachen, wenn sie stark belastet werden
Nachdem die umverdrahteten Muskeln verheilt waren, unterzog das Team sie anspruchsvollen Testreihen. Sie verglichen native Muskeln mit den neuen Aktuatoren bei wiederholten Einzelzuckungen und längeren Phasen kontinuierlicher Kontraktion. Die myoneuralen Aktuatoren verloren ihre Kraft deutlich langsamer und zeigten über die Zeit eine stabilere Leistung – mit einer um 260 Prozent verbesserten Ermüdungsresistenz bei kontinuierlicher Arbeit. Ihr Verhalten über Minuten hinweg unterschied sich grundlegend von unveränderten Muskeln: Anstatt eines schnellen Kraftabfalls nahm die Kraft gradueller ab und stabilisierte sich dann. Trotz eines gewissen Massenverlusts während des Umbaus behielten die Aktuatoren gesunde Faserstrukturen bei und erzeugten pro Masseneinheit ähnliche Kräfte wie native Muskeln; zudem hielten sie ihren Zustand mindestens 15 Wochen lang ohne Training oder zusätzliche Stimulation aufrecht.
Computersteuerung ohne Störung des Gehirns
Da die neue Nervenverdrahtung den Muskel von den normalen motorischen Signalen des Gehirns trennt, stammen alle Kontraktionen nun von einem externen Stimulator. Die Forschenden binden den Muskel in eine Rückkopplungsschleife ein: Ein Sensor misst die Kraft, ein Regler passt die Nervenstimulation an, und das System verfolgt über viele Zyklen einen vorgegebenen Zielwert. Native Muskeln versagen in diesem Aufbau schnell, aber die myoneuralen Aktuatoren folgen weiterhin den Kommandos. Um das System sicherer und flexibler zu machen, führen die Autoren außerdem eine reversible „Nervenblockade“ ein. Durch Anlegen eines hochfrequenten elektrischen Signals am Nerv näher am Rückenmark verhindern sie, dass Stimulationsimpulse unerwünschte Signale zurück in das zentrale Nervensystem senden, während die Muskelseite weiterhin reagiert. In Tests erzeugte der Aktuator kontrollierte Kräfte, während das Gehirn effektiv von der künstlichen Stimulation abgeschirmt blieb.
Von bionischen Gliedmaßen bis zur Unterstützung versagender Organe
Um zu demonstrieren, wie dieser lebende Motor eingesetzt werden könnte, bauen die Autoren zwei Demonstrationssysteme in Ratten. Im ersten koppeln sie den Aktuator in Reihe mit einem anderen Muskel, der den verbleibenden Muskel an einer Amputationsstelle simuliert. Durch Anspannen oder Entspannen dieses Paares verändern sie die Dehnung des Residualmuskels und damit die Aktivität seiner sensorischen Nervenfasern – im Grunde stellen sie so das Lage- und Kraftgefühl der Extremität höher oder niedriger ein. Diese „propriozeptive mechanoneurale Schnittstelle“ könnte schließlich natürlich wirkendes Feedback von Robotik-Prothesen oder virtuellen Avataren liefern. Im zweiten System legen sie den Aktuator um eine Schleife des Dünndarms, die mit Flüssigkeit gefüllt ist. Bei Nervenstimulation presst der Muskel das Darmsegment zusammen und lässt es wieder los; Bewegungsverfolgung zeigt, dass das Organ synchron mit dem Aktuator bewegt wird. Das deutet auf künftige Geräte hin, die geschwächten Organen wie Darm, Blase oder sogar Herz mechanische Unterstützung geben könnten.
Was das für die Medizin von morgen bedeuten könnte
Insgesamt zeigt diese Arbeit, dass durch sorgfältiges Umlenken von Nerven der eigene Muskel eines Menschen in einen ermüdungsresistenten, computergetriebenen Aktuator verwandelt werden kann, der sich weiterhin wie nativeres Gewebe verhält und bei Bedarf elektrisch vom Gehirn isoliert werden kann. Da der Ansatz auf chirurgischen Techniken und Elektroden beruht, die bereits bestehenden klinischen Werkzeugen ähneln, könnte er leichter übertragbar sein als vollständig synthetische Implantate oder im Labor gezüchtetes Gewebe. Wenn ähnliche myoneurale Aktuatoren sicher beim Menschen gebaut und gesteuert werden können, könnten sie den Kern neuer biohybrider Systeme bilden, die Sensibilität in Gliedmaßen wiederherstellen, versagende Organe unterstützen und präzise mechanische Signale an den Körper liefern – ohne die Masse und Steifigkeit traditioneller Maschinen.
Zitation: Song, H., Herrera-Arcos, G., Friedman, G.N. et al. A myoneural actuator with engineered biophysics for implantable biohybrid systems. Nat Commun 17, 2584 (2026). https://doi.org/10.1038/s41467-026-70626-6
Schlüsselwörter: biohybrider Aktuator, Neuroprothetik, Muskelermüdung, Nervregeneration, Organunterstützung