Clear Sky Science · de
Eine metrologische Grundlage für absolute Transkriptomik mithilfe an das Internationale Einheitensystem (SI) angekoppelter Kalibrierstandards
Warum es wichtig ist, RNA-Signale in reale Zahlen zu überführen
Moderne Gentests können ablesen, welche Gene in unseren Zellen an- oder abgeschaltet sind, doch sie scheitern an einer grundlegenden Frage: Wie viele Moleküle sind tatsächlich vorhanden? Die heutigen RNA-Sequenziermethoden vergleichen meist relative Veränderungen zwischen Proben, statt verlässliche, absolute Zählungen zu liefern. Das ist problematisch, wenn man universelle Krankheitsgrenzwerte festlegen, Ergebnisse zwischen Kliniken vergleichen oder präzise Modelle zellulärer Vorgänge erstellen möchte. Diese Studie stellt einen neuen Ansatz vor, RNA-Sequenzierung an dieselben internationalen Einheiten der Chemie und Physik zu koppeln und so unscharfe relative Signale in absolute, vergleichbare Zahlen zu verwandeln.
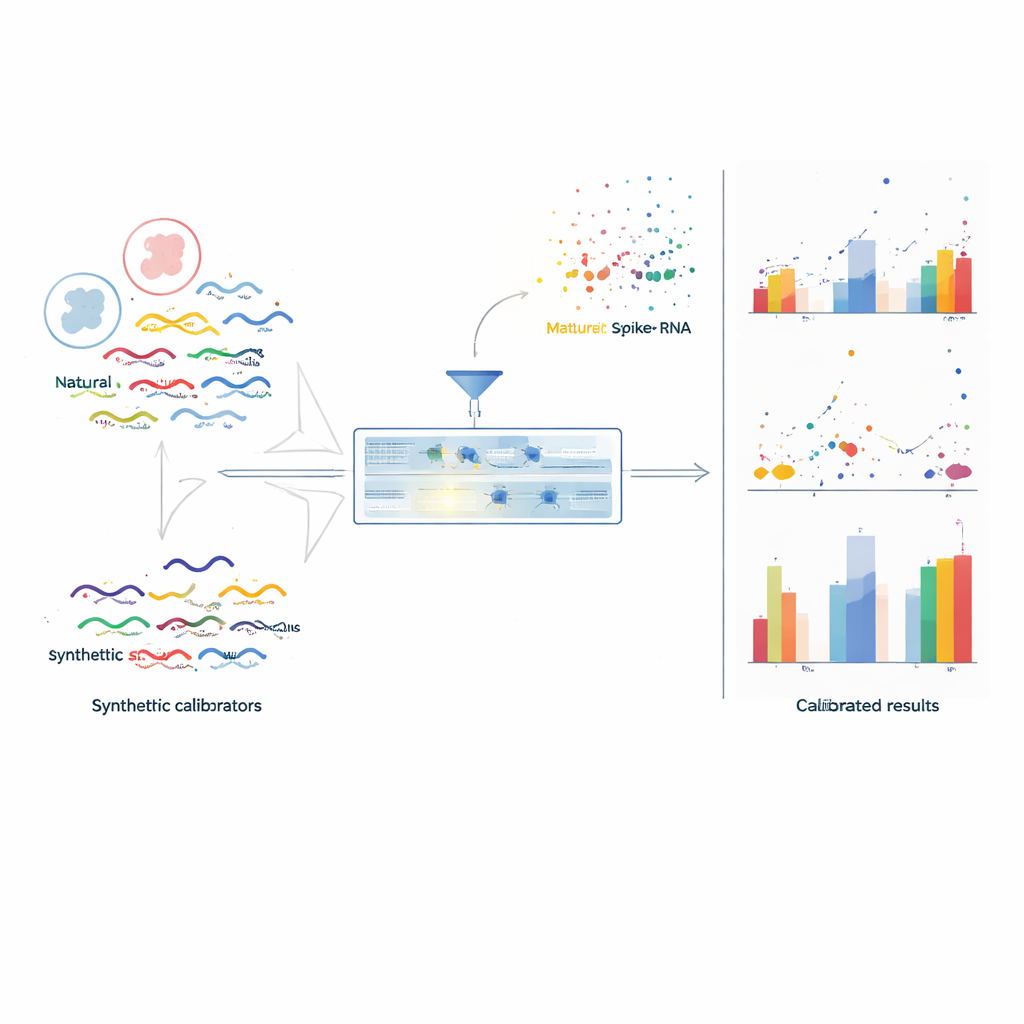
Das Problem beim Vergleich von Genaktivität
Bei der RNA-Sequenzierung werden RNA-Moleküle in Fragmente zerlegt und gezählt, wie oft jedes Gen vertreten ist. Dabei schleichen sich zwei Arten von Verzerrungen ein. Erstens führen systematische Unterschiede zwischen Experimenten – etwa verschiedene Labore, Geräte oder Probenvorbereitungen – zu sogenannten Batch-Effekten, die dieselbe Probe bei wiederholter Messung unterschiedlich erscheinen lassen. Zweitens bewirken sequencing-abhängige Effekte, dass Gene mit bestimmten Längen oder Basenzusammensetzungen eher oder seltener erfasst werden; innerhalb einer Probe werden manche Gene also systematisch über- und andere unterbewertet. Folglich sind Wissenschaftler weitgehend gezwungen, über Faltungsänderungen zwischen Bedingungen zu sprechen statt über wahre Molekülzahlen, und diese Faltungsänderungen können von Charge zu Charge irreführend sein.
Ein neuer Satz Messlatten für RNA-Messungen
Um das zu beheben, entwickelten die Autoren TranScale, ein Panel von 100 synthetischen RNA-Molekülen, die sich wie echte menschliche Transkripte verhalten, gleichzeitig aber rechnerisch unterscheidbar bleiben. Diese Standards decken ein breites Spektrum an Längen, Sequenzeigenschaften und klinisch relevanten Varianten wie Spleißformen und Genfusionen ab und spiegeln damit die Vielfalt zellulärer RNA gut wider. Entscheidend ist, dass jedem TranScale-Molekül eine exakte Konzentration zugewiesen wird, bestimmt durch eine primäre Messtechnik namens Isotopenverdünnungs-Massenspektrometrie, die auf das Internationale Einheitensystem (SI) rückführbar ist. Durch das Mischen einer bekannten, sehr kleinen Menge TranScale in jede RNA-Probe vor dem Sequenzieren erhält das Experiment ein internes Messlineal, das dieselben Laborprozesse und Verzerrungen wie die natürlichen RNAs durchläuft.
Rauschhafte Reads in absolute Zählungen umwandeln
Mit TranScale in jeder Bibliothek kann das Team die Anzahl der Sequenzier-Reads für jedes Spike-in-Molekül mit seiner zertifizierten Konzentration vergleichen. Für jede Charge wählen sie gut funktionierende Spike-ins aus und passen eine lineare Kalibrierkurve an, die Read-basierte Einheiten mit echten Molekülzahlen verknüpft. Dieses einfache Modell erfasst gleichzeitig sowohl chargenweite als auch sequenzbezogene Verzerrungen. Dieselbe Kurve wird dann auf alle Gene der Probe angewandt und wandelt deren relative Reads in absolute Kopienzahlen pro Einheit RNA um. In einer großen Multi-Labor- und Multi-Plattform-Studie, die bewusst starke Batch-Effekte erzeugen sollte, senkte diese Kalibrierung die mittlere Variation absoluter Messwerte zwischen Zentren von über 85 % auf unter 15–25 % und stellte die korrekte Gruppierung biologischer Proben wieder her, die durch technischen Lärm verschleiert war.
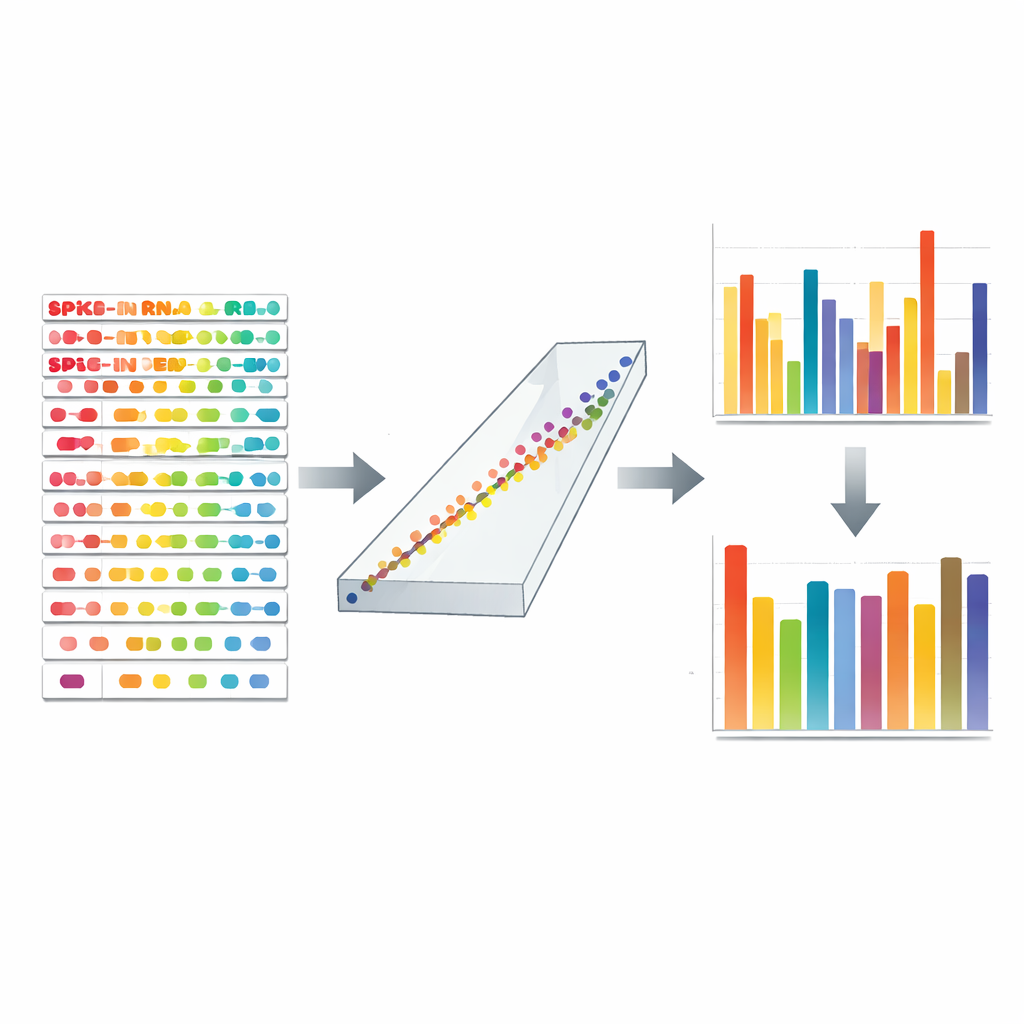
Verborgene Fehler erkennen und beheben
Die TranScale-Standards dienen auch als diagnostische Sonden zur Qualitätskontrolle der Daten. Durch den Vergleich gemessener Werte mit ihren zertifizierten Wahrheiten trennten die Autoren zwei Fehlerarten: wie stark der absolute Level jedes Gens abweicht und wie stark die Verhältnisse zwischen Bedingungen falsch sind. Sie fanden überraschende Fälle, in denen relative Unterschiede konsistent wirkten, aber absolute Zahlen stark verzerrt waren, und umgekehrt. Das bedeutet, dass konventionelle Prüfungen, die nur Faltungsänderungen betrachten, schwerwiegende Probleme übersehen können. Nach der Kalibrierung stimmten sowohl absolute Level als auch Verhältnisse von Spike-ins und Tausenden echten menschlichen Genen eng mit unabhängigen digitalen PCR-Messungen und einem externen Referenzdatensatz überein. Die korrigierten Daten offenbarten eine deutlich klarere quantitative Landschaft, sodass es möglich wurde, Haushaltsgene mit krebsrelevanten Treibern auf derselben absoluten Skala zu vergleichen und DNA-Veränderungen, etwa ko-amplifizierte Krebsgene, direkt mit ihren RNA-Ausgängen zu verknüpfen.
Von relativen Trends zu klinischen Schwellenwerten
Abschließend zeigten die Forscher, wie absolute Skalierung medizinische Entscheidungen schärfen kann. Mittels eines häufig in Brustkrebs gemessenen Onkogens definierten sie eine feste Schwelle basierend auf digitaler PCR und prüften, ob RNA-Sequenzierung Proben über viele Chargen hinweg zuverlässig als normal oder Tumor klassifizieren kann. Unkorrigierte Daten lieferten wegen Batch-Effekten inkonsistente Ergebnisse. Nach TranScale-Kalibrierung stimmte jede Bibliothek mit der korrekten Klassifikation überein. Indem die RNA-Sequenzierung durch biomimetische Standards an SI-Einheiten gekoppelt wird, legt diese Arbeit eine metrologische Grundlage für die Transkriptomik. Sie öffnet die Tür zu universellen diagnostischen Grenzwerten, robustem Datenaustausch zwischen Standorten und präziseren, systemweiten Modellen der Genexpression in Gesundheit und Krankheit.
Zitation: Zhang, Y., Yang, B., Yu, Y. et al. A metrological foundation for absolute transcriptomics using International System of Units-anchored calibrators. Nat Commun 17, 2747 (2026). https://doi.org/10.1038/s41467-026-70582-1
Schlüsselwörter: RNA-Sequenzierung, absolute Quantifizierung, Metrologie, Kalibrierung der Genexpression, biomolekulare Standards