Clear Sky Science · de
Strukturelle Übergänge beim schrittweisen Zusammenbau von Proteasom-Kernpartikeln
Wie Zellen den molekularen Müll entsorgen
In jeder unserer Zellen müssen verbrauchte und beschädigte Proteine abgebaut werden, bevor sie sich wie Müll anhäufen. Eine riesige molekulare Maschine, das Proteasom, übernimmt einen Großteil dieser Aufräumarbeit und ist bereits Ziel von Krebsmedikamenten. Diese Studie wirft einen Blick hinter die Kulissen, wie der katalytische Kern des Proteasoms in Hefezellen Schritt für Schritt aufgebaut wird, und enthüllt unerwartete Abkürzungen und Sicherheitsmechanismen, die sicherstellen, dass die fertige Maschine präzise arbeitet und erst dann aktiv wird, wenn sie bereit ist.
Aufbau eines proteinzerreißenden Fasses
Das aktive Zentrum des Proteasoms ist ein fassförmiger Kern, bestehend aus übereinandergestapelten Ringen von Proteinuntereinheiten. In diesem Fass sitzen die versteckten Schnittstellen, die andere Proteine in kleine Stücke zerlegen. Da es gefährlich wäre, diese Cutter zu früh zu aktivieren, baut die Zelle das Fass in einer Reihe partiell zusammengesetzter Zwischenformen auf. Die Autoren konzentrierten sich auf frühe Versionen des Kerns, sogenannte Vorläuferkomplexe, die meist selten und kurzlebig sind. Indem sie einen der letzten Assemblierungsschritte leicht verlangsamten, konnten sie diese frühen Formen aus Hefe einfangen und reinigen und sie mittels hochauflösender Kryo-Elektronenmikroskopie abbilden, die Moleküle in Aktion einfriert und ihre dreidimensionalen Formen zeigt.
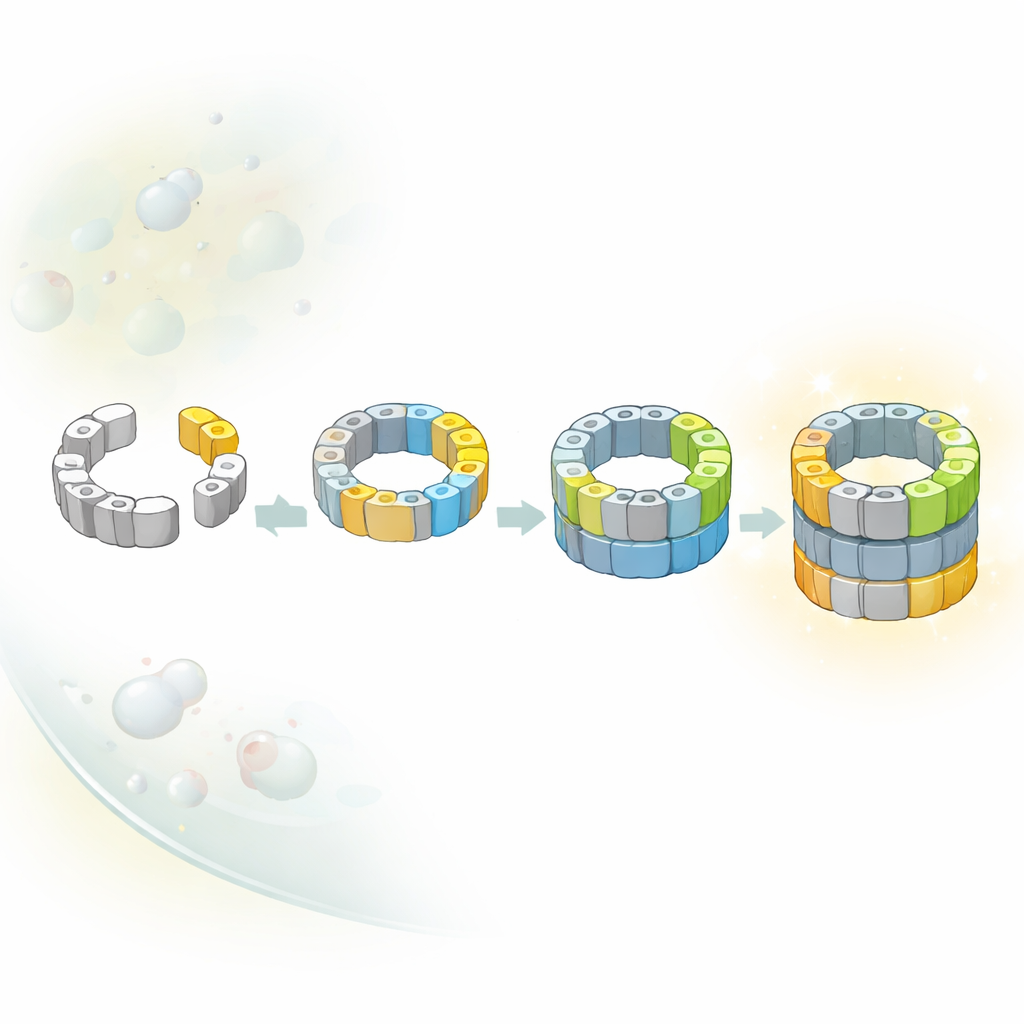
Mehrere Wege zum selben Kern
Klassische Lehrbuchdiagramme legen oft nahe, dass komplexe Maschinen in Zellen entlang einer einzigen, festen Route aufgebaut werden. Die Forscher zeigten jedoch, dass dies für den Proteasomkern nicht zutrifft. Sie identifizierten mehrere unterschiedliche Zwischenformen, die sich darin unterscheiden, welche katalytischen Untereinheiten dem halb fertigen Fass bereits beigetreten sind. Durch die Kombination struktureller Momentaufnahmen mit genetischen Tricks, mit denen einzelne Untereinheiten an- und abgeschaltet werden können, zeigten sie, dass mindestens zwei alternative Wege von einem frühen Halbfass zu einem nahezu vollständigen Kern führen. Auf einem Weg trifft eine bestimmte Untereinheit namens β5 zuerst ein; auf einem anderen kann eine andere Untereinheit, β1, früher eingebaut werden. Das Gleichgewicht zwischen diesen Routen hängt wahrscheinlich davon ab, welche Bausteine in der dicht gepackten Umgebung der Zelle am verfügbarsten sind.
Von losen Teilen zu einer verriegelten Schnittkammer
Die Strukturen zeigen außerdem, wie die Schnittstellen des Proteasoms während der Assemblierung sorgfältig vorbereitet werden. In frühen Zwischenformen sind wichtige Schleifenregionen um die verborgenen Schnittreste herum flexibel und wenig geordnet, und die katalytischen Zentren werden noch von kurzen „Propeptid“-Segmenten blockiert. Wenn zusätzliche Untereinheiten rund um den Ring einrasten, nehmen diese Schleifen allmählich definiertere Formen an, die entscheidende Aminosäuren für die Selbstaktivierung ausrichten. Erst wenn zwei Halbfässer schließlich zusammenkommen und das Doppelring-Fass vervollständigen, verriegeln sich diese Schleifen vollständig in der aktiven Anordnung und lösen die Entfernung der blockierenden Segmente aus. Diese Kopplung von Geometrie und Chemie stellt sicher, dass die potente Schnittaktivität nur innerhalb einer verschlossenen Kammer erscheint und den Rest der Zelle schützt.
Chaperone helfen, führen und lassen dann los
Auf dem Weg dorthin begleiten spezialisierte Helferproteine, sogenannte Chaperone, das assemblierende Fass und verhindern falsche Kombinationen. Ein Chaperon, Ump1, ist anfangs weitgehend ungeordnet, faltet sich aber schrittweise, während mehr Untereinheiten es umgeben; schließlich wird es in der zentralen Höhlung eingeschlossen und nach Aktivierung des Fasses zerstört. Ein anderes Chaperonpaar, Pba1–Pba2, greift die Außenseite des Rings auf zwei clevere Arten. Eine flexible Schleife von Pba1 klemmt sich wie ein Abstandshalter zwischen zwei Außenring-Untereinheiten und hält sie leicht auseinander, wodurch ein vorzeitiges Schließen verhindert wird. Gleichzeitig hilft das Schwanzende einer Außenring-Untereinheit (α1), benachbarte Segmente so zu positionieren, dass die Chaperone in der Endphase freigesetzt werden können und der Ring sich richtig schließt. Als die Forscher das α1-Schwanzende entfernten, blieb das Fass in einem späten, fast fertigen Zustand stecken, der hartnäckig seine Chaperone behielt, was bestätigt, dass diese kleine Region als Teil eines Freigabeschalters fungiert.
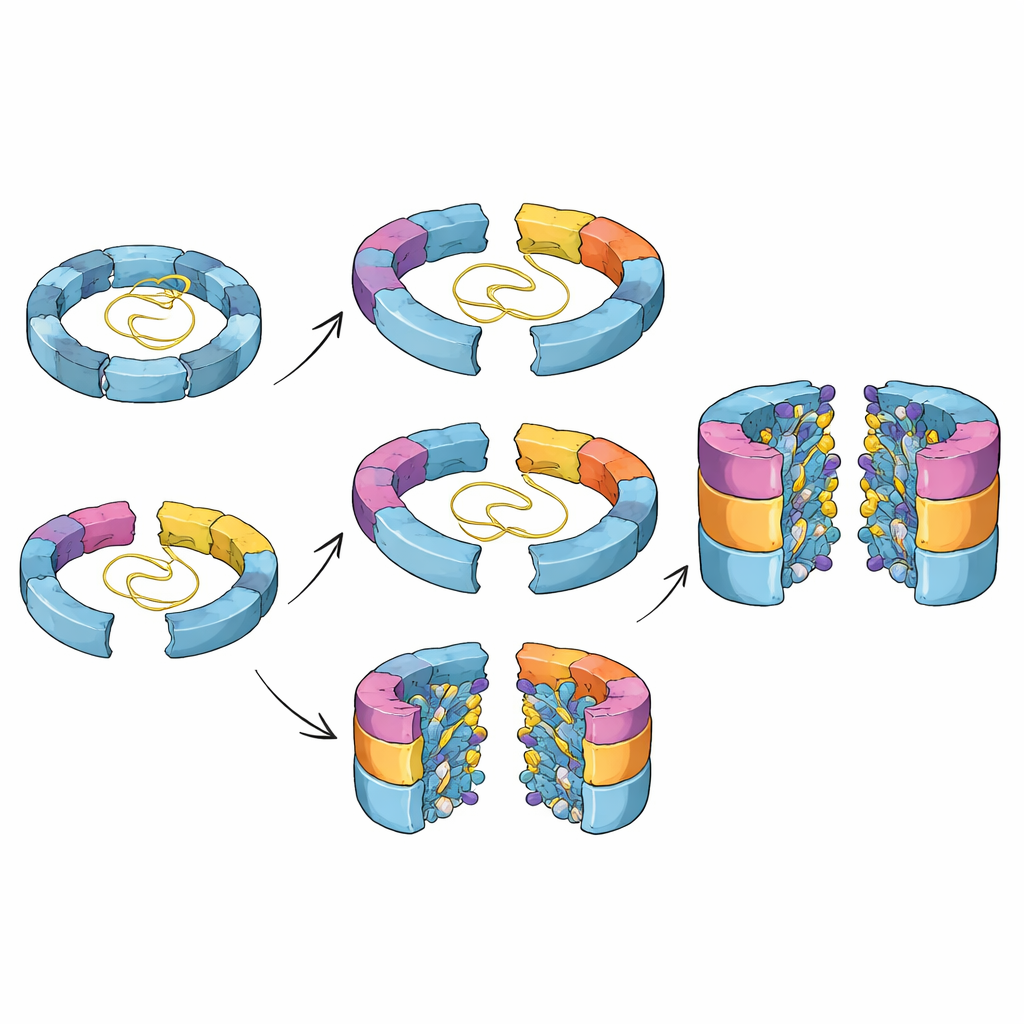
Warum diese verborgenen Schritte wichtig sind
Zusammen zeichnen diese Befunde ein detailliertes Bild davon, wie Zellen den Zusammenbau eines gefährlichen, aber lebenswichtigen Proteinzerlegers choreografieren. Die Arbeit zeigt, dass der Proteasomkern auf mehr als einem Weg gebaut werden kann, dass seine aktiven Zentren schrittweise herausgebildet werden und dass Helferproteine nicht nur frühe Zwischenformen stabilisieren, sondern auch in einen Zeitsteuerkreis eingebunden sind, der sicherstellt, dass sie genau im richtigen Moment abgehen. Das Verständnis dieser verborgenen Schritte hilft zu erklären, wie kleine genetische Veränderungen in Assemblierungsfaktoren zu Krankheiten beitragen können, und könnte die Entwicklung von Medikamenten unterstützen, die die Proteasomaktivität bei Krebs, Immunstörungen oder Neurodegeneration durch Eingreifen in seinen Aufbau statt in seine Endform feinjustieren.
Zitation: Mark, E., Ramos, P.C., Nunes, M.M. et al. Structural transitions in the stepwise assembly of proteasome core particles. Nat Commun 17, 2582 (2026). https://doi.org/10.1038/s41467-026-70525-w
Schlüsselwörter: Zusammenbau des Proteasoms, Proteinabbau, molekulare Chaperone, Cryo-Elektronenmikroskopie, zelluläre Qualitätskontrolle