Clear Sky Science · de
Transiente molekulare Chimäre zur Nutzung xenogener Organellen
Geliehene Solarpaneele in einer einzigen Zelle
Wir denken bei solarbetriebener Lebensweise meist an Pflanzen und Algen, doch einige einzellige Räuber nehmen eine Abkürzung: Sie stehlen die „Solarpaneele“ – Chloroplasten – von ihrer Beute. Diese Studie untersucht, wie ein solches Mikroorganismus, Rapaza viridis, diese gestohlenen Teile über Wochen funktionsfähig hält, obwohl sie von einer völlig anderen Art stammen. Indem untersucht wird, wie die Proteine des Wirts in diese fremden Chloroplasten eindringen und sie unterstützen, wirft die Arbeit ein Licht darauf, wie komplexe Zellbestandteile wie Chloroplasten möglicherweise einst entstanden sind.
Wie ein Mikroben Räuber grüne Energie stiehlt und nutzt
Rapaza viridis ist ein winziger Geißeltierchen, das eine bestimmte Grünalge namens Tetraselmis frisst. Anstatt alles zu verdauen, behält Rapaza die aufgenommenen Chloroplasten, nun „Kleptoplasten“ genannt, und wirft den Rest der Algenzelle weg, einschließlich ihres Zellkerns. Diese Kleptoplasten werden in Stücke geschnitten und an Tochterzellen weitergegeben. Etwa zwei Wochen lang kann der Wirt nahezu vollständig von der Energie und dem Kohlenstoff leben, die diese geliehenen Chloroplasten erzeugen, obwohl diese keine Anweisungen oder Ersatzteile mehr aus dem ursprünglichen Algen-Genom erhalten. Dieser ungewöhnliche Lebensstil bietet ein lebendes Fenster darauf, wie frühe Schritte hin zu permanenten Chloroplasten ausgesehen haben könnten.
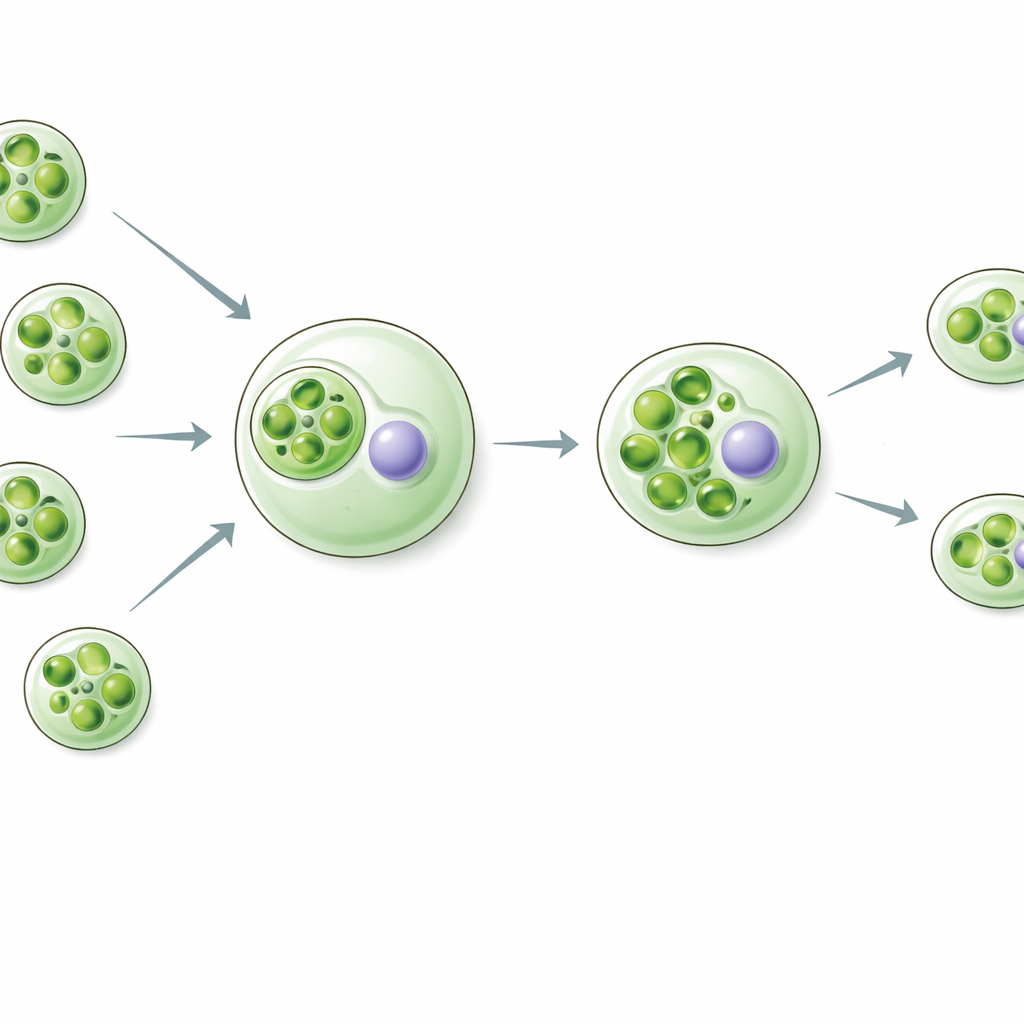
Wirtgene greifen ein, um gestohlene Teile am Leben zu erhalten
Die Forschenden stellten eine entscheidende Frage: Wenn der Algenkern fehlt, wer liefert die Proteine, die nötig sind, damit der Kleptoplast funktioniert? Durch Analyse der Genaktivität über die Zeit in Rapaza identifizierten sie 37 Wirtsgene, deren Produkte so aussehen, als würden sie im Chloroplasten arbeiten. Viele dieser Gene ähneln Komponenten der photosynthetischen Maschinerie – Lichtfangproteine, Bestandteile des Elektronentransports und Enzyme zur Kohlenstofffixierung. Zwei fielen besonders auf: ein RuBisCO-Kleinuntereinheits-ähnliches Protein (RvRbcS-like) und ein RuBisCO-Aktivase-ähnliches Protein (RvRca-like). Beide sind mit wichtigen Helfern von RuBisCO verwandt, dem zentralen Enzym zur Aufnahme von Kohlendioxid. Diese Wirtsgene schalten sich stark an, nachdem die Beute gefressen wurde, genau dann, wenn die Kleptoplasten umgestaltet und für eine langfristige Nutzung vorbereitet werden.
Nachweis, dass Wirtsproteine in die Kleptoplasten gelangen
Hinweise in Sequenzen allein reichen nicht; die Proteine müssen tatsächlich ins Innere der Kleptoplasten gelangen. Mit maßgeschneiderten Antikörpern und fluoreszenzmikroskopischen Methoden verfolgte das Team, wo RvRbcS-like und RvRca-like akkumulieren. Sie konstruierten Rapaza-Stämme mit winzigen nachweisbaren Tags an RvRbcS-like und zeigten, dass das Signal mit den Kleptoplasten und mit RuBisCO selbst überlappt. Ähnliche Bildgebung mit einem Antikörper gegen RvRca-like zeigte, dass dieses Protein ebenfalls in den Kleptoplasten konzentriert ist. Auf Protein-Gelen erschienen beide Proteine verkürzt, was mit dem Entfernen eines speziellen N-terminalen Segments beim Durchqueren von Membranen übereinstimmt – ähnlich den Zielsignalen, die Proteine in gewöhnliche Chloroplasten leiten.
Warum diese geliehenen Helfer wichtig sind
Um zu testen, ob diese Wirtsproteine wirklich bedeutsam sind, setzten die Autoren CRISPR-basierte Genomeditierung ein, um jedes Gen auszuschalten. Zellen ohne RvRbcS-like wuchsen schlecht, verloren an photosynthetischer Leistungsfähigkeit, bildeten deutlich weniger energiereiche Speichergranula und starben deutlich früher als normal. Die Pegel der algalen RuBisCO-Großuntereinheit sanken ebenfalls, was darauf hindeutet, dass ohne die vom Wirt gelieferte Ersatz-Kleinuntereinheit der Enzymkomplex zerfällt. Das Entfernen von RvRca-like hatte einen milderen, aber dennoch klaren Effekt: Das frühe Wachstum blieb nahe dem Normalzustand, später gingen aber Photosynthese und Kohlenstoffspeicherung zurück, was einen schrittweisen Effizienzverlust offenbart. Zusammen zeigen diese Ergebnisse, dass Rapaza gestohlene Chloroplasten nicht einfach nur parkt; es erhält und remodeliert sie aktiv mit seinem eigenen Proteininventar.
Maßgeschneiderte Liefersignale und rekonstruierte innere Strukturen
Die meisten der mutmaßlich an Kleptoplasten gerichteten Proteine in Rapaza besitzen lange, wenig strukturierte „Köpfe“ an ihrem N‑Ende, oft mit vorhergesagten membranüberspannenden Segmenten. Durch das Verschmelzen eines dieser Köpfe an ein Luciferase-Reportergen zeigten die Autoren, dass dieses Segment allein ausreicht, um ein Frachtprotein in Kleptoplasten zu transportieren. Detaillierte Sequenzanalysen enthüllten mehrere Klassen dieser Targeting-Regionen, die stark denen ähneln, die von einer verwandten Algengruppe verwendet werden, um Proteine in ihre permanenten, dreifach membranumhüllten Chloroplasten zu importieren. Ein besonders auffälliges Wirtsprotein, RvRbcS-like, trägt vier RuBisCO-ähnliche Domänen und einen flexiblen Schwanz, reich an sich wiederholenden Motiven, von denen angenommen wird, dass sie die Phasentrennung von Proteinen fördern. Die Autoren schlagen vor, dass dieser Schwanz hilft, das Pyrenoid – das dichte Kohlenstofffixierungszentrum im Kleptoplasten – in mehrere Tropfen umzubauen, die an Tochterzellen vererbt werden können.
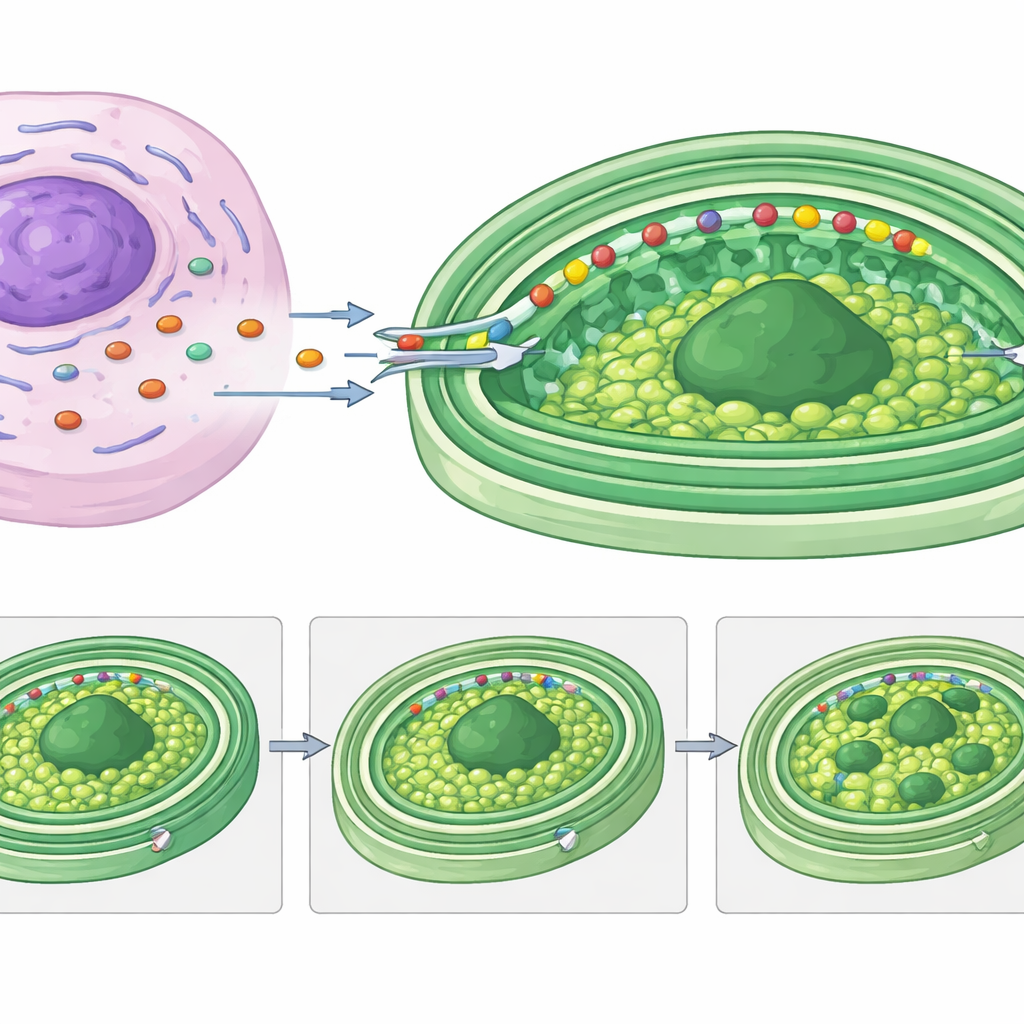
Was das für die Entstehung komplexer Zellen bedeutet
Für Nichtfachleute lautet die Kernbotschaft: Rapaza viridis zeigt eine lebende, reversible Version dessen, was geschehen sein könnte, als urzeitliche Zellen freie Bakterien in permanente Zellbestandteile wie Chloroplasten verwandelten. Hier baut der Wirt rasch eine temporäre molekulare Partnerschaft auf: Eigene Gene liefern entscheidende Ersatzteile und formen sogar die innere Struktur der gestohlenen Chloroplasten um, alles gesteuert von spezialisierten Liefersignalen. Diese „transiente molekulare Chimärie“ demonstriert, dass selbst kurzlebige Integrationen zwischen Arten anspruchsvoll und fein abgestimmt sein können. Die Untersuchung dieses Systems liefert Wissenschaftlern ein kraftvolles Modell, um aufzudecken, wie komplexe Zellen gelernt haben, fremde Energieanlagen zu kontrollieren, zu ernähren und sicher zu nutzen – und wie über evolutionäre Zeit hinweg weiterhin neue Organellen entstehen könnten.
Zitation: Kashiyama, Y., Maruyama, M., Nakazawa, M. et al. Transient molecular chimerism for exploiting xenogeneic organelles. Nat Commun 17, 2371 (2026). https://doi.org/10.1038/s41467-026-70516-x
Schlüsselwörter: Kleptoplastie, Chloroplast-Evolution, Rapaza viridis, Endosymbiose, Organellenbiogenese