Clear Sky Science · de
Labelfreie Massen- und Größenermittlung von Biomolekülen im Bereich weniger kDa mittels hierarchischem Vision-Transformer-unterstützter nanofluidischer Streumikroskopie
Die kleinsten Moleküle sichtbar machen
Viele der wichtigsten Botenstoffe im Körper – etwa Hormone und Immunmediatoren – sind so winzig, dass sie für leistungsfähige Mikroskope kaum sichtbar sind, sofern sie nicht mit fluoreszierenden Markern versehen werden. Solche Marker können das Verhalten der Moleküle verändern, was für die Wirkstoffentwicklung und die Grundlagenforschung ein erhebliches Problem darstellt. Diese Studie stellt eine Methode vor, mit der sich einzelne Moleküle so klein wie Insulin ohne jegliche Markierung wiegen und vermessen lassen, indem nanofluidische Chips mit moderner Künstlicher Intelligenz kombiniert werden. Sie eröffnet einen Weg, um wichtige Biomoleküle in ihrem natürlichen Zustand einzeln zu beobachten.
Kleine Kanäle als Reagenzgläser
Im Zentrum der Methode steht die nanofluidische Streumikroskopie, die einen nagelgroßen Chip mit extrem schmalen Kanälen nutzt. Diese Kanäle sind nur einige Dutzend Nanometer breit – tausendfach dünner als ein menschliches Haar. In ihnen treiben gelöste Moleküle frei durch den Kanal und haften nicht an einer Oberfläche. Wird der Chip mit sichtbarem Licht beleuchtet, streuen sowohl die Kanalwände als auch durchgehende Moleküle Licht. Weil der Kanal deutlich größer ist als das Molekül, interferieren die gestreuten Felder so, dass das optische Signal des Moleküls stark verstärkt wird. Durch Subtraktion von Bildern eines leeren Kanals von Bildern, die ein vorbeiziehendes Molekül zeigen, erhalten die Forscher eine filmartige Aufzeichnung (einen Kymographen) seines Durchgangs durch den Kanal, die Informationen über seine Masse und seine Diffusionsgeschwindigkeit enthält.
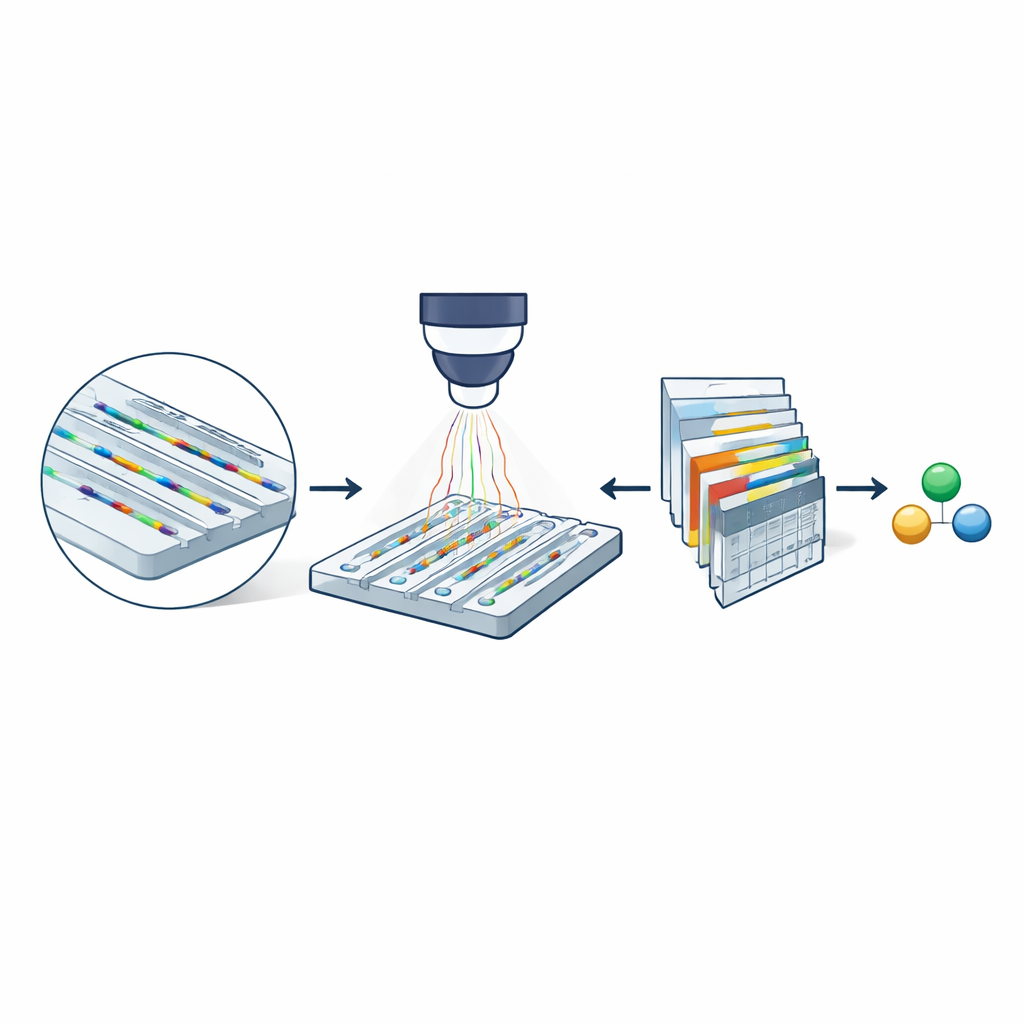
Warum kleinere Kanäle wichtig sind
Selbst mit dieser optischen Verstärkung konnten frühere Versionen der Technik nur Moleküle über etwa 60 Kilodalton charakterisieren – typische große Proteine –, weil die Signale kleinerer Spezies im Rauschen untergingen. Das Team zeigt, dass das Verkleinern des Querschnitts der Nanokanäle die Empfindlichkeit deutlich verbessert: der optische Kontrast eines Moleküls nimmt zu, wenn die Kanalfläche abnimmt. Experimente mit zwei Kanalgrößen und dem Protein Serumalbumin vom Rind zeigen, dass sich seine Bahn im schmaleren Kanal klar abzeichnet, im breiteren Kanal dagegen nahezu verloren geht. Diese einfache geometrische Änderung deutet darauf hin, dass prinzipiell deutlich kleinere Biomoleküle detektierbar werden könnten, sofern ihre schwachen Signale zuverlässig aus verrauschten Bildsequenzen extrahiert werden können.
Eine KI, die verrauschte Filme liest
Um dieses Regime zu erreichen, entwickelten die Forscher ein spezialisiertes Deep-Learning-Modell, den hierarchischen Vision Transformer. Anstatt zu versuchen, die exakte Spur jedes Moleküls Pixel für Pixel zu rekonstruieren, scannt das Modell den Kymographen auf mehreren Skalen und erzeugt zwei Ausgaben: eine Wahrscheinlichkeitskarte, die anzeigt, wo sich ein Molekül zu jedem Zeitpunkt und Ort wahrscheinlich befindet, und eine Eigenschaftskarte, die Schätzungen für Molekulargewicht und hydrodynamische Größe kodiert. Durch Gewichtung der Eigenschaftsschätzungen mit der Wahrscheinlichkeitskarte kann das Modell Bereiche ignorieren, die überwiegend Rauschen sind. Das Training beruht vollständig auf simulierten Trajektorien, die über experimentell gemessenes Hintergrundrauschen gelegt werden, sodass das System lernt, wie reale Signale aussehen sollten, selbst wenn sie mit bloßem Auge kaum sichtbar sind.
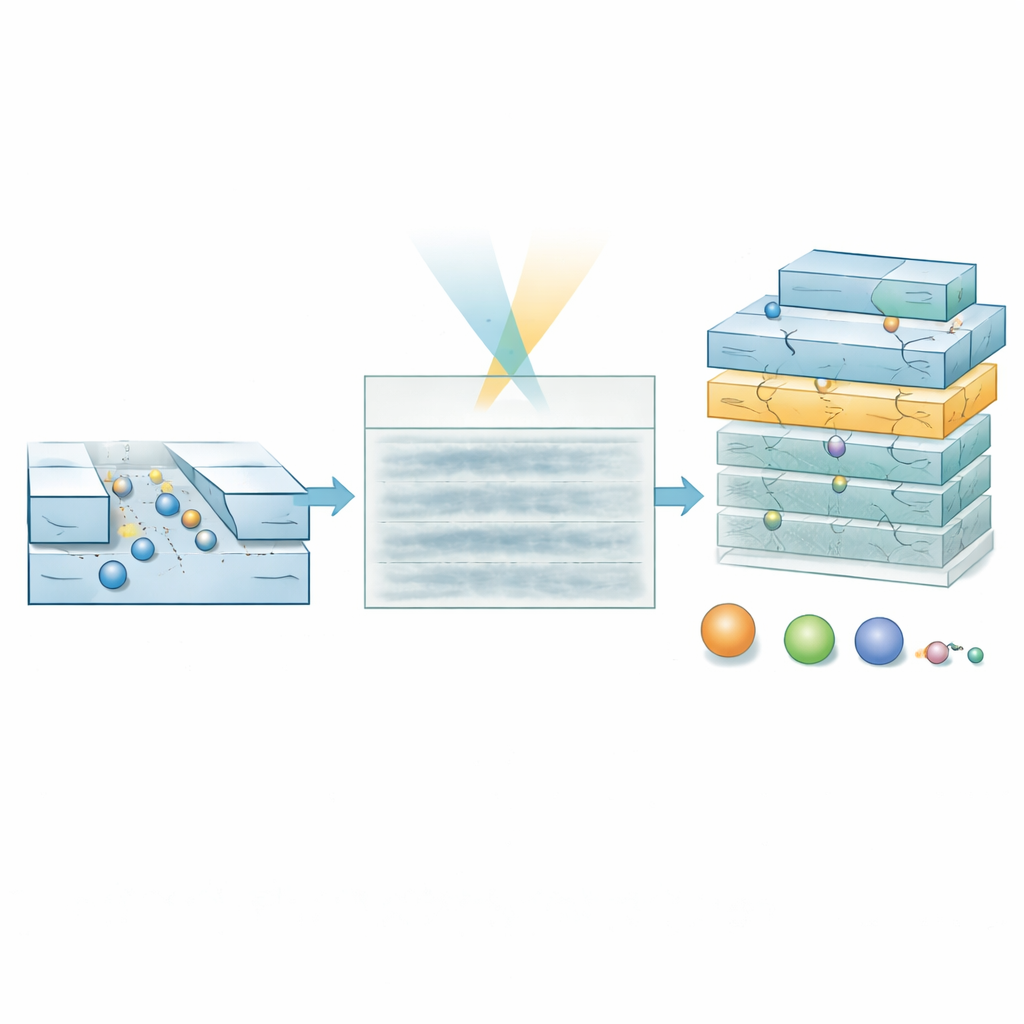
Tests mit DNA- und Hormonmolekülen
Die Autoren validierten den Ansatz zunächst mit einer Standard-DNA-Leiter, einer Mischung doppelsträngiger Fragmente bekannter Länge und Masse, in relativ breiten Kanälen, in denen alle Fragmente absichtlich unterhalb der üblichen Nachweisgrenze lagen. In den Rohfilmen sind keine klaren DNA-Spuren zu sehen. Dennoch erzeugt das KI-Modell Wahrscheinlichkeitskarten, die korrekt anzeigen, wo Moleküle passieren, und sagt Massen voraus, die nach Filterung von gering vertrauenswürdigen Daten den erwarteten Werten entsprechen. Die Methode berichtet außerdem korrekt kleinere effektive Größen für die steifen, stabförmigen DNA-Fragmente gegenüber ihrer vollständigen physikalischen Länge, was widerspiegelt, wie ihre Form die Diffusion beeinflusst. Die anspruchsvollste Prüfung verwendete ultraschmale Kanäle zur Untersuchung des Peptidhormons Insulin, das nur etwa 5,8 Kilodalton wiegt und ungefähr 1,5 Nanometer groß ist. Auch hier erscheinen die Kymographen feldleer, doch das Modell extrahiert einen engen Cluster von Massen- und Größenwerten, die sehr gut mit Literaturwerten übereinstimmen und sich sauber von Pufferkontrollen unterscheiden.
An die Grenzen gehen
Um zu verstehen, wie weit diese Strategie gehen kann, verglich das Team die Präzision des Modells mit der Cramér–Rao-Untergrenze, einer statistischen Grenze, die die bestmögliche Genauigkeit jedes unverzerrten Schätzers für ein gegebenes Rauschebene definiert. Anhand umfangreicher Simulationen zeigen sie, dass die Schätzungen von Masse und Größe des Modells diese theoretische Grenze erreichen, sobald die Anzahl der zur Trajektorie beitragenden Frames etwa zehntausend übersteigt – sogar für ein Teilchen von sechs Kilodalton. Experimente mit Insulin bei verschiedenen Konzentrationen reproduzieren denselben Trend: längere effektive Trajektorien ergeben präzisere Messungen, begrenzt vor allem durch die Verweildauer winziger, schnell diffundierender Moleküle im Sichtfeld. Die Autoren schlagen künftige Strategien vor – wie das sanfte Einfangen von Molekülen in den Kanälen oder das erneute Verwenden von Daten mittels Bootstrapping –, um die nutzbare Beobachtungszeit weiter zu erhöhen.
Bedeutung für Biologie und Medizin
Einfach gesagt zeigt diese Arbeit, dass es nun möglich ist, einige der kleinsten und wichtigsten Moleküle des Körpers einzeln zu wiegen und zu vermessen, ohne sie mit fluoreszierenden Markern zu berühren oder auf einer Oberfläche festzuhalten. Durch die Kombination nanofabrizierter Kanäle mit einer speziell entwickelten KI, die verrauschte Lichtstreuungsfilme liest, senkt die Methode die Massenerfassungsgrenze dieser labelfreien Mikroskopie um etwa den Faktor zehn. Das öffnet die Tür, Familien kleiner Signalmoleküle und Peptidhormone – etwa Zytokine, Chemokine und Insulin – auf Einzelmolekülniveau zu untersuchen und winzige biologische Nanopartikel und Arzneiträger mit beispielloser Empfindlichkeit zu charakterisieren. Wenn sich die Technologie weiterentwickelt, könnte sie ein mächtiges Instrument in der Wirkstoffforschung, Diagnostik und in grundsätzlichen Studien darüber werden, wie molekulare Wechselwirkungen das Leben auf den kleinsten Skalen gestalten.
Zitation: K. Moberg, H., Yeroshenko, B., Fritzsche, J. et al. Label-free mass and size characterization of few-kDa biomolecules by hierarchical vision transformer augmented nanofluidic scattering microscopy. Nat Commun 17, 2533 (2026). https://doi.org/10.1038/s41467-026-70514-z
Schlüsselwörter: labelfreie Einzelmolekülmikroskopie, nanofluidische Streuung, Vision Transformer, kleine Biomoleküle, Insulin-Nachweis