Clear Sky Science · de
Sororin verschließt das DNA-Ausgangstor von Cohesin, um die Schwesterchromatidkohäsion zu bewahren
Kopierte Chromosomen sicher zusammenhalten
Jedes Mal, wenn eine Zelle sich teilt, muss sie ihre DNA kopieren und dann jedem Tochterzelle einen vollständigen Satz übergeben. Entfernen sich diese Kopien zu früh, kann das zu gebrochenen Chromosomen, genetischem Chaos und Krankheiten wie Krebs führen. Diese Studie zeigt, wie ein kurzes Proteinfragment — das Ende von Sororin — wie ein physikalisches Schloss an einer ringförmigen Klammer wirkt, die Schwester‑DNA‑Kopien zusammenhält, und erklärt, wie Zellen Chromosomen bis zum genauen Zeitpunkt der Trennung gepaart halten.
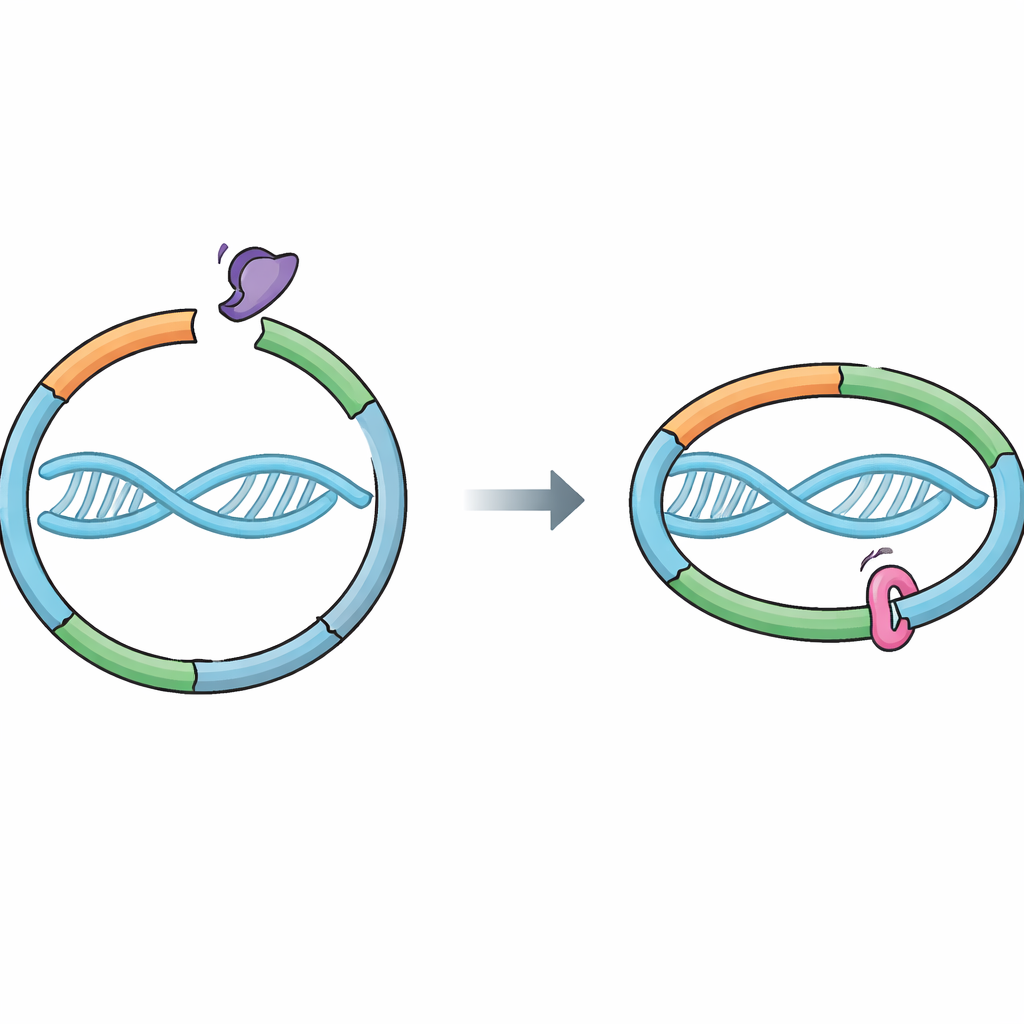
Ein molekularer Ring, der unsere Gene bewacht
Zellen verlassen sich auf eine Proteinfunktion namens Cohesin, um frisch kopierte Chromosomen zusammenzuhalten. Cohesin bildet einen Ring, der die DNA umschließt und die beiden Schwesterstränge verbindet, die während der DNA‑Replikation entstanden sind. Diese Verbindung muss stabil genug sein, um den Erschütterungen der Zellteilung zu widerstehen, aber sich zum richtigen Zeitpunkt lösen lassen, damit die Schwestern sauber trennen können. Ein Helferprotein, Wapl, fördert das Öffnen eines spezifischen „Ausgangstors“ im Ring an der Stelle, wo zwei Cohesin‑Teile, RAD21 und SMC3, aufeinandertreffen. Das Öffnen dieses Tors erlaubt der DNA herauszugleiten und Cohesin zu lösen. Bislang nahm man an, dass Sororin Kohäsion hauptsächlich bewahrt, indem es Wapls Partner Pds5 blockiert; unklar war jedoch, ob Sororin auch direkt den Cohesin‑Ring berührt.
Ein winziger Schwanz mit großer Haltekraft
Die Autoren konzentrierten sich auf Sororins äußerstes Schwanzende — die letzten 30 Aminosäuren, genannt C‑terminaler Bereich (CTR). Durch zerschneiden von Sororin in Stücke und Testen dieser Fragmente in menschlichen Zellen fanden sie heraus, dass genau dieser winzige CTR sowohl notwendig als auch ausreichend ist, um Schwesterchromosomen zusammenzuhalten. Wenn der CTR künstlich an Zentromere gebunden wurde, die zentralen Stellen, an denen Schwestern am längsten verbunden bleiben, konnte er Kohäsion in Zellen ohne vollständiges Sororin nahezu vollständig wiederherstellen. Umgekehrt führte eine Anheftung des CTR entlang des gesamten Chromatins dazu, dass Cohesin nicht mehr effizient entfernt werden konnte und Chromosomen sich nicht richtig verdichteten und entwirrten. Diese Zellen zeigten lange, unscharfe mitotische Chromosomen, DNA‑Brücken zwischen sich trennenden Schwestern und Segregationsfehler — Probleme, die frappierend denen ähneln, die auftreten, wenn Wapl selbst entfernt wird.
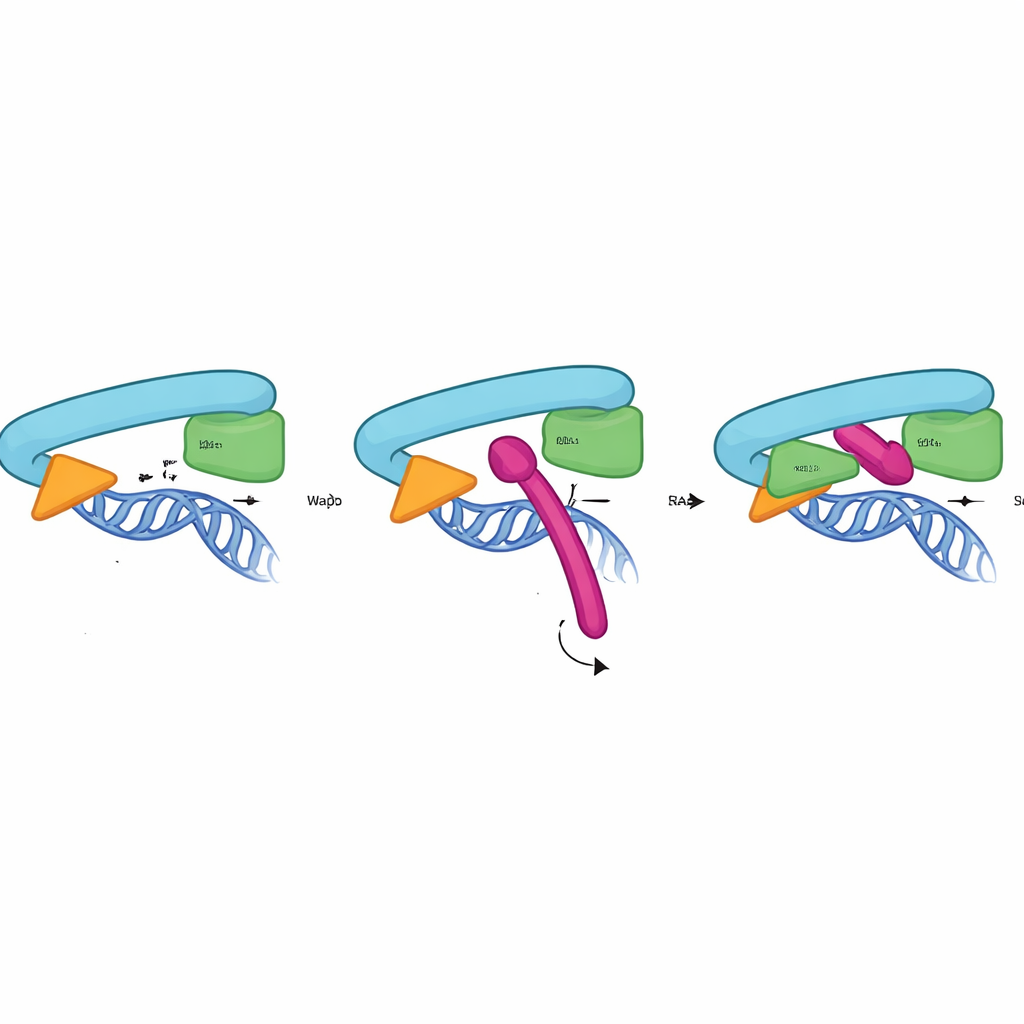
Wie Sororins Schloss am Ring greift
Um zu verstehen, wie der CTR auf atomarer Ebene wirkt, kombinierten die Forscher biochemische Tests, Mutagenese und AlphaFold3‑Strukturvorhersagen. Sie zeigten, dass der CTR direkt und spezifisch an die Schnittstelle zwischen RAD21 und dem Kopfbereich von SMC3 bindet — genau an der Stelle, die das DNA‑Ausgangstor bildet. Diese Wechselwirkung benötigt weder Pds5 noch die SA2‑Untereinheit und tritt nur bei chromatingebundenem Cohesin auf, mit einem Maximum in der Phase, in der Kohäsion stabil erhalten werden muss. Das Strukturmodell legt nahe, dass eine kurze Helix im CTR in eine Tasche zwischen RAD21 und SMC3 einsinkt und sich mit einer Anordnung konservierter hydrophober und negativ geladener Reste festkrallt. Bereits das Mutieren einiger weniger Kontaktpunkte in Sororin, RAD21 oder SMC3 reichte aus, die Bindung aufzuheben und eine vorzeitige Schwesterntrennung zu verursachen — ein eindeutiger Beleg dafür, dass diese Schnittstelle als physikalisches Tor‑Schloss fungiert.
Ein zeitgesteuerter Freigabeschalter für Chromosomentrennung
Zellen müssen Cohesin auch zum richtigen Zeitpunkt freigeben. Das Team entdeckte, dass Sororin eine nahegelegene Kontrollstelle trägt, eine einzelne Aminosäure (S145), die von der mitotischen Kinasen Aurora B phosphoryliert wird. Diese Modifikation löst gezielt Sororins Griff an Pds5, sodass Wapl wieder eingreifen und die Entfernung von Cohesin von den Chromosomenarmen fördern kann, während der Kontakt des CTR mit dem RAD21–SMC3‑Tor weitgehend erhalten bleibt. An den Zentromeren rekrutiert ein anderer Faktor, Sgo1, eine Phosphatase, die diese Phosphatgruppe entfernt und dadurch Sororin–Pds5‑Bindung sowie das starke Tor‑Verschließen bis zum finalen Schnitt von RAD21 in der Anaphase bewahrt. Genetische Tests zeigten, dass beim Entfernen von Wapl die Kohäsionsdefekte, die durch Störung der CTR–Tor‑Interaktion verursacht werden, verschwinden — ein Hinweis darauf, dass Sororins wesentliche Aufgabe darin besteht, das Ausgangstor gezielt vor Wapl‑gesteuertem Öffnen zu schützen.
Was das für Genomstabilität und Krankheit bedeutet
Insgesamt stellen diese Befunde Sororin als Wächter mit Doppelrolle dar: Es konkurriert einerseits mit Wapl um den Zugang zu Pds5 und klemmt andererseits über seinen winzigen CTR das DNA‑Ausgangstor von Cohesin direkt zu. Diese doppelte Kontrolle stellt sicher, dass Kohäsion dort stark ist, wo sie benötigt wird — insbesondere an den Zentromeren — und sich gleichzeitig in der frühen Mitose von den Chromosomenarmen lösen lässt, um richtige Verdichtung und Entwirrung zu ermöglichen. Da Mutationen in Cohesin und seinen Regulatoren häufig bei Entwicklungsstörungen und Krebserkrankungen vorkommen, hebt die präzise kartierte Kontaktfläche zwischen Sororin, RAD21 und SMC3 eine neue Verwundbarkeit hervor, an der kleine Veränderungen Chromosomen destabilisieren können — und einen potenziellen Ansatzpunkt für künftige Therapien, die die Bindung unseres genetischen Materials gezielt modulieren wollen.
Zitation: Chen, Q., Yuan, X., Shi, M. et al. Sororin locks the DNA-exit gate of cohesin to preserve sister-chromatid cohesion. Nat Commun 17, 2284 (2026). https://doi.org/10.1038/s41467-026-70484-2
Schlüsselwörter: Schwesterchromatidkohäsion, Cohesin-Komplex, Sororin, Chromosomentrennung, Genomstabilität