Clear Sky Science · de
Oberflächenhydrophobizität und Steifigkeit bestimmen die Proteinkorona auf oral verabreichten Nanopartikeln zur Behandlung von Kolitis
Pillen in intelligentere Therapien verwandeln
Menschen mit entzündlichen Darmerkrankungen wie Kolitis nehmen oft starke entzündungshemmende Medikamente ein, doch ein großer Teil jeder Dosis geht verloren oder verursacht Nebenwirkungen an anderer Stelle im Körper. Diese Studie untersucht einen neuen Weg, orale Arzneimittel wie gelenkte Geschosse wirken zu lassen: durch das Design winziger, Wirkstoff tragender Partikel, die körpereigene Darmproteine als natürliches Zielsystem anziehen und so dabei helfen, Medikamente zu den Immunzellen zu lenken, die die Entzündung im Darm antreiben.
Wie der Darm Nanopartikel bekleidet
Wenn ein Nanopartikel in den Körper gelangt, wird er schnell von einer dünnen Proteinschicht überzogen, der sogenannten „Proteinkorona“. Im erkrankten Darm sieht diese Korona ganz anders aus als in gesundem Gewebe, weil sich die lokale Proteinmischung verändert hat. Die Autorinnen und Autoren fanden zuvor, dass Kolitis eine spezielle intestinale Korona erzeugt, die Partikel moderat in Richtung Makrophagen lenkt — jener Immunzellen, die Entzündung sowohl antreiben als auch abschwächen können. Hier wollten sie diese Korona gezielt formen, indem sie zwei grundlegende Eigenschaften der Wirkstoffträger anpassen: ihre Wasserabweisung (Hydrophobizität) und ihre Steifigkeit (Rigidity), um den schwachen, krankheitsbedingten Effekt in eine starke Zielsteuerungsstrategie zu verwandeln.
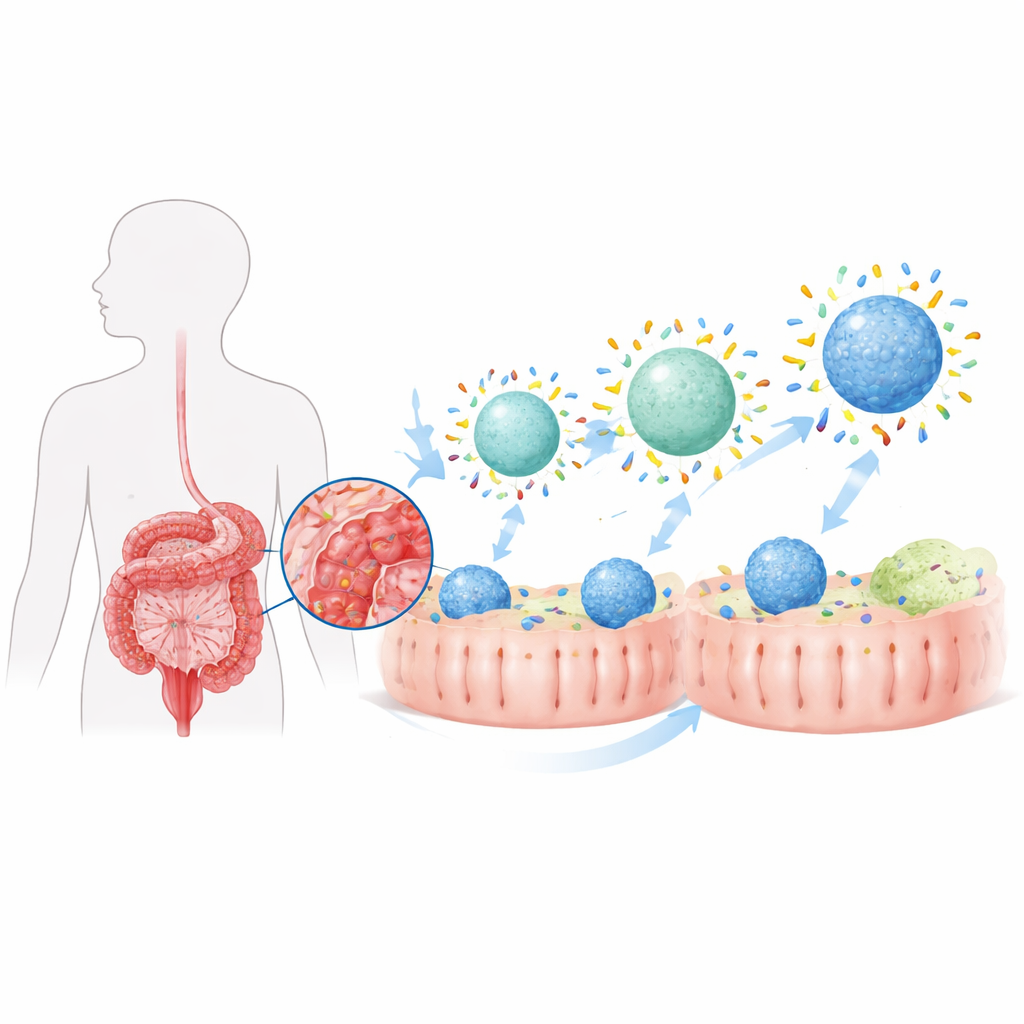
Partikel für Proteine attraktiver machen
Das Team baute lipidbasierte Nanopartikel, ähnlich winzigen Fettbläschen, und justierte, wie wasserliebend oder wasserabweisend ihre Oberflächen durch Zugabe unterschiedlicher Mengen einer üblichen Polymerbeschichtung waren. Partikel mit stärker hydrophoben Oberflächen banden bei Exposition gegenüber Kolitis-Flüssigkeiten deutlich mehr Darmproteine, sowohl in Tiermodellen als auch in Testproben. Wurden diese „phoben“ Partikel mit dem Steroid Budesonid beladen und Ratten mit Kolitis oral verabreicht, lieferten sie weitaus mehr Wirkstoff an Kolon-Makrophagen als die wasserliebenderen Varianten. Infolgedessen gewannen behandelte Tiere mehr Körpergewicht zurück, zeigten weniger Verkürzung des Kolons und Gewebeschäden und hatten niedrigere Werte entzündlicher Moleküle im Darm. Zwar verbesserte sich die Entzündung, kehrte jedoch nicht vollständig in einen gesunden Zustand zurück, was darauf hindeutet, dass allein die Erhöhung der Gesamtmenge an Koronaproteinen nicht ausreichte.
Partikel versteifen, um bessere Partner zu wählen
Um das Konzept weiter voranzutreiben, behielten die Forschenden die Oberflächen hydrophob bei, veränderten jedoch die innere Struktur, um Partikel weich, mittel oder steif zu machen, indem sie ihre Kerne mit Kunststoffkugeln unterschiedlicher Größe füllten. Alle drei Varianten nahmen ähnliche Gesamtmengen an intestinalen Proteinen auf, doch die Zusammensetzung der Proteine änderte sich. Die steifsten Partikel bildeten Koronas, die besonders reich an Proteinen waren, die an Rezeptoren auf Makrophagen andocken oder kleine Nährstoffe transportieren können, die diese Zellen aufnehmen. Ein solches Protein, S100A8, ist im entzündeten Darm reichlich vorhanden und kann spezifische Makrophagenrezeptoren ansprechen. Das Blockieren von S100A8 auf der Korona reduzierte die Aufnahme der steifen Partikel durch Makrophagen deutlich, wodurch es als wichtiger Zielbestandteil identifiziert wurde, der durch die Steifigkeit des Partikels selektiert wird.
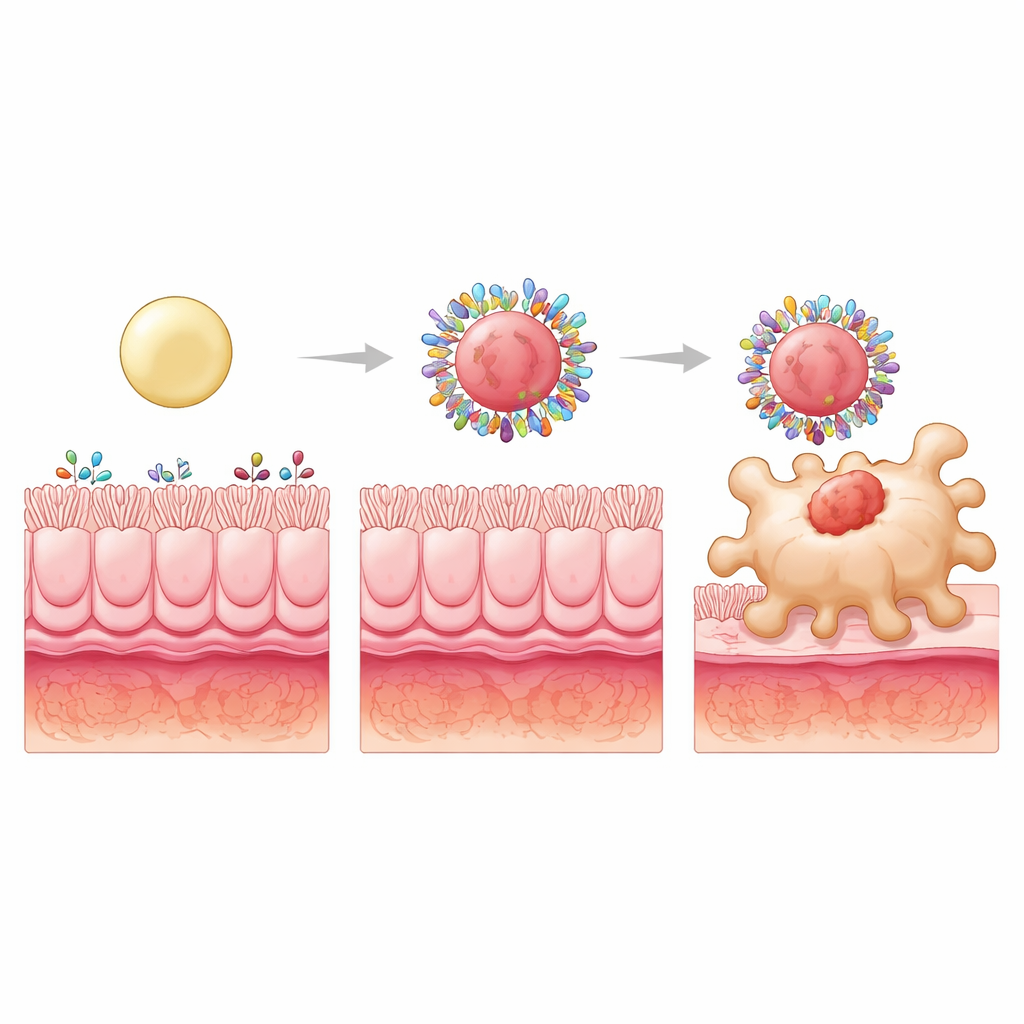
Von besserer Zielsteuerung zu besserer Heilung
Wurde Budesonid in diese hochhydrophoben, hochsteifen Partikel verpackt und Ratten mit Kolitis oral verabreicht, waren die Vorteile deutlich. Die steife Formulierung reduzierte nicht nur Gewebeschäden und oxidativen Stress, sondern normalisierte auch mehrere entzündliche Signale auf Werte, wie sie in gesunden Tieren zu sehen sind. Sie stellte ein gesünderes Gleichgewicht zwischen „angreifenden“ und „beruhigenden“ Makrophagen wieder her und förderte regulatorische T-Zellen, die helfen, Immunreaktionen zu kontrollieren. Wichtig ist, dass diese Verbesserungen von der krankheitsveränderten Proteinumgebung bei Kolitis abhingen; dasselbe Design zeigte in gesunden Ratten keine spezielle Zielsteuerung, was unterstreicht, dass die Korona ein dynamischer, krankheitsspezifischer Verbündeter ist.
Warum das für zukünftige Medikamente wichtig ist
Diese Arbeit zeigt, dass wir körpereigene Proteine als intelligente, sich erneuernde „Etiketten“ auf oralen Wirkstoffträgern nutzen können, indem wir einfach die Oberflächen- und mechanischen Eigenschaften der Träger anpassen. Durch zunächst gesteigerte Proteinerfassung über hydrophobe Oberflächen und anschließendem Einsatz von Steifigkeit, um Makrophagen-anzielende Proteine wie S100A8 zu bevorzugen, schufen die Forschenden Nanopartikel, die von Natur aus die Immunzellen aufsuchen, die Kolitis antreiben, und die Therapie dorthin liefern, wo sie am dringendsten benötigt wird. Dieselbe Designlogik — die Manipulation des „Gefühls“ und Verhaltens von Partikeln an der Darmoberfläche — könnte an viele Arten von Nanomedizinen und Erkrankungen angepasst werden und bietet einen neuen, subtileren Weg zur gezielten Behandlung, ohne künstliche Zielmoleküle anzubringen.
Zitation: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
Schlüsselwörter: Nano-gestützte Wirkstofffreisetzung, entzündliche Darmerkrankung, Proteinkorona, orale Nanomedizin, Makrophagen-Zielsteuerung