Clear Sky Science · de
Ein genusweiter Interaktionsatlas über NS4B-Orthologe identifiziert eine konservierte Rolle der UFMylierung bei der Replikation von Orthoflaviviren
Warum diese Virusstudie wichtig ist
Viren wie Dengue, Zika und West-Nil breiten sich in neue Regionen aus und können Erkrankungen von Fieber bis zu Hirninfektionen und Geburtsfehlern verursachen. Trotzdem fehlen uns nach wie vor breit wirksame, verlässliche Therapien. Diese Studie untersucht, wie eine verborgene Partnerschaft zwischen diesen Viren und einem wenig bekannten zellulären Markierungssystem namens UFMylierung den Erregern beim Vermehren hilft. Indem die Beziehung über viele verwandte Viren hinweg kartiert wird, entdecken die Autorinnen und Autoren eine gemeinsame Schwachstelle, die sich zukünftig zur Entwicklung antiviraler Mittel nutzen lassen könnte.
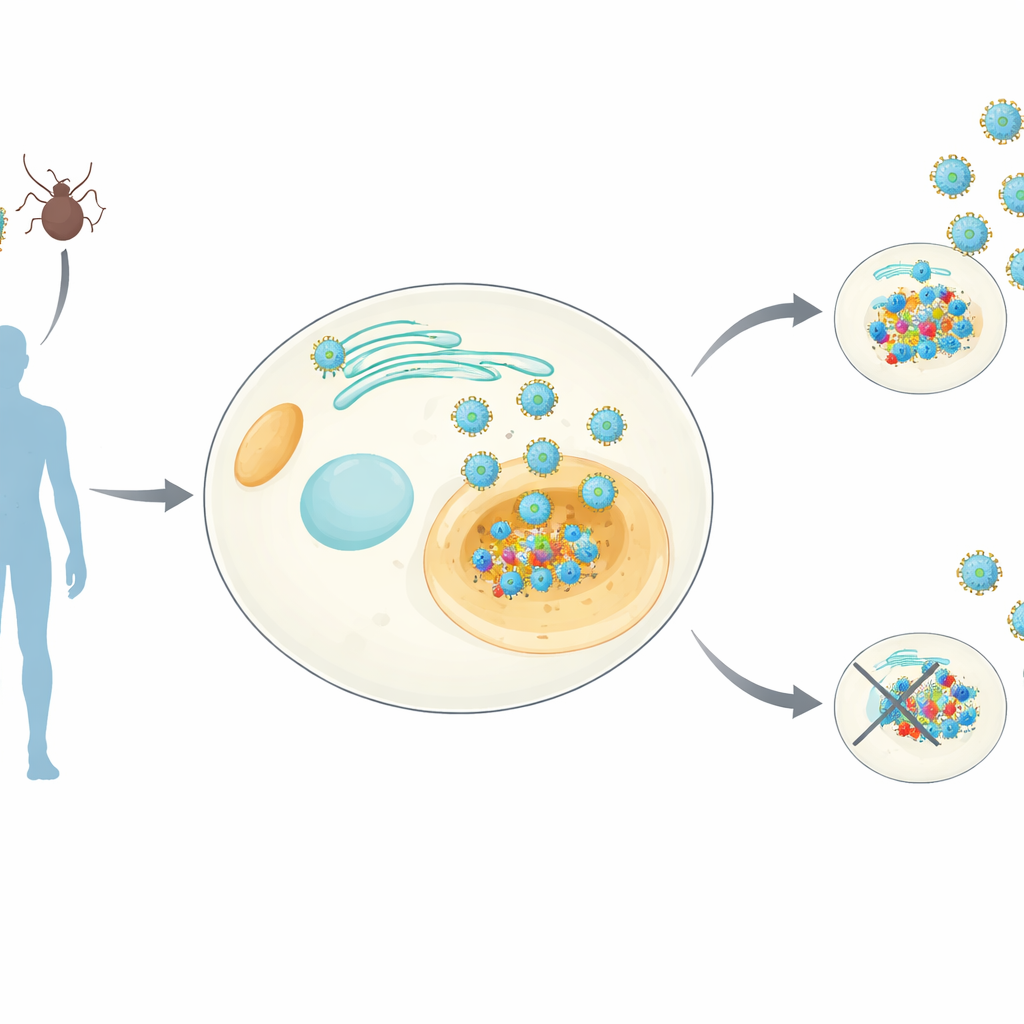
Auf den Spuren eines wichtigen viralen Insiders
Orthoflaviviren – die Gruppe, zu der Dengue, Zika, Gelbfieber und andere gehören – tragen alle ein kleines Protein namens NS4B, das sich in Membranen innerhalb unserer Zellen einnistet. NS4B ist für die virale Replikation essentiell, doch seine genauen Aufgaben blieben unklar. Die Forschenden erzeugten humane Zelllinien, die stabil NS4B von acht verschiedenen Orthoflaviviren produzieren. Anschließend nutzten sie empfindliche Massenspektrometrie-Verfahren, um NS4B zusammen mit allen daran haftenden menschlichen Proteinen herauszufischen, und maßen parallel, wie die NS4B-Expression das gesamte Proteom der Zelle verändert. Das ergab einen genusweiten "Interaktionsatlas" – den sie NS4Bom nennen – der sowohl gemeinsame als auch virusspezifische Wirtsziele zeigt.
Geteilte Tricks und individuelle Anpassungen
Der Atlas offenbarte 538 menschliche Proteine, die mit NS4B interagieren, und mehr als 500 Proteine, deren Menge sich bei NS4B-Präsenz verändert. Viele davon konzentrieren sich auf Wege, die Energieproduktion in Mitochondrien, die Formung interner Membranen und den Transport neu synthetisierter Proteine und Lipide steuern. Einige Interaktionen wurden von den meisten Viren geteilt, was auf evolutionär konservierte Tricks hinweist, die alle Orthoflaviviren nutzen. Andere traten nur in bestimmten Arten oder Stämmen auf und könnten erklären, warum manche Viren Mücken statt Zecken bevorzugen oder Hirnerkrankungen statt hämorrhagischem Fieber verursachen. Diese systematische Übersicht verwandelt eine zersplitterte Sammlung früherer Einzelergebnisse in eine kohärente Karte, wie diese Viren die Zelle umprogrammieren.
Ein überraschender Verbündeter: das UFMylierung-System
Unter den vielen Partnern, an die NS4B andockte, fiel eines besonders auf: UBA5, das aktivierende Enzym der UFMylierungs‑Kaskade. UFMylierung ist ein zelluläres System, das das kleine Protein UFM1 an ausgewählte Zielmoleküle anhängt und so Prozesse wie Protequalitätskontrolle und Stressantworten beeinflusst. Mithilfe von RNA-Interferenz und CRISPR-basierten Gen-Knockouts zeigte das Team, dass Zellen ohne UBA5 oder anderweitig unfähig zur UFMylierung eine stark verringerte Replikation von Zika und mehreren verwandten Viren aufwiesen. Die Wiedereinführung normaler UBA5‑Funktionen stellte das Virenwachstum wieder her, während Mutanten, die die UFMylierung nicht mehr ausführen konnten, dies nicht taten – ein Beleg dafür, dass gerade die Markierungsaktivität für die Infektion entscheidend ist.
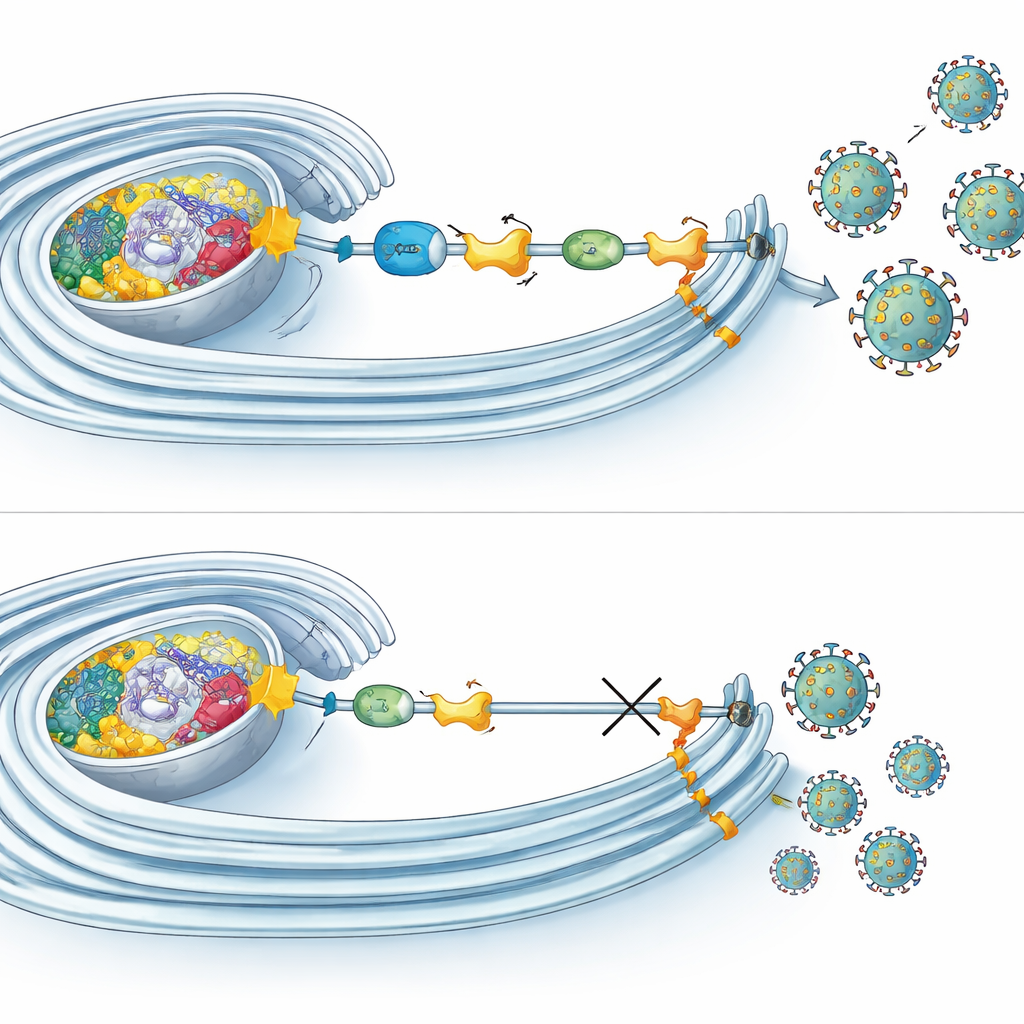
Wie die Markierung virale Fabriken unterstützt
Mikroskopische und biochemische Experimente zeigten, dass mehrere Komponenten der UFMylierung genau an den Stellen zusammenkommen, an denen virale RNA in umgestalteten Membranen kopiert wird. Dort assoziieren sie nicht nur mit NS4B, sondern auch mit anderen viralen Proteinen, die die Replikationsmaschinerie aufbauen. Interessanterweise blockierte das Abschalten der UFMylierung nicht das Eindringen des Virus, die RNA-Produktion oder die Proteinsynthese. Stattdessen wurde vor allem der späte Zyklusabschnitt beeinträchtigt, etwa der Zusammenbau oder die Freisetzung infektiöser Partikel. Gleichzeitig beeinflusste die UFMylierung die mitochondriale Atmung: Wenn der Weg deaktiviert war, zeigten Zellen reduzierte Sauerstoffverbrauchswerte und veränderte Mitochondrienformen. Im Gegensatz dazu stieg die mitochondriale Atmung früh während der Zika-Infektion an, was darauf hindeutet, dass Viren die UFMylierung anzapfen könnten, um die Energieproduktion der Zelle genau dann zu steigern, wenn sie sie am meisten brauchen.
Test eines Medikaments in Zellen und winzigen Fischen
Die Autorinnen und Autoren untersuchten anschließend eine kleinmolekulare Verbindung, DKM 2‑93, die die aktive Stelle von UBA5 blockiert. In kultivierten Humanzellen reduzierte dieser Inhibitor die Zika-Virusproduktion um etwa das Zehnfache bei Dosen, die die Zellen größtenteils unverändert ließen, und zeigte Wirksamkeit in mehreren Zelltypen. Um zu prüfen, ob die Strategie auch in einem lebenden Organismus wirkt, verwendeten sie ein Zebrafischmodell der Zika-Infektion, das wichtige Merkmale der Erkrankung im sich entwickelnden Gehirn nachbildet. Die Behandlung infizierter Embryonen mit DKM 2‑93 während der frühen Hirnentwicklung senkte die virale RNA-Menge deutlich und verringerte den Anteil der Fische mit schweren Missbildungen, was einen echten antiviralen Nutzen in vivo anzeigt.
Was das für zukünftige Behandlungen bedeutet
Durch den Aufbau einer umfassenden Karte, wie NS4B vieler Orthoflaviviren mit menschlichen Proteinen interagiert, rückt diese Studie die UFMylierung als konservierten Helferweg in den Fokus, den diese Viren zur Produktion infektiöser Partikel benötigen. Da dasselbe Wirtsystem offenbar Dengue, Zika, West-Nil und andere unterstützt, könnten Wirkstoffe, die die UFMylierung gezielt dämpfen, als Breitbandantiviralia wirken, statt nur einen einzelnen Erreger anzugehen. Zwar ist weitere Forschung nötig, um genau zu klären, welche Proteine markiert werden und die Sicherheit solcher Eingriffe zu bestätigen, doch die Ergebnisse identifizieren ein vielversprechendes wirtsspezifisches Ziel, das eines Tages helfen könnte, Ausbrüche mehrerer durch Mücken und Zecken übertragener Krankheiten mit einem einzigen Therapieansatz zu mildern.
Zitation: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
Schlüsselwörter: Zika-Virus, Dengue, Wirt–Virus-Interaktionen, UFMylierung, Breitbandantiviralia