Clear Sky Science · de
3D‑Pentakultur‑Modell enthüllt malign gesteuerte Makrophagenpolarisation beim hochgradigen serösen Ovarialkarzinom
Warum diese Forschung wichtig ist
Eierstockkrebs wird oft spät entdeckt und kann sich hartnäckig gegen Therapien erweisen. Ein Grund ist, dass Krebszellen in einer unterstützenden Nachbarschaft aus Immun‑ und Bindegewebszellen leben, die ihnen helfen, Medikamente und die Abwehr des Körpers zu umgehen. Diese Studie entwickelt ein ausgeklügeltes Labor‑Modell — mit fünf menschlichen Zelltypen in 3D — um diese Nachbarschaft nachzubilden und in Echtzeit zu beobachten, wie Krebszellen benachbarte Immunzellen, sogenannte Makrophagen, dazu bringen, dem Tumor zu helfen, statt ihn zu bekämpfen.
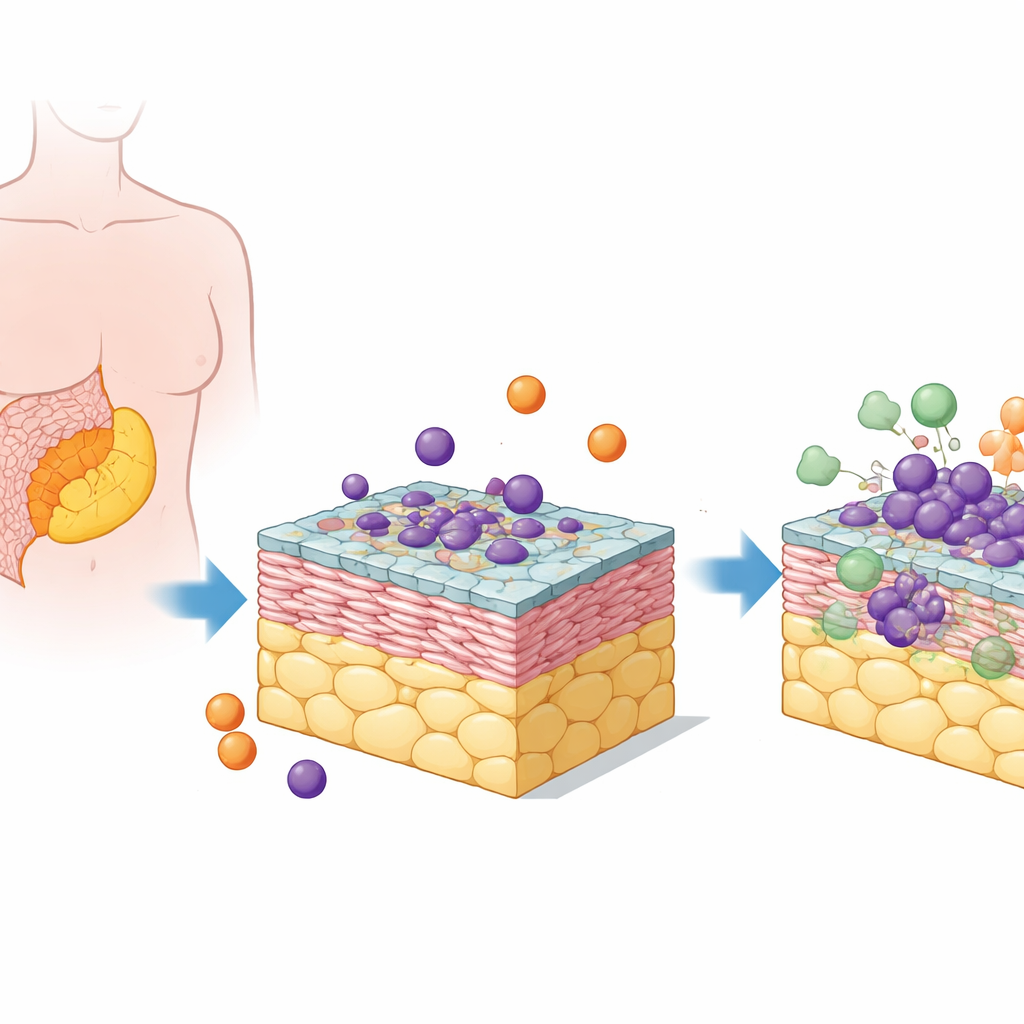
Bau einer winzigen Tumornachbarschaft
Die Forschenden konzentrierten sich auf das hochgradige seröse Ovarialkarzinom, die häufigste und tödlichste Form der Erkrankung. Seine Metastasen wachsen häufig im Omentum, einem Fettgewebe im Bauchraum. Um dieses Umfeld nachzustellen, kombinierten die Teams menschliche Fettzellen, Bindegewebszellen (Fibroblasten), eine Mesothel‑Epithel‑Schicht, Eierstockkrebszellen und zirkulierende Immunzellen, sogenannte Monozyten. Diese fünf Zelltypen wurden zu geschichteten 3D‑„Pentakulturen“ zusammengestellt, die echten Tumorablagerungen näher kommen als flache Zellschichten in einer Petrischale.
Verwandlung von Immunverteidigern in Beiwerk
Innerhalb dieses Mini‑Tumorumfelds reiften Monozyten auf natürliche Weise zu Makrophagen heran — ohne die künstlichen Wachstumsfaktoren, die im Labor sonst üblicherweise zugegeben werden. Mittels Genaktivitätsprofilierung und Vergleichen mit Einzelzell‑Daten aus Patiententumoren zeigten die Forschenden, dass die Makrophagen im Modell denen in echten Ovarialmetastasen sehr ähnlich sind. Verschiedene Krebszelllinien erzeugten unterschiedliche Mischungen von Makrophagentypen und verschiedene Gesamtarchitekturen der Mini‑Tumoren, was darauf hindeutet, dass genetische und molekulare Unterschiede innerhalb der Krebszellen die umliegende Immunlandschaft stark prägen.
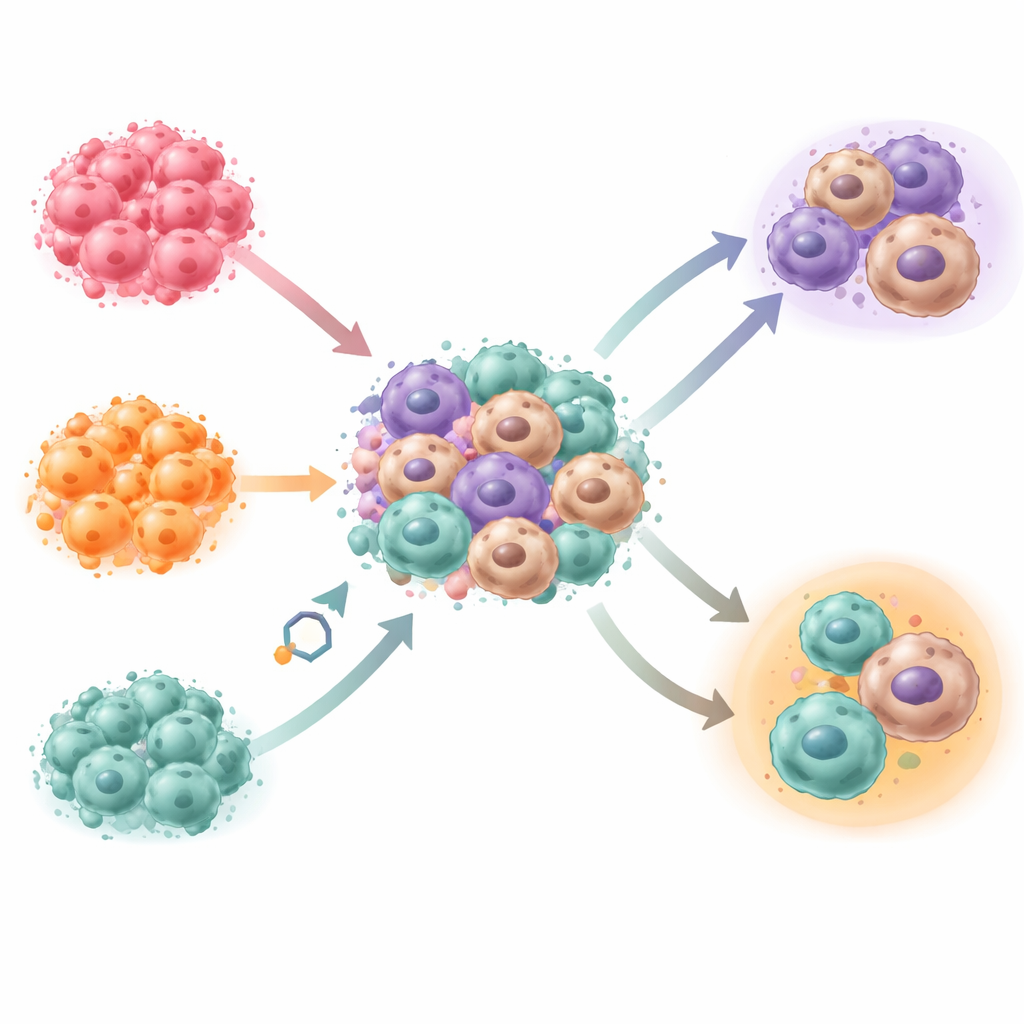
Wie Krebszellen dem Verschlucktwerden entgehen
Makrophagen können Krebszellen verschlingen und zerstören, aber Tumoren senden oft „Nicht‑fressen‑mich“‑Signale über ihre Oberfläche aus. Das Team untersuchte zwei solche Signale, CD47 und CD24, an drei in dem 3D‑Modell gezüchteten Eierstockkrebszelllinien. Krebszellen mit höheren Mengen dieser Signale wurden seltener von Makrophagen aufgenommen. In den Pentakulturen wurde eine Zelllinie leicht verschlungen, eine andere weitgehend verschont und eine dritte zeigte ein gemischtes Verhalten. Live‑Aufnahmen zeigten, dass sich Makrophagen je nach Krebszelllinie unterschiedlich bewegten und sich näher an oder weiter von Krebsclustern positionierten — ein Muster, das auch in Patientengeweben beobachtet wird.
Testen von Wegen zur Wiederaktivierung der Immunantwort
Da sich diese Oberflächensignale mit Antikörpern blockieren lassen, behandelten die Forschenden die Modelle mit experimentellen Antikörpern gegen CD47 oder CD24. In Pentakulturen, die mit einer bestimmten Zelllinie aufgebaut waren, erhöhte die Blockade eines der Signale die Makrophagenkontakte mit Krebszellen, steigerte das Verschlingen und reduzierte die Zahl der Krebszellen, während die übrigen Zelltypen im Modell weitgehend unversehrt blieben. In einer anderen, stark resistenten Zelllinie zeigte die Blockade dieser Signale kaum Wirkung, doch die Inhibition eines separaten Kommunikationsweges (der TGFβ‑Signalachse) reduzierte die Krebszellzahlen auf eine Weise, die weiterhin von der Anwesenheit von Makrophagen abhing — was auf alternative, nicht‑Verschlingungs‑Tötungsmechanismen wie die Freisetzung toxischer Zytokine hindeutet.
Was das für Patienten bedeutet
Für eine fachfremde Leserin oder einen fachfremden Leser ist die wesentliche Botschaft, dass nicht alle Eierstocktumoren Immunzellen auf die gleiche Weise manipulieren, selbst wenn sie unter dem Mikroskop ähnlich erscheinen. Durch den Aufbau eines realistischen fünfzelligen 3D‑Modells aus menschlichem Gewebe zeigt diese Arbeit, wie Tumorzellen Makrophagen so einstellen können, dass sie sie entweder ignorieren oder angreifen, und wie die Blockade spezifischer „Nicht‑fressen‑mich“‑Signale diesen Schalter manchmal umlegen kann. Das Modell spiegelt Patiententumoren gut wider und ist damit ein vielversprechendes Testsystem mittlerer Durchsatzkapazität, um herauszufinden, welche immunzielgerichteten Medikamente für welche Tumorprofile wahrscheinlich wirksam sind. Langfristig könnten solche maßgeschneiderten Laborsysteme helfen, einzelne Patientinnen und Patienten besser den Therapien zuzuordnen, die ihre eigenen Immunzellen gegen den Eierstockkrebs am wirkungsvollsten wieder aktivieren.
Zitation: Malacrida, B., Elorbany, S., Laforêts, F. et al. 3D pentaculture model unveils malignant cell-driven macrophage polarization in high-grade serous ovarian cancer. Nat Commun 17, 2451 (2026). https://doi.org/10.1038/s41467-026-70398-z
Schlüsselwörter: Eierstockkrebs, Tumormikroumgebung, Makrophagen, Immuntherapie, 3D‑Zellkultur