Clear Sky Science · de
Ribosomale Modifikationen stehen im Zusammenhang mit der Auswahl mesenchymaler Zellschicksale in der Neuralleistenzelllinie
Wie winzige Zellfabriken Gesichter und Tumoren formen
Unsere Gesichter und Teile unseres Nervensystems entstehen aus einer wandernden Gruppe embryonaler Zellen, der Neuralleiste. Diese Zellen können zu Knochen, Knorpel, Nerven und mehr werden. Die Studie zeigt, dass ihre Entscheidungen nicht nur von Genen abhängen, sondern auch von feinen chemischen Veränderungen an den Proteinfabriken der Zelle – den Ribosomen. Dieselben molekularen Eigenschaften, die beim Aufbau eines normalen Gesichts helfen, können bei Fehlsteuerung gefährlichere Formen von Kinderkrebs kennzeichnen.
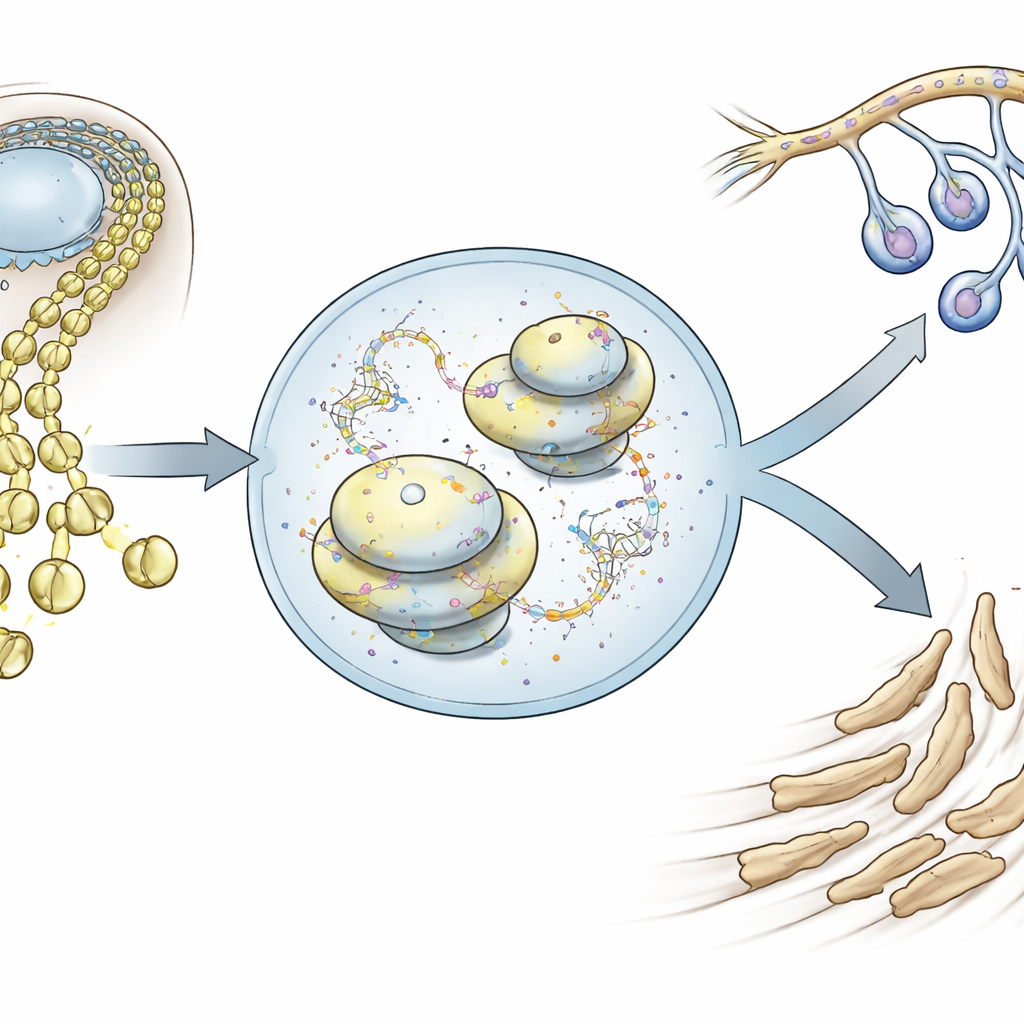
Formwandelnde Zellen, die das Gesicht bilden
Neuralleistenzellen entstehen entlang des frühen Gehirns und Rückenmarks und wandern dann nach außen, wobei sie schließlich einen Großteil des Schädels, der Kiefer und der peripheren Nerven bilden. Mithilfe von Einzelzell-RNA-Sequenzierung in Maus-Embryonen verfolgten die Autor:innen tausende einzelne kraniale Neuralleistenzellen, wie sie das Neuralrohr verließen und ins Gesicht zogen. Sie fanden heraus, dass diese Zellen sehr früh bereits eine subtile Neigung zu einem von zwei Hauptschicksalen zeigen: einem mesenchymalen Weg, der Gesichtsknochen und Knorpel bildet, oder einem neuro-glialen Weg, der Neuronen und gliale Stützzellen hervorbringt. Diese beiden Genaktivitätsprogramme liegen anfangs gemischt in denselben Zellen vor, werden mit der Entwicklung aber gegenseitig ausschließend und erzwingen so eine Schicksalsentscheidung.
Proteinfabriken als Entscheidungsträger
Als das Team untersuchte, welche Gene mit der frühen Neigung zur facialen Mesenchym-Bildung verknüpft sind, kamen zwei Hauptgruppen zum Vorschein. Die eine enthielt bekannte Akteure, die Zellen lockern, bewegen und Identität ändern lassen – ein Vorgang, der als epithelial-mesenchymale Transition bekannt ist. Die andere, überraschendere Gruppe drehte sich um die Ribosomenzusammenlagerung und die chemische Modifikation ribosomaler RNA, den Kern der Proteinfertigungsmaschinerie. Statt einfach mehr Ribosomen zu produzieren, schalteten kraniale Neuralleistenzellen Faktoren ein, die feinsteinstellungen an der Ribosomen-Biogenese und deren chemischer Kennzeichnung vornehmen. Die Störung der ribosomalen RNA-Produktion in Maus-Embryonen zum Zeitpunkt der Schicksalsentscheidung verschonte weitgehend die sich entwickelnden Nerven, ließ jedoch die Gesichtsskelettstrukturen stark verkümmern. Dies zeigt, dass der mesenchymale Weg besonders abhängig von dieser ribosomalen Kontrolle ist.
Eine besondere Markierung auf ribosomaler RNA
Bei genauerem Hinsehen konzentrierten sich die Forschenden auf ein einzelnes Nukleotid innerhalb der 18S-ribosomalen RNA, an einer Position, die für die genaue Proteinbiosynthese wichtig ist. In kranialen Neuralleistenzellen, die zum mesenchymalen Schicksal geneigt waren, wurde diese Position in den Sequenzdaten wiederholt falsch gelesen – ein Kennzeichen für starke chemische Modifikation statt einer echten Mutation. Frühere Arbeiten hatten gezeigt, dass ein Trio von Enzymen an dieser Stelle durch mehrere Schritte eine komplexe Modifikation anbringt. Durch die Kombination menschlicher genomischer und RNA-Daten mit Massenspektrometrie aus Maus-Embryonen bestätigte die Studie, dass diese Stelle in der DNA unverändert ist, aber in der RNA unterschiedlich stark chemisch modifiziert vorkommt und dass der Anteil der modifizierten Form zwischen Gehirn- und Gesichtgewebe variiert. Durch Überexpression oder Ausschalten der Enzyme, die diese Modifikation erzeugen, in Zellkulturen und Maus-Embryonen wurde die Neuralleistenentwicklung gestört und es entstanden ausgeprägte kraniofaziale Defekte. Das unterstreicht, dass präzise Mengen dieses RNA-Fingerabdrucks helfen, Zellen in den skeletogenen Pfad zu lenken.
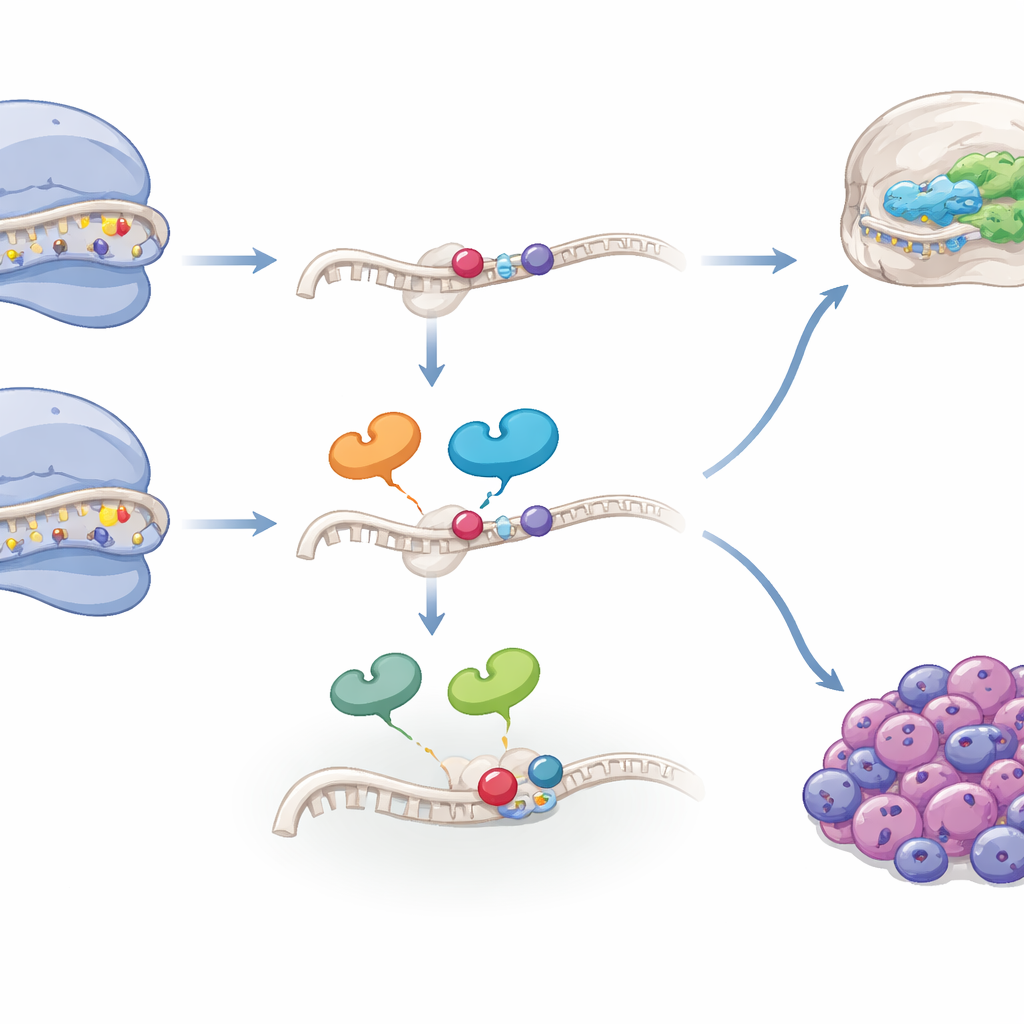
Von der Entwicklung zum Krebsrisiko
Da Neuralleistenzellen auch Tumoren wie Neuroblastome hervorrufen können, fragten die Autor:innen, ob dieselben ribosomalen Merkmale in Krebs vorkommen. Bei der Analyse von Einzelzell- und Bulk-RNA-Daten aus mehreren Neuroblastom- und Hirntumor-Kohorten fanden sie, dass eine ribosomale „Kontrolle- und RNA-Modifikations“-Gen-Signatur in Tumorzell-Subpopulationen mit stärker mesenchymal ähnlichen Eigenschaften angereichert ist – Zustände, die oft mit Therapieresistenz und schlechter Prognose verbunden sind. In mehreren Patientenkohorten sagten hohe Werte dieser Signatur eine deutlich schlechtere Überlebensrate voraus, insbesondere bei Neuroblastomen ohne Amplifikation des bekannten Risikogens MYCN. Bestimmte Komponenten, wie der Assemblierungsfaktor WDR74 und das Modifikationsenzym TSR3, waren in aggressiven Zelllinien erhöht und machten diese Zellen empfindlicher gegenüber Medikamenten, die das Ribosom stressen. Auffällig war außerdem, dass Tumoren mit sehr niedrigen oder sehr hohen Levels der Schlüssel-RNA-Modifikation an der hervorgehobenen Stelle schlechter abschnitten als solche mit mittleren Werten, was nahelegt, dass sowohl Mangel als auch Überschuss dieses spezialisierten Ribosomenpools schädlich sein können.
Was das für Gesichter und Kinderkrebs bedeutet
Zusammen deuten diese Ergebnisse darauf hin, dass Ribosomen nicht bloß passive Proteinfabriken sind, sondern abgestimmte Geräte, deren chemische Zusammensetzung mitentscheidet, wie embryonale Zellen das Gesicht formen und wie sich manche Tumoren verhalten. In Neuralleistenzellen scheint eine bestimmte chemische Markierung auf ribosomaler RNA die Produktion von Proteinen zu begünstigen, die für die Bildung von Gesichtsknochen und Knorpel benötigt werden, während ihre Fehlregulation in Krebs mit gefährlicheren, formwandelnden Tumorzellen assoziiert ist. Das Verständnis und die mögliche gezielte Beeinflussung dieses ribosomalen „Feintexts“ könnten neue Wege eröffnen, kraniofaziale Fehlbildungen zu verhindern und hochriskante Neuroblastome zu identifizieren oder zu behandeln.
Zitation: Poverennaya, I., Murtazina, A., Li, L. et al. Ribosomal modifications are associated with mesenchymal fate selection in the neural crest lineage. Nat Commun 17, 2326 (2026). https://doi.org/10.1038/s41467-026-70375-6
Schlüsselwörter: Entwicklung der Neuralleiste, Ribosom-Modifikationen, Kraniofaziale Bildung, Neuroblastom, spezialisierte Ribosomen