Clear Sky Science · de
CPF‑CF‑terminierte snoRNAs pendeln durch das Zytoplasma über einen von mRNA‑Schutzproteinen vermittelten Überwachungsmechanismus
Wie winzige RNA‑Guides einen unerwarteten Umweg nehmen
In jeder Zelle hängt die Proteinsynthese von einer präzisen molekularen Choreographie ab. Ein zentraler Teil dieses Ablaufs wird von kleinen nucleolaren RNAs, den snoRNAs, gesteuert, die beim Formen der Ribosomen helfen — der Maschinen, die Proteine bauen. Diese Studie zeigt, dass einige dieser winzigen Guides unerwartet den Zellkern verlassen, kurz das Zytoplasma passieren und dann zurückkehren, und dass dies mit der Art zusammenhängt, wie ihre Produktion beendet wird. Das Verständnis dieser verborgenen Verkehrsroute erläutert, wie Zellen die RNA‑Qualität schützen und ihre genetische Information bewahren.
Ein genauerer Blick auf die RNA‑Hilfsarbeiter der Zelle
SnoRNAs sind kurze RNA‑Moleküle, die als Guides fungieren und chemische Modifikationen auf andere RNAs lenken, insbesondere auf solche, die Ribosomen bilden. In Hefezellen werden die meisten snoRNAs im Zellkern hergestellt und galten dort als dauerhaft verbleibend, indem sie stabile Partnerschaften mit spezifischen Proteinen eingehen und so snoRNPs bilden, die funktionellen Komplexe, die ribosomale RNA modifizieren. Frühere Arbeiten hatten jedoch gezeigt, dass snoRNAs mit Proteinen in Kontakt kommen, die sonst für den Export von messenger RNAs aus dem Kern zuständig sind. Diese überraschende Beobachtung warf die Frage auf: Reisen snoRNAs manchmal ins Zytoplasma, und falls ja, warum?
Entdeckung beweglicher snoRNAs
Durch die erneute Auswertung von RNA‑Sequenzierungsdaten aus sorgfältig getrennten Kern‑ und Zytoplasmafraktionen fanden die Autor:innen heraus, dass viele snoRNAs tatsächlich im Zytoplasma normaler Hefezellen vorkommen, in Mengen, die denen typischer mRNAs ähneln. Wenn sie wichtige Exportfaktoren, Mex67 und Xpo1, ausschalteten, nahm der zytoplasmatische Pool an snoRNAs ab und unreife, 3′‑verlängerte snoRNA‑Vorstufen häuften sich im Kern. Mikroskopische Untersuchungen mit fluoreszenten Sonden bestätigten diese Verschiebung: Signale, die normalerweise sowohl im Nucleolus als auch schwach im Zytoplasma erschienen, wurden stark nukleär, wenn der Export blockiert war. Diese Befunde zeigen, dass ein Subset von snoRNAs, häufig noch mit zusätzlichen Endsequenzen, aktiv aus dem Kern transportiert wird und nicht bloß durch Leckage oder Kontamination entsteht.
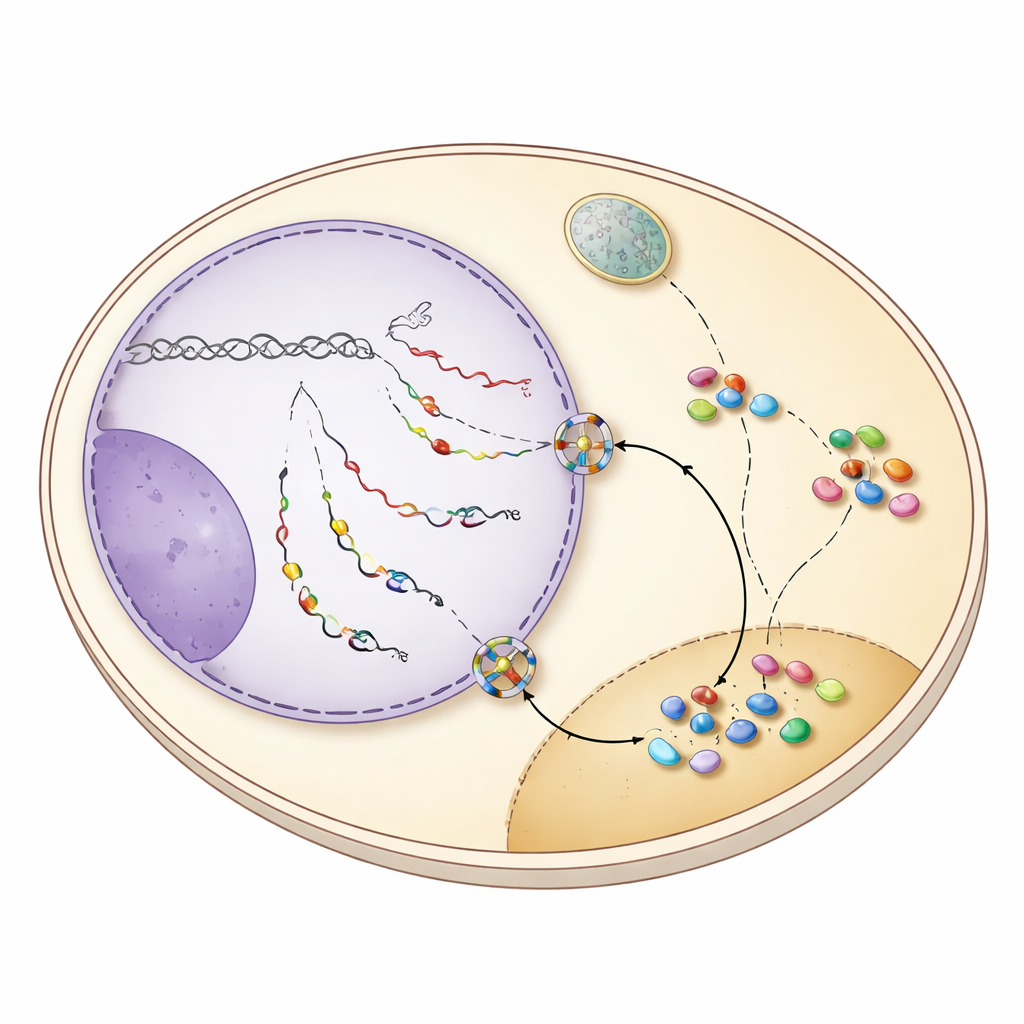
Der Schutzprotein‑Schalter, der snoRNAs hinausentsendet
Der Schlüssel zu diesem Shuttle‑Verhalten liegt in der Art, wie die Transkription von snoRNAs terminiert wird. In Hefe werden die meisten snoRNAs normalerweise durch ein System namens NNS von der Transkriptionsmaschinerie abgeschnitten, wodurch sie mit einem kurzen Schwanz zurückbleiben, der schnell im Kern beschnitten wird. Viele snoRNA‑Gene besitzen jedoch auch Backup‑Stoppstellen, die von einem zweiten System, CPF‑CF, erkannt werden, das vor allem dafür bekannt ist, mRNAs zu beenden und lange Poly(A)‑Schwänze hinzuzufügen. Wenn die NNS‑Termination versagt, laufen snoRNA‑Transkripte bis zu diesen nachfolgenden CPF‑CF‑Stellen weiter und erhalten einen längeren Schwanz. Dieses veränderte Ende rekrutiert eine Gruppe von „Schutz“proteinen — unter ihnen Hrp1 und Nab2 —, die die korrekte Verarbeitung prüfen und gleichzeitig den Exportfaktor Mex67 anziehen. Die Studie zeigt, dass, wenn snoRNAs durch CPF‑CF beendet werden, Schutzproteine und Mex67 gemeinsam wirken, um diese geschwänzten snoRNAs durch Kernporen ins Zytoplasma zu schicken.
Hin‑ und Rückfahrkarten und Qualitätskontrolle
Einmal im Zytoplasma, werden snoRNAs nicht sich selbst überlassen. Sie bleiben von einem schützenden Ring aus Lsm‑Proteinen und dem Faktor Lhp1 umgeben, die das verwundbare RNA‑Ende abschirmen. Diese Merkmale erlauben es zwei Importrezeptoren, Cse1 und Mtr10, die shuttlenden snoRNAs zu erkennen und zurück in den Kern zu bringen. Als die Autor:innen diese Importfaktoren oder den Lsm‑Ring deaktivierten, sammelten sich unreife snoRNAs im Zytoplasma an, was bestätigte, dass diese Maschinerie ihre Rückkehr vermittelt. Zurück im Kern werden die langen Schwänze durch das nukleäre Exosom beschnitten, Kern‑snoRNP‑Proteine vollständig zusammengesetzt und die reifen Komplexe wieder zum Nucleolus umverteilt. Wichtig ist: snoRNAs, die diesen Umweg genommen hatten, blieben voll funktionsfähig: eine Modell‑snoRNA, snR13, führte ihre spezifischen chemischen Modifikationen an ribosomaler RNA weiterhin aus, nachdem sie durch CPF‑CF terminiert und durchs Zytoplasma geschickt worden war.
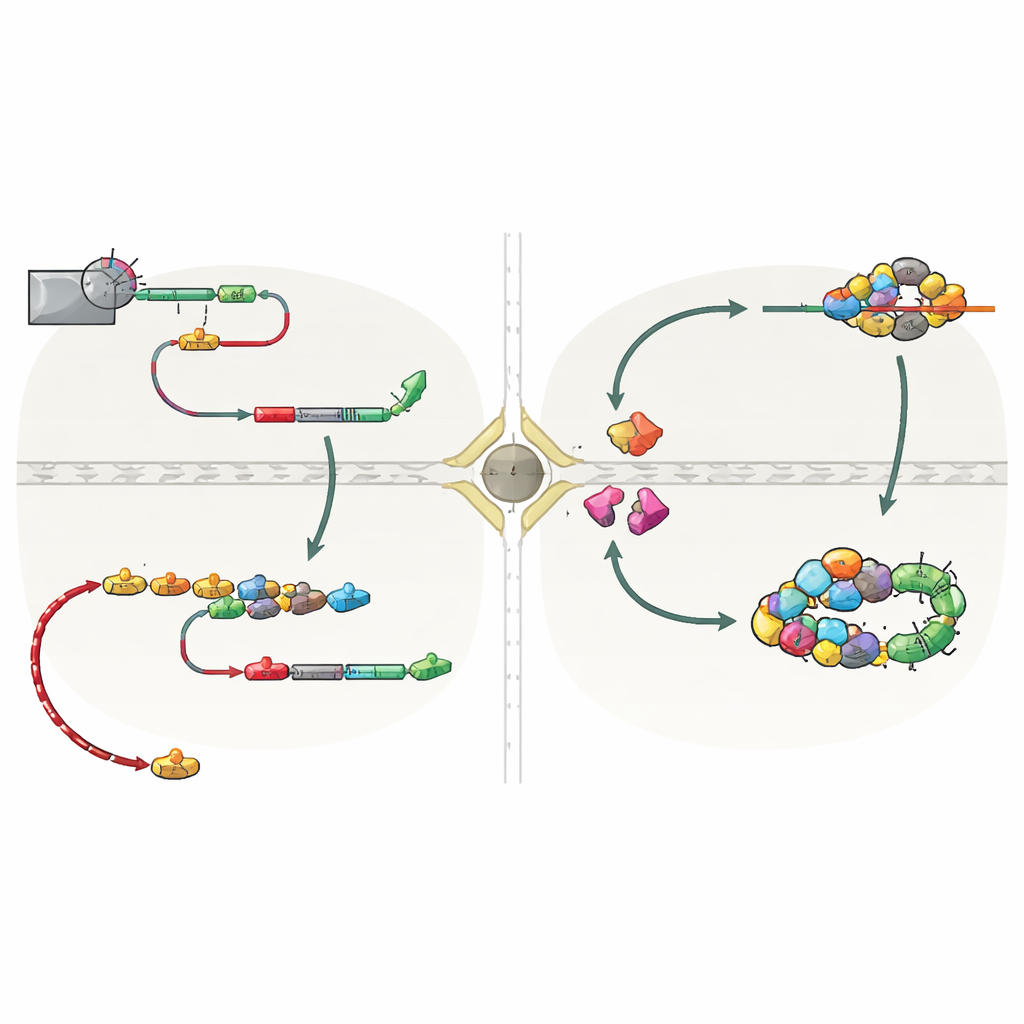
Warum dieser verborgene Weg wichtig ist
Diese Arbeit zeigt, dass snoRNA‑Reise kein Einzelfall ist, sondern eine eingebaute Backup‑Route, die von der Art der Transkriptionsbeendigung gesteuert wird. Wenn das primäre NNS‑System geschwächt ist — etwa in bestimmten Phasen des Zellzyklus — retten nachfolgende CPF‑CF‑Signale die snoRNA‑Produktion. Dies verhindert das Wegwerfen bereits synthetisierter RNA und vermeidet unkontrollierte Transkription, die benachbarte Gene stören und DNA schädigen könnte. Die Autor:innen finden zudem Hinweise auf ein ähnliches Backup auch in menschlichen Zellen, wo einzeln kodierte snoRNAs an verwandten Stellen Poly(A)‑Schwänze erwerben können. Vereinfacht gesagt zeigt die Studie, dass das am Ende eines snoRNA‑Gens gewählte „Stopp‑Signal“entscheidet, ob diese RNA still im Kern reift oder vorübergehend unter Aufsicht von Schutzproteinen hinaus- und zurückgeschickt wird. Dieser durch Transkriptions‑Terminierung gesteuerte Überwachungsmechanismus trägt dazu bei, die RNA‑Landschaft der Zelle zugleich flexibel und sicher zu halten.
Zitation: Yu, F., Zaccagnini, G., Duan, Y. et al. CPF-CF-terminated snoRNAs shuttle through the cytoplasm via an mRNA guard protein-mediated surveillance mechanism. Nat Commun 17, 2328 (2026). https://doi.org/10.1038/s41467-026-70373-8
Schlüsselwörter: snoRNA, RNA‑Qualitätskontrolle, nukleärer Export, Transkriptions‑Terminierung, Hefe‑Genetik