Clear Sky Science · de
Synchronisierte Aktivierung striataler cholinerger Interneurone induziert lokale Freisetzung von Serotonin
Warum diese Entdeckung der Hirnchemie wichtig ist
Gewohnheiten, Motivation und zwanghaftes Verhalten hängen alle von einer kleinen, aber wichtigen Hirnregion ab, dem Striatum. Zwei bekannte Botenstoffe, Dopamin und Serotonin, stimmen diese Region fein ab, und viele psychiatrische Medikamente zielen darauf ab, ihr Gleichgewicht zu verändern. Diese Studie zeigt eine zuvor verborgene Kommunikationslinie: Eine besondere Klasse von Nervenzellen, die Acetylcholin freisetzt, kann direkt an Serotoninfasern anknüpfen und deren Serotoninfreisetzung erhöhen — allerdings nur in einem bestimmten Teil des Striatums. Diese neu entdeckte Verbindung könnte erklären, warum Störungen wie die Zwangsstörung (OCD) und die Parkinson-Krankheit häufig verwobene Veränderungen mehrerer Neurochemikalien gleichzeitig zeigen.
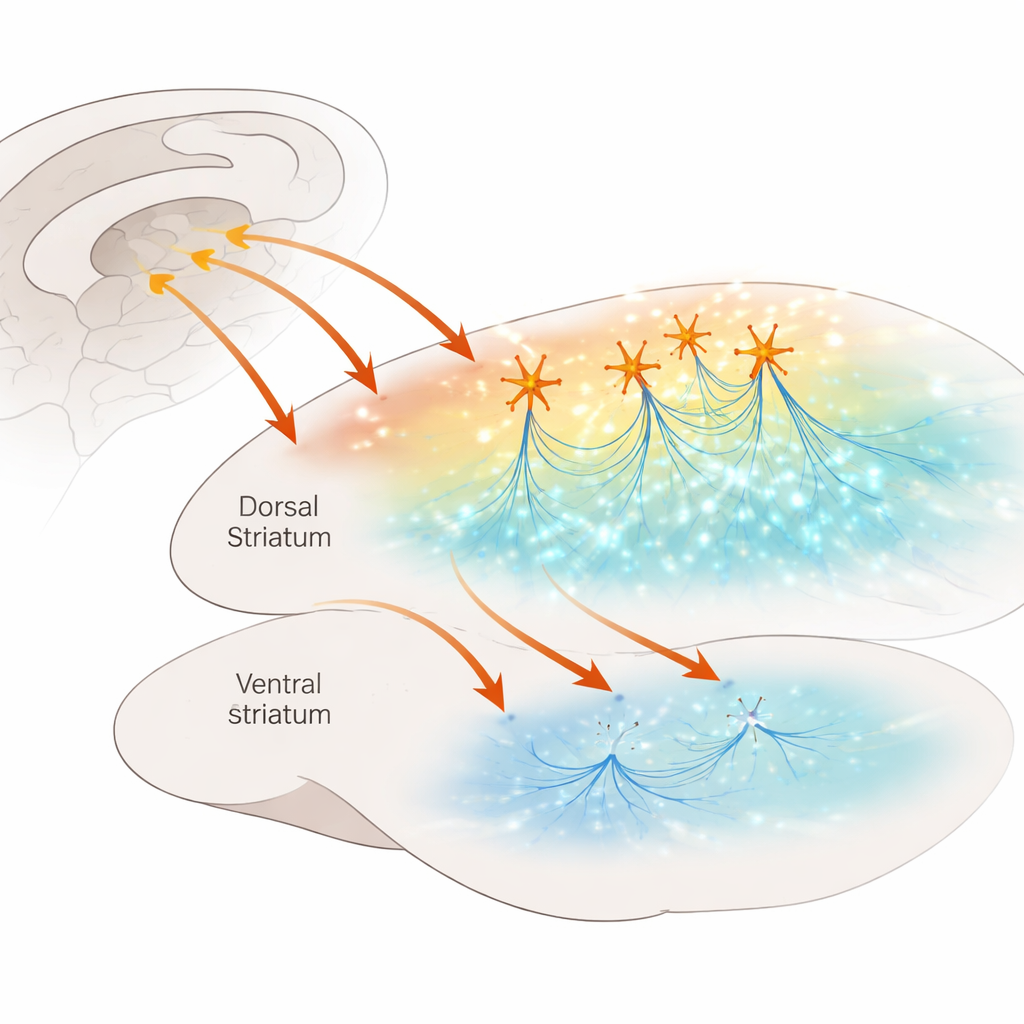
Ein geschäftiger Verkehrsknotenpunkt im Gehirn
Das dorsale Striatum fungiert als Entscheidungszentrum und hilft uns, zwischen zielgerichteten Handlungen und automatischen Gewohnheiten zu wechseln. Es erhält dichte Eingänge aus der Hirnrinde und ist von Neuromodulatoren wie Dopamin und Serotonin durchzogen, die steuern, wie Signale verarbeitet werden. Innerhalb dieses Zentrums gibt es eine spärliche, aber leistungsfähige Population cholinerger Interneurone — Zellen, die Acetylcholin freisetzen und regelmäßig wie kleine Metronome feuern. Frühere Arbeiten zeigten, dass diese Zellen bei synchroner Aktivität die Dopaminfreisetzung stark verstärken können, indem sie auf nikotinische Acetylcholinrezeptoren auf Dopaminfasern wirken. Ob es eine ähnliche Abkürzung für Serotonin gibt, war unbekannt, obwohl Serotonin zentral für Stimmung, Lernen und die Wirkung von Medikamenten gegen OCD und Depression ist.
Serotonin in Echtzeit beobachten
Um diese Frage zu untersuchen, verwendeten die Forschenden Mäuse, in denen ein fluoreszierender Sensor bei Anwesenheit von Serotonin heller leuchtet. Sie injizierten ein Virus, das diesen Sensor in das Striatum bringt, bereiteten dünne Hirnschnitte vor und nutzten dann Zwei-Photonen-Mikroskopie, um Serotoninsignale während gezielter Stimulation zu beobachten. Elektrische Stimulation im dorsalen Striatum löste deutliche, langsam abklingende Aufhellungen des Serotoninsensors aus. Als das Team ein Mittel anwandte, das nikotinische Acetylcholinrezeptoren blockiert, wurden diese Aufhellungen kleiner und räumlich begrenzter, was darauf hinweist, dass Acetylcholin über diese Rezeptoren sowohl die Serotoninfreisetzung erhöht als auch ihre Ausbreitung über einen größeren Bereich fördert. Auffällig war, dass dieselben Experimente im ventralen Striatum — einer angrenzenden Region mit noch dichterer Serotonin-Vernetzung — keinen solchen nikotinischen Beitrag zeigten; dies deutet darauf hin, dass diese Querverbindung regionsspezifisch ist.
Serotonin mit gezieltem Licht auslösen
Um herauszufinden, ob Acetylcholin aus cholinergen Interneuronen allein die Serotoninfreisetzung antreiben kann, setzten die Autorinnen und Autoren Optogenetik ein. Sie konstruierten diese Interneurone so, dass sie auf kurze Blitze blauen oder gelben Lichts reagieren, und aktivierten sie synchron, während sie den Serotoninsensor weiter überwachten. Ein einzelnes Millisekunden-Licht genügte, um im dorsalen Striatum ein robustes Serotoninsignal auszulösen, dessen Zeitverlauf dem nikotinisch-empfindlichen Anteil der elektrisch evozierten Antwort ähnelte. Die Blockade nikotinischer Rezeptoren beseitigte dieses Signal nahezu vollständig, selbst wenn andere chemische Eingänge und Rezeptoren in den Schnitten pharmakologisch ausgeschaltet waren. Diese Kombination aus präziser Stimulation und Rezeptorblockade zeigte, dass Acetylcholin direkt an nikotinischen Rezeptoren entlang der Serotoninfasern wirkt, um lokale Serotoninfreisetzung auszulösen, statt auf indirekte Wege über andere Zelltypen oder Dopaminaxone angewiesen zu sein.
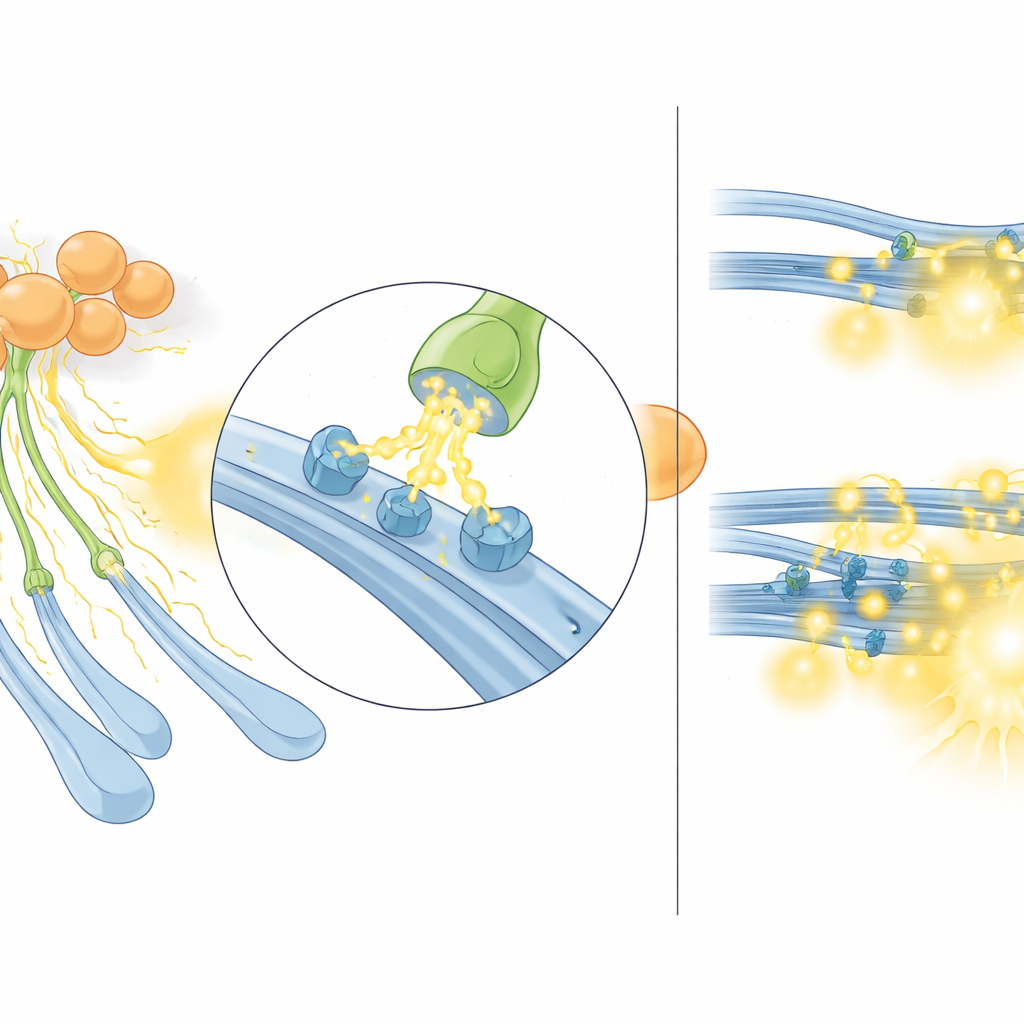
Wenn das System überhitzt
Als Nächstes fragte das Team, was in einem krankheitsrelevanten Zustand passiert, in dem die Acetylcholin-Signalgebung ungewöhnlich stark ist. Sie verwendeten Sapap3-Knockout-Mäuse, ein gut etabliertes Modell, das übermäßiges Putzen und andere OCD-ähnliche Verhaltensweisen zeigt und bei dem zuvor bereits aktivere cholinerge Interneurone und höhere Acetylcholinfreisetzung nachgewiesen wurden. Bei diesen Mäusen erzeugte elektrische Stimulation des dorsalen Striatums größere Signale des Serotoninsensors als in normalen Tieren. Wichtig war, dass dieser Unterschied verschwand, wenn nikotinische Rezeptoren blockiert wurden, was bedeutet, dass nur der acetylcholinabhängige Anteil der Serotoninfreisetzung erhöht war. Ein ähnliches Muster zeigte sich für Dopamin. Anders ausgedrückt: In diesem hypercholinergen Zustand verstärken cholinerge Interneurone den nikotinischen Anteil der Monoaminfreisetzung überproportional und lassen Acetylcholin effektiv Serotoninfasern als Hauptweg für Serotoninausgang „kapern“.
Breitere Implikationen für Hirnerkrankungen
Diese Befunde zeigen ein fein abgestimmtes und regional begrenztes Wechselspiel zwischen Acetylcholin und Serotonin im dorsalen Striatum. In gesunden Gehirnen können synchrone Bursts cholinerger Interneurone — etwa ausgelöst durch plötzliche, verhaltensrelevante Ereignisse — Serotoninsignale vorübergehend vergrößern und verstärken und so beeinflussen, wie Handlungen erlernt oder unterdrückt werden. In pathologischen Zuständen, in denen Acetylcholin dauerhaft erhöht ist, wie bei Sapap3-Knockout-Mäusen und möglicherweise bei Erkrankungen wie OCD oder Parkinson, kann derselbe Mechanismus übersteigert werden und zu abnormalen Mustern von Serotonin- und Dopamin-Signalen beitragen. Das Verständnis dieser verborgenen Verbindung eröffnet neue Denkwege dafür, wie mehrere Neuromodulatoren im normalen Verhalten und bei Krankheiten interagieren, und könnte schließlich auf Behandlungen hinweisen, die ihre gemeinsame Dynamik gezielter ansprechen, anstatt jeden Botenstoff isoliert zu behandeln.
Zitation: Matityahu, L., Hobel, Z.B., Berkowitz, N. et al. Synchronous activation of striatal cholinergic interneurons induces local serotonin release. Nat Commun 17, 2278 (2026). https://doi.org/10.1038/s41467-026-70359-6
Schlüsselwörter: striataler Serotonin, cholinerge Interneurone, nikotinische Acetylcholinrezeptoren, Zwangsstörung, Basalganglien