Clear Sky Science · de
siRNA-Nanopartikel, die auf Tudor-Domain-enthaltendes Protein 9 abzielen, mildern Pseudomonas aeruginosa-Lungenschäden in präklinischen Modellen, indem sie die Cuproptose von Neutrophilen fördern
Die Ersthelfer des Körpers zu präzisen Verbündeten machen
Durch das Bakterium Pseudomonas aeruginosa verursachte Pneumonien sind besonders schwer zu behandeln, vor allem bei Menschen mit geschwächtem Immunsystem oder geschädigten Lungen. Diese Studie untersucht einen neuen Ansatz, mit dem die körpereigenen Immunzellen, die sogenannten Neutrophilen, Infektionen sicherer und effektiver beseitigt werden können. Mittels winziger genetischer Stränge, die in speziell entworfenen Nanopartikeln ausgeliefert werden, programmieren die Forschenden Neutrophile so um, dass sie zur richtigen Zeit und am richtigen Ort absterben — was Lungenschäden reduziert und gleichzeitig die Bekämpfung der Bakterien aufrechterhält.
Warum dieses Bakterium so schwer zu bezwingen ist
Pseudomonas aeruginosa ist ein hoch anpassungsfähiger Erreger, der vielen Antibiotika widerstehen und schützende Biofilme bilden kann, wodurch Lungeninfektionen schwer kontrollierbar werden. Als Reaktion darauf rekrutiert der Körper große Mengen an Neutrophilen, weiße Blutkörperchen, die als Ersthelfer agieren. Obwohl sie für das Abtöten von Keimen essenziell sind, kann ein Übermaß an Neutrophilen — insbesondere wenn sie verzögert aus der Lunge entfernt werden — kontraproduktiv sein und Schwellungen, Flüssigkeitsansammlungen und Gewebeschäden verursachen. Aktuelle Therapien richten sich meist darauf, die Bakterien direkt anzugreifen, und bieten nur wenige Möglichkeiten, die Immunantwort selbst sicher zu modulieren.
Ein überraschendes Gen in Neutrophilen
Das Team begann mit der Untersuchung von Neutrophilen, die aus Lungenflüssigkeit von Patienten mit Pneumonie gewonnen wurden, und verglich Proben von Pseudomonas-Infektionen mit anderen Pneumonien oder keinen Pneumonien. Durch RNA-Sequenzierung entdeckten sie, dass ein Gen namens TDRD9 in Neutrophilen von Pseudomonas-Patienten stark hochreguliert war. TDRD9 war zuvor vor allem für Funktionen bei der Spermienentwicklung bekannt, nicht für Lungenerkrankungen, dennoch zeigten sowohl menschliche Proben als auch infizierte Mäuse konsistent erhöhte Werte. Das deutet darauf hin, dass TDRD9 schädliches Verhalten von Neutrophilen während schwerer bakterieller Lungeninfektionen antreiben könnte.
Den Zelltod der Neutrophilen für die Heilung nutzbar machen
Neutrophile sterben normalerweise kontrolliert ab, nachdem sie ihre Aufgabe erfüllt haben, sodass sich die Entzündung zurückbildet. Die Forschenden konzentrierten sich auf eine neu erkannte Form des Zelltods, die Cuproptose, die von intrazellulärem Kupfer abhängt. In Mäusen und menschlichen Neutrophilen, die mit Pseudomonas infiziert waren, fanden sie, dass TDRD9 die Neutrophilen vor Cuproptose schützte und sie in der entzündeten Lunge länger am Leben hielt. Wurde TDRD9 gezielt reduziert, waren die Neutrophilen anfälliger für diesen kupferabhängigen Tod und die Lungenläsionen verbesserten sich insgesamt: Es gab weniger Flüssigkeit in den Lungen, geringere Mengen entzündlicher Moleküle und reduzierte Bakterienzahlen. Mechanistische Experimente zeigten, dass TDRD9 über eine Signalkette wirkt, die Proteine wie PD-L1, CD80 und den p38-MAPK-Weg einbezieht — einen bekannten Regulator zellulärer Stressreaktionen.
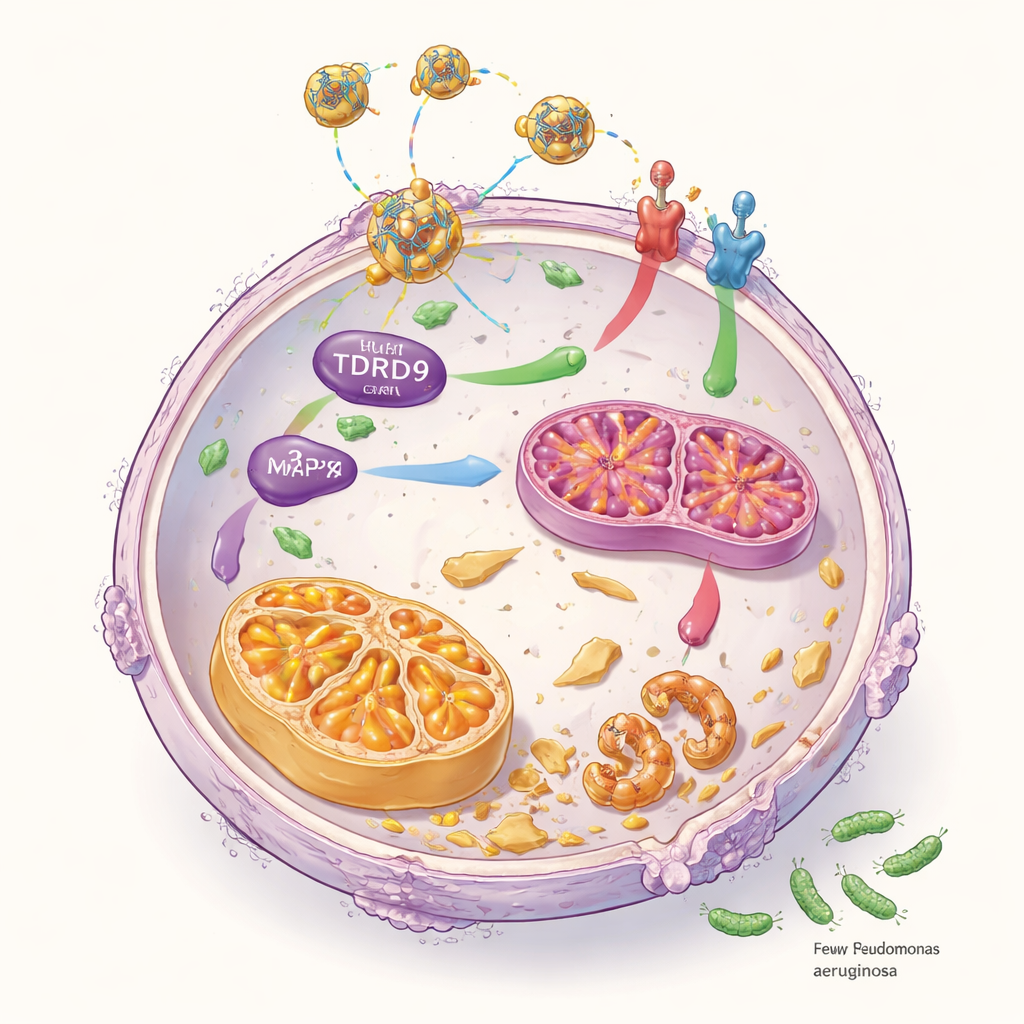
Intelligente Nanopartikel zur gezielten Genstilllegung
Um diese Erkenntnisse in eine potenzielle Therapie zu überführen, entwickelten die Wissenschaftler ein Abgabesystem auf Basis von Nanopartikeln, die mit Hyaluronsäure beschichtet sind — einem Zucker, der ihnen hilft, über den Oberflächenrezeptor CD44 spezifisch die Neutrophilen anzusteuern. In jedem Nanopartikel ist eine kleine interferierende RNA (siRNA) verpackt, die gezielt TDRD9 blockiert. In Labortests wurden diese Partikel gut von menschlichen Neutrophilen aufgenommen und senkten TDRD9 effektiv. Bei infizierten Mäusen reduzierte eine intravenöse Behandlung mit den auf TDRD9 ausgerichteten Nanopartikeln die bakterielle Belastung, die Lungenschwellung und entzündliche Marker, ohne nachweisbare Leber- oder Nierentoxizität. Die Neutrophilen zeigten Veränderungen, die mit verstärkter Cuproptose und einer beruhigteren Entzündungsumgebung vereinbar sind.
Menschlichere Lungen ins Labor bringen
Um die Lücke zwischen Tiermodellen und menschlicher Erkrankung zu überbrücken, züchtete das Team zudem dreidimensionale menschliche Lungenorganoide — winzige, gewebeähnliche Strukturen, die aus nicht‑tumorigem Lungengewebe gewonnen wurden. Bei Exposition gegenüber Pseudomonas zeigten diese Organoide strukturelle Schäden, Entzündung und Zelltod. Die Behandlung mit TDRD9‑zielenden Nanopartikeln bremste das bakterielle Wachstum, senkte entzündliche Moleküle und verringerte Anzeichen von Zelltod, was darauf hindeutet, dass der Ansatz menschliches Lungengewebe vor infektionsbedingten Schäden schützen könnte.
Was das für Patientinnen und Patienten bedeuten könnte
Insgesamt zeigt die Studie, dass das Dämpfen des TDRD9‑Wegs in Neutrophilen durch präzise gelieferte siRNA‑Nanopartikel eine kontrollierte Form des Zelltods fördern kann, die überschüssige Neutrophile beseitigt und Lungenschäden bei schweren Pseudomonas-Infektionen lindert. Statt die Bakterien lediglich mit mehr Antibiotika anzugreifen, verfeinert diese Strategie die Immunantwort selbst. Zwar sind weitere Untersuchungen nötig, um Langzeitsicherheit und Wirksamkeit beim Menschen zu bestätigen, doch die Ergebnisse weisen in Richtung einer Zukunft, in der intelligente Nanopartikel übervorsichtige Immunzellen von Schadensquellen in Partner der Heilung verwandeln.
Zitation: Zhang, W., Li, H., Jia, H. et al. Tudor domain-containing protein 9-targeting siRNA nanoparticles alleviate Pseudomonas aeruginosa lung injury in preclinical models by promoting neutrophil cuproptosis. Nat Commun 17, 2277 (2026). https://doi.org/10.1038/s41467-026-70349-8
Schlüsselwörter: Pseudomonas aeruginosa Pneumonie, Neutrophile, Nanopartikeltherapie, siRNA-Abgabe, Cuproptose