Clear Sky Science · de
Steuerung der Lysosomenfunktion durch das GTPase‑aktivierende Protein TBC1D9B und seinen Bindungspartner TMEM55B
Wie die Recycling‑Zentren der Zelle das Gleichgewicht halten
In jeder unserer Zellen befinden sich winzige Bläschen, sogenannte Lysosomen, die wie Recycling‑Zentren und Steuerzentralen für Wachstum fungieren. Arbeiten sie richtig, werden verschlissene Teile abgebaut und ihre Bestandteile wiederverwendet; versagen sie, häufen sich Abfälle und es können Krankheiten entstehen, darunter Neurodegeneration und Krebs. Diese Studie zeigt, wie zwei wenig bekannte Proteine dabei helfen, Lysosomen zwischen einem umherwandernden, wachstumsfreundlichen Zustand und einem zusammengezogenen, abfallverarbeitenden Modus umzuschalten, und beleuchtet, wie Zellen sich an Überfluss und Mangel anpassen.
Die Recycling‑Zentren im Zellinneren verschieben
Lysosomen sind nicht fest verankert. Sie bewegen sich entlang innerer Schienen, nach außen gezogen von einem Satz molekularer Motoren und nach innen gezogen von einem anderen. Ihr Standort in der Zelle ist bedeutsam: Bei reichlich vorhandenen Nährstoffen verteilen sich Lysosomen in Richtung Zellperipherie und unterstützen Wachstumssignale; bei Nahrungsmangel ziehen sie sich zur Zellmitte zurück, werden saurer und steigern den Abbau von Zellmaterial. Ein kleines schalterähnliches Protein namens ARL8 ist dafür bekannt, Lysosomen nach außen zu treiben, doch bisher war kein dediziertes Bremssystem identifiziert, das dieses Vorankommen drosselt. Die Autoren vermuteten, dass eine solche Bremse entscheidend wäre, damit Zellen bei Hungersituationen schnell in einen Sparmodus umschalten können.
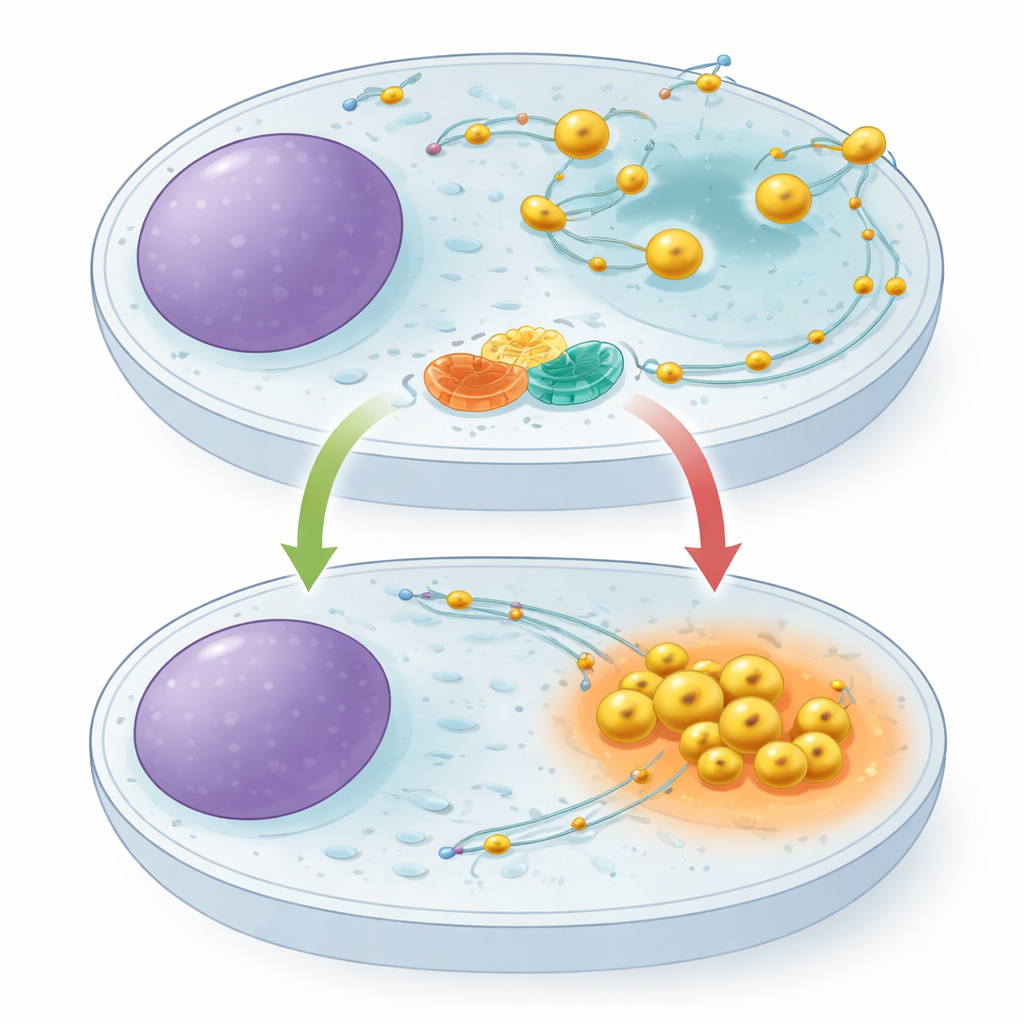
Eine molekulare Partnerschaft an der Lysosomenoberfläche
Mit Methoden zum "Protein‑Fischen" und Massenspektrometrie entdeckten die Forscher, dass ein Protein namens TBC1D9B an ein lysosomales Membranprotein namens TMEM55B bindet. TMEM55B sitzt quer durch die äußere Hülle des Lysosoms, während TBC1D9B überwiegend löslich ist und an die Membran andocken kann. Das Team zeigte, dass diese beiden einen direkten Komplex bilden: gereinigtes TBC1D9B bindet im Reagenzglas an den exponierten Teil von TMEM55B, und markierte Versionen der Proteine ziehen sich gegenseitig aus Zellextrakten. Sorgfältige Kartierung von Proteinsegmenten ergab, dass mehrere Bereiche von TBC1D9B Kontakt zu TMEM55B haben und TBC1D9B an der Lysosomenoberfläche positionieren, ohne den Teil des Proteins zu blockieren, der für seine katalytische Aktivität verantwortlich ist.
Wenn die Bremse ausfällt, laufen Lysosomen Amok
Um herauszufinden, was diese Partnerschaft bewirkt, entfernten die Autoren mittels CRISPR‑Editing entweder TMEM55B oder TBC1D9B aus menschlichen Zellen. In beiden Fällen gruppierten sich Lysosomen nicht länger in der Nähe des Zellkerns, sondern streuten zur Zellperipherie und bewegten sich schneller entlang ihrer Schienen – ein Bild, das Zellen im dauerhaft gefütterten Zustand ähnelt. Die Wiedereinführung von normalem TBC1D9B stellte die richtige Positionierung wieder her, eine Version ohne katalytische Funktion jedoch nicht, was darauf hindeutet, dass seine enzymatische Aktivität wesentlich ist. Bei Hunger zogen Kontrollzellen ihre Lysosomen nach innen und steigerten deren Verdauungskraft, nachgewiesen durch erhöhte Aktivität wichtiger Enzyme und verstärkten Abbau testweise zugeführter Fracht. Zellen ohne TMEM55B oder TBC1D9B konnten dies nicht: Ihre Lysosomen blieben peripher und ihre degradative Reaktion auf Nahrungsentzug war abgeschwächt. Auch die Autophagie, der Prozess, mit dem Zellen beschädigte Komponenten selbst verdauen, war beeinträchtigt, mit weniger effizienter Verarbeitung eines Autophagie‑Reporters und Akkumulation des Adapterproteins p62.
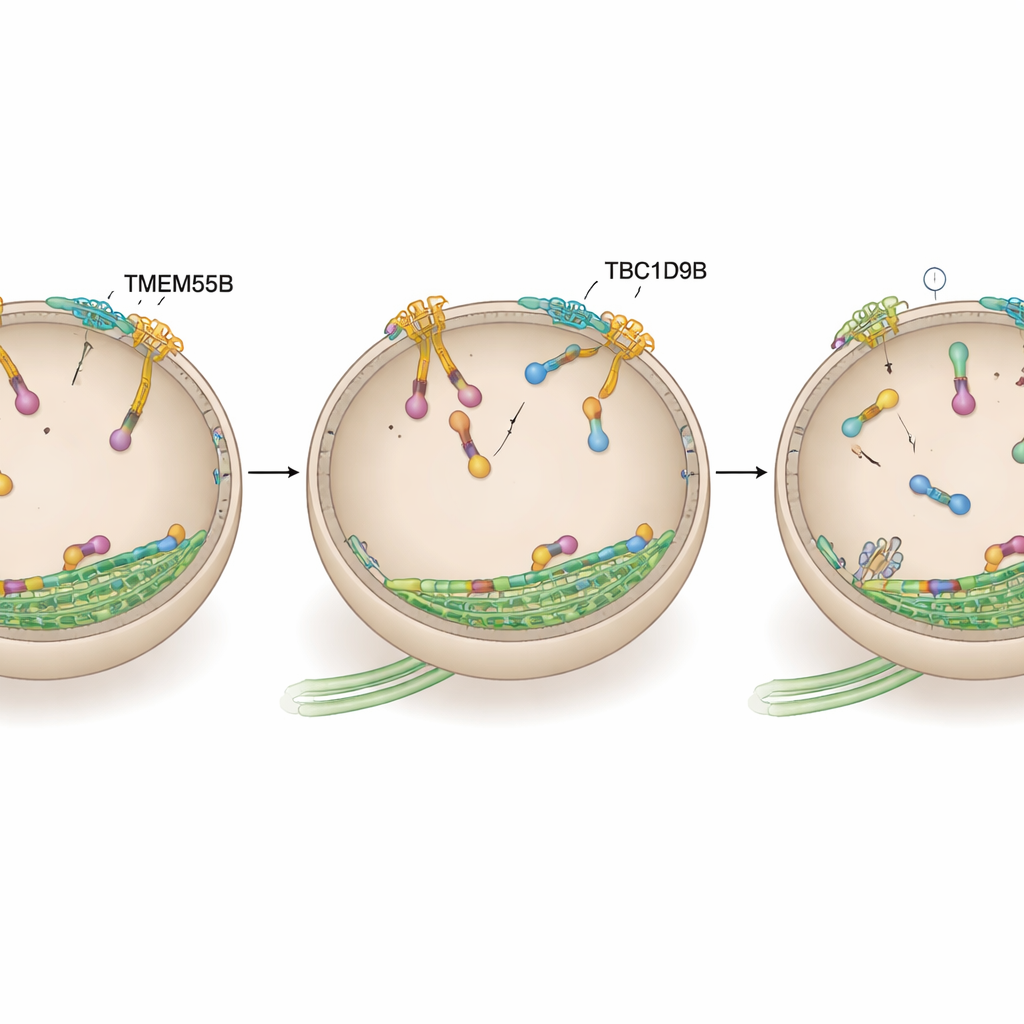
Den Lysosomenmotor ausschalten
Das Team prüfte dann, ob TBC1D9B seine Wirkung ausübt, indem es direkt auf ARL8 einwirkt, den Motor‑Schalter für die Außenbewegung. Mithilfe von Proximity‑Labeling in menschlichen Neuronen sowie Bindungstests in Zelllinien und mit gereinigten Proteinen zeigten sie, dass TBC1D9B selektiv an die aktive, GTP‑beladene Form der ARL8B‑Variante bindet, nicht jedoch an deren inaktive Form oder an das eng verwandte ARL8A. Strukturmodellierung sagte voraus, dass Schlüsselreste in TBC1D9B die GTP‑Tasche von ARL8B kontaktieren. In biochemischen Assays beschleunigte TBC1D9B die Hydrolyse von an ARL8B gebundenem GTP und schaltete das Protein damit effektiv vom "an" in den "aus"‑Zustand um; eine mutierte TBC1D9B‑Variante ohne diese Reste konnte dies nicht. Konsistent damit zeigten Zellen ohne TMEM55B oder TBC1D9B vermehrtes ARL8B an Lysosomen, während Überexpression von TBC1D9B Lysosomen zur Zellmitte zurückzog, ähnlich wie eine Herunterregulierung der ARL8B‑Aktivität.
Ein neuer Stellknopf für die zelluläre Haushaltsführung
Schließlich testeten die Autoren, ob diese ARL8B‑Bremse die beobachteten zellulären Veränderungen bei fehlendem TBC1D9B erklärt. Wurde ARL8B reduziert, blieben Lysosomen unabhängig vom Vorhandensein von TMEM55B oder TBC1D9B in der Nähe des Zellkerns gehäuft, und die durch den Verlust von TBC1D9B verursachten Autophagie‑Defekte wurden weitgehend aufgehoben. Insgesamt stützen die Daten ein Modell, in dem TMEM55B TBC1D9B zu Lysosomen rekrutiert, wo es ARL8B inaktiviert und Lysosomen den Wechsel von einem dispergierten, wachstumsfördernden Zustand zu einem zentralisierten, auf Verdauung ausgerichteten Zustand ermöglicht. Für Nicht‑Spezialisten bedeutet dies, dass die Studie einen wichtigen Drehregler aufgedeckt hat, den Zellen nutzen, um zu entscheiden, wann sie aggressiver recyceln – ein Prozess mit Implikationen für Erkrankungen, die mit Abfallansammlungen im Gehirn, dem Stoffwechsel und Krebs zusammenhängen.
Zitation: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
Schlüsselwörter: Lysosomen, Autophagie, Zell‑Signalübertragung, Organelltransport, Neurodegeneration