Clear Sky Science · de
SLIT3-Fragmente orchestrieren neurovaskuläre Ausdehnung und Thermogenese im braunen Fettgewebe
Wie unser „gutes Fett“ uns warm hält
Wenn wir in die Kälte treten, arbeitet unser Körper schnell daran, uns warm zu halten. Ein zentraler Akteur in dieser Reaktion ist braunes Fett, eine spezielle Fettform, die Kalorien verbrennt, um Wärme zu erzeugen. Diese Studie zeigt, wie braunes Fett seine feinen Blutgefäße und Nervenfasern organisiert, um die Wärmeproduktion zu steigern, und legt ein verborgenes Kommunikationssystem offen, das eines Tages zur Verbesserung des Stoffwechsels und zur Behandlung von adipositasbedingten Erkrankungen genutzt werden könnte.
Ein versteckter Ofen im Körper
Das braune Fettgewebe funktioniert wie ein innerer Ofen. Anders als das weiße Fett, das Energie speichert, verbraucht braunes Fett Brennstoff, um bei Kälteeinwirkung Wärme zu erzeugen. Damit das effizient gelingt, benötigen braune Fettzellen eine reiche Blutversorgung für Sauerstoff und Nährstoffe sowie ein dichtes Netz sympathischer Nerven, die signalisieren, wann die Temperatur erhöht werden soll. Bei Kälte erweitern sich diese Gefäße und Nerven bemerkenswert. Bislang war jedoch unklar, wie diese verschiedenen Bestandteile des Gewebes ihr Wachstum so präzise koordinieren.
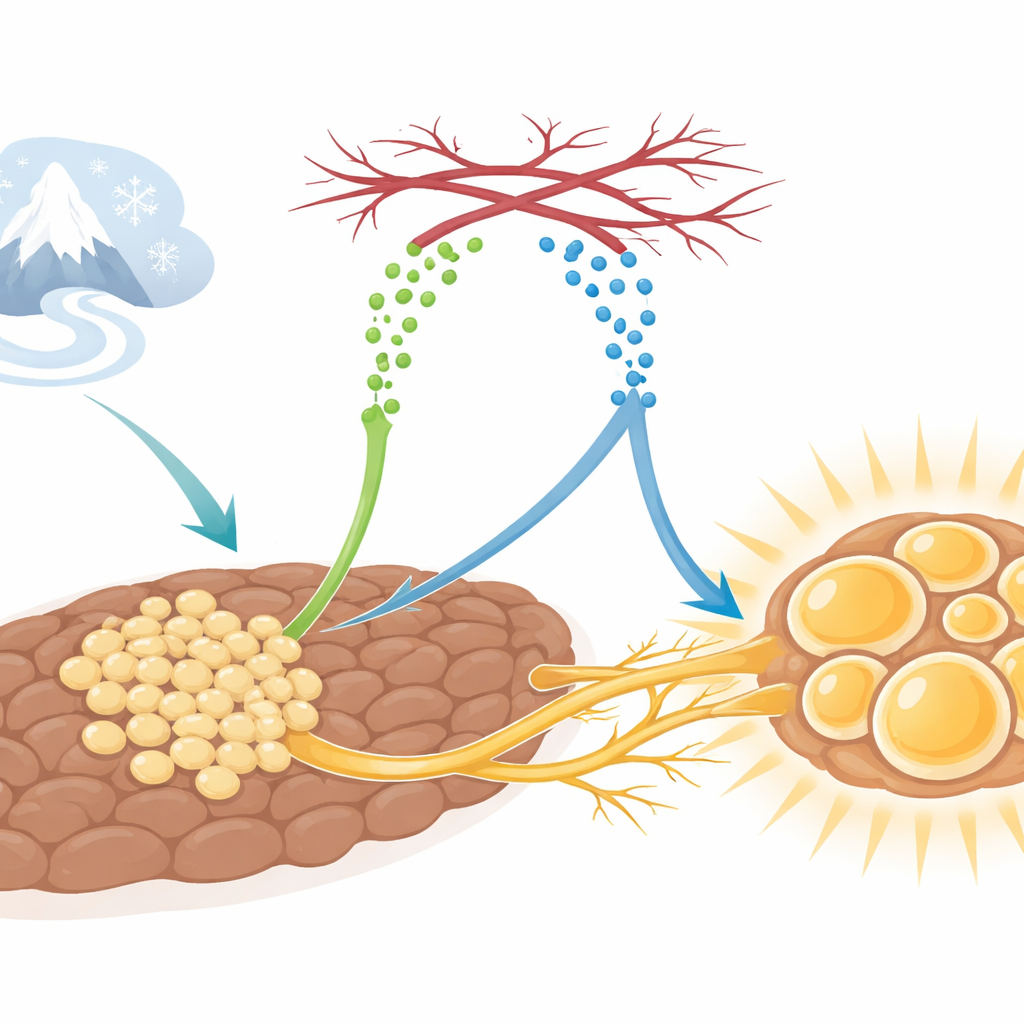
Das Botenmolekül, das alles in Gang setzt
Die Forschenden entdeckten, dass ein Protein namens SLIT3, das von unreifen Fettzellen, den Adipozytenprogenitoren, produziert wird, zentral für diese Koordination ist. Bei Mäusen, die Kälte ausgesetzt waren, stiegen die SLIT3-Spiegel im braunen Fett an. Wurde SLIT3 gezielt im braunen Fett oder in diesen Progenitorzellen blockiert, hatten die Tiere Schwierigkeiten, bei Kälte die Körpertemperatur zu halten. Ihr braunes Fett wurde „weißer“, mit größeren Fetttropfen, geringerer Expression von wärmeerzeugenden Genen wie Ucp1 und vermindertem Energieverbrauch, obwohl Nahrungsaufnahme und Aktivitätsniveau unverändert blieben. Das deutet darauf hin, dass SLIT3 ein zentraler Organisator der Kältereaktion des braunen Fettes ist — nicht durch Veränderung der zellulären Maschinerie selbst, sondern durch Gestaltung der umgebenden Gewebsumgebung.
Aufbau von Blutgefäßen und Nervenleitungen im Zusammenspiel
Bei genauerer Betrachtung stellten die Wissenschaftler fest, dass braunes Fett ohne SLIT3 weniger kleine Blutgefäße und weniger sympathische Nervenfasern aufwies, die sich durchs Gewebe zogen. 3D-Bildgebung bestätigte, dass das Nervennetz deutlich dünner war. Wichtig ist, dass die Fettzellen normal reagierten, wenn das übliche Nervensignal mit einem Wirkstoff umgangen wurde, der braunes Fett direkt aktiviert. Das zeigte, dass SLIT3 nicht notwendig ist, damit die Fettzellen Brennstoff verbrennen, wohl aber für den Aufbau der neurovaskulären „Verdrahtung“, die dem Gehirn die Kontrolle ermöglicht. Das Team identifizierte Adipozytenprogenitoren als die wichtigste lokale Quelle von SLIT3 und zeigte, dass das Entfernen von SLIT3 nur in diesen Zellen ausreichte, um Gefäßwachstum, Nervenausbildung und Wärmeerzeugung bei Kälteeinwirkung zu dämpfen.
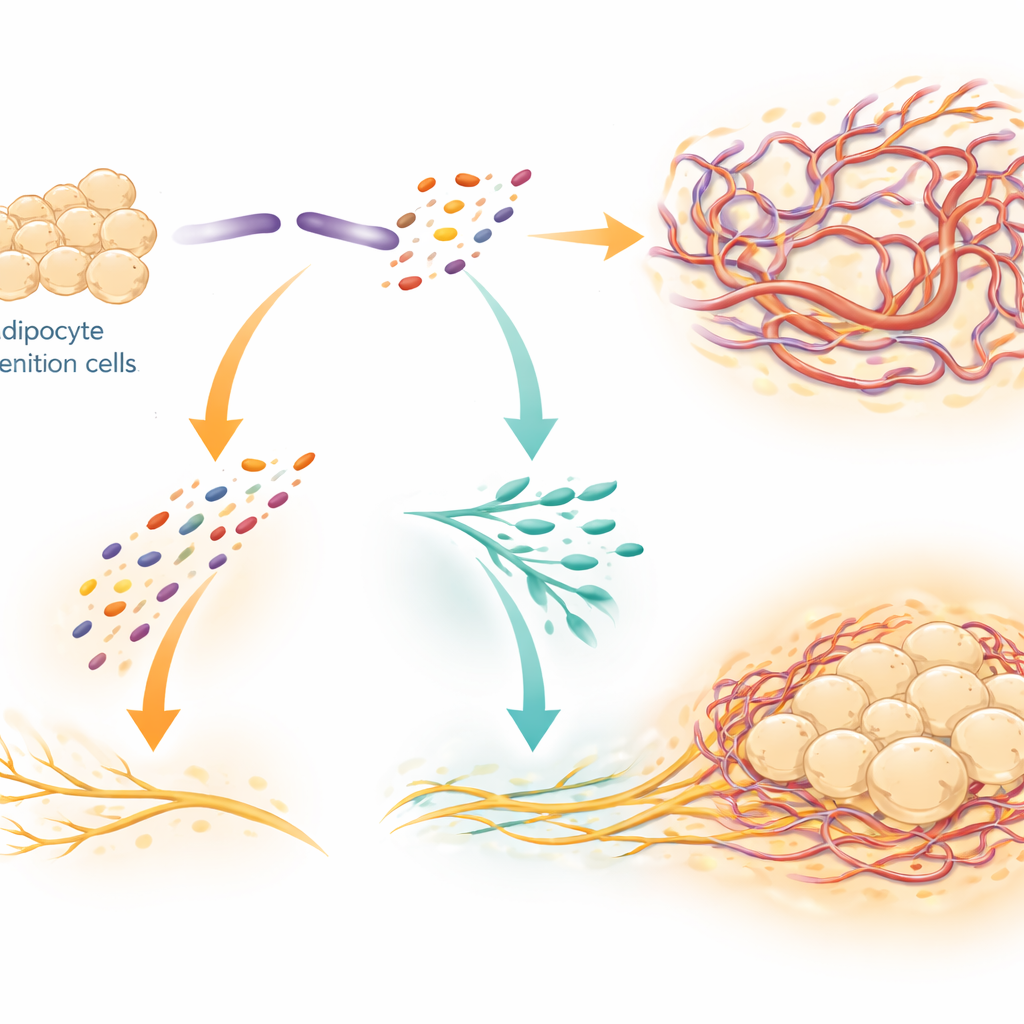
Ein Protein, zwei Fragmente, zwei Aufgaben
SLIT3 wirkt nicht als ein einzelnes, statisches Signal. Die Forschenden zeigten, dass ein Enzym namens BMP1 SLIT3 in zwei separate Fragmente schneidet, die unterschiedliche Rollen haben. Das N-terminale Fragment (SLIT3-N) stimuliert hauptsächlich das Wachstum von Kapillaren und wirkt über Rezeptoren auf Endothelzellen, die Blutgefäße auskleiden. Das C-terminale Fragment (SLIT3-C) fördert vor allem die Ausdehnung sympathischer Nerven. Sie identifizierten einen Rezeptor namens PLXNA1 auf Nervenfasern als direkten Andockpartner für SLIT3-C, gestützt durch biochemische Bindungstests und computerbasierte Strukturmodelle. Bei Reduktion von PLXNA1 ging die Fähigkeit von SLIT3 oder SLIT3-C verloren, das Nervwachstum zu fördern und die Temperatur des braunen Fettes zu erhöhen; die Nervendichte und die Norepinephrinkonzentration im Gewebe sanken deutlich.
Bezüge zum menschlichen Stoffwechsel und zur Gesundheit
Um zu prüfen, ob dieses System beim Menschen relevant ist, analysierten die Autorinnen und Autoren Fettproben aus großen Adipositas-Kohorten. Höhere SLIT3-Expression im Fettgewebe war mit gesünderen Profilen verbunden: mehr des Hormons Adiponektin, weniger entzündliche Immunzellen im viszeralen Fett, bessere Blutzuckerkontrolle und höhere Werte des vorteilhaften Adipokins Omentin. Genetische Studien aus anderen Arbeiten haben Varianten nahe SLIT3 und dessen Rezeptor PLXNA1 ebenfalls mit Adipositas und Insulinresistenz in Verbindung gebracht. Zusammengenommen deuten diese Befunde darauf hin, dass der SLIT3-Weg beim Menschen zur Erhaltung gesunden Fettgewebes und metabolischen Gleichgewichts beitragen könnte.
Was das für Wärme und Gesundheit bedeutet
Insgesamt zeigt die Studie, dass unreife Fettzellen im braunen Fett mehr tun, als nur zu reifen Fettzellen zu werden; sie formen aktiv das Unterstützungsnetzwerk des Gewebes. Indem sie SLIT3 freisetzen und dessen Aufspaltung in zwei Fragmente zulassen, treiben sie unabhängig voneinander, aber synchron das Wachstum von Blutgefäßen und Nerven an, das für effektive Wärmeerzeugung nötig ist. Dieses fein abgestimmte „Zwei-in-eins“-Signalsystem stellt sicher, dass braunes Fett bei Bedarf rasch hochgefahren werden kann. Langfristig könnte das Verständnis und die sichere Nutzung dieses Weges neue Ansätze eröffnen, um die Energieverbrennung zu steigern, die Gesundheit des Fettgewebes zu verbessern und metabolische Erkrankungen zu bekämpfen.
Zitation: Serdan, T.D.A., Cervantes, H., Frank, B. et al. SLIT3 fragments orchestrate neurovascular expansion and thermogenesis in brown adipose tissue. Nat Commun 17, 2445 (2026). https://doi.org/10.1038/s41467-026-70310-9
Schlüsselwörter: braunes Fettgewebe, Thermogenese, neurovaskuläres Remodeling, SLIT3-Signalgebung, metabolische Gesundheit