Clear Sky Science · de
NF-κB-Aktivierung in Astrozyten beeinträchtigt die Wundheilung nach traumatischer Hirnverletzung bei männlichen Mäusen
Warum Gehirnprellungen nicht immer sauber heilen
Wenn jemand einen Schlag auf den Kopf erleidet, ist die äußerlich sichtbare Verletzung nur ein Teil der Geschichte. Tief im Inneren des Gehirns läuft eine komplexe Heilungsreaktion ab, die darüber entscheiden kann, ob eine Person sich gut erholt oder langfristige Probleme mit Denken, Stimmung oder Bewegung entwickelt. Diese Studie an männlichen Mäusen zeigt, wie ein wichtiger Stressweg in Stützzellen, den sogenannten Astrozyten, eine normale Heilungsantwort in eine solche verwandeln kann, die den Schaden nach einer traumatischen Hirnverletzung tatsächlich verschlimmert.
Die verborgenen Ersthelfer des Gehirns
Astrozyten sind sternförmige Zellen, die Nervenzellen und Blutgefäße umgeben und zur Stabilität des inneren Hirnmilieus beitragen. Nach einer Kopfverletzung verändern sie schnell ihre Form und ihr Verhalten, bilden eine Barriere um den geschädigten Bereich und helfen beim Wiederaufbau von Gewebe. Die Forscher konzentrierten sich auf einen molekularen Schalter in diesen Zellen, NF-κB, der dafür bekannt ist, Entzündungsprozesse in vielen Geweben zu steuern. Sie untersuchten, ob dieser Schalter nach einer geschlossen-kopf-Verletzung — ähnlich gängigen menschlichen Gehirnerschütterungen und Prellungen — der Heilung des Gehirns eher nutzt oder schadet.
Ein Stressschalter, der nach dem Aufprall anspringt
Durch die Analyse der Genaktivität in Hirngewebe von Mäusen nach der Verletzung stellte das Team eine Zunahme von Genen fest, die mit Entzündung und NF-κB-Signalgebung verknüpft sind, insbesondere drei bis sieben Tage nach dem Trauma, wenn sich sekundäre Schäden verstärken. Mithilfe von Reporter-Mäusen zeigten sie, dass die NF-κB-Aktivierung nicht gleichmäßig im Gehirn verteilt war, sondern sich um die Einschlagstelle konzentrierte. Dort war sie besonders in Mikroglia (den Immunwachposten des Gehirns) und in Astrozyten aktiv, die die Wundgrenze bildeten. Dieses Timing und diese Lokalisation deuteten darauf hin, dass NF-κB in Astrozyten ein entscheidender Regulator dafür sein könnte, wie das Gehirn seine Narbe organisiert und die Immunantwort steuert.
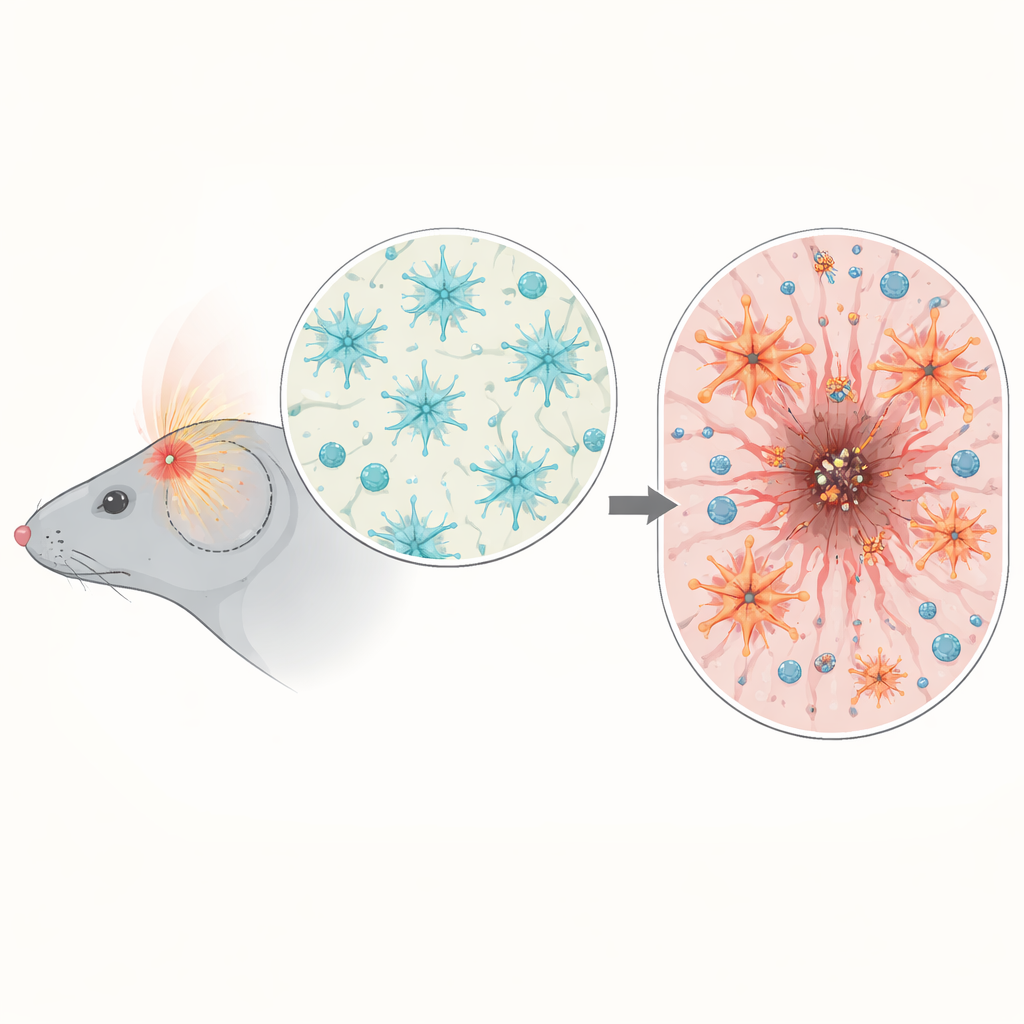
Astrozyten, die zu stark aktiviert sind
Um Ursache und Wirkung zu prüfen, erzeugten die Wissenschaftler Mäuse, bei denen die NF-κB-Aktivität in Astrozyten entweder künstlich erhöht oder gedämpft war — jedoch erst nach Abschluss der Gehirnentwicklung. Nach einer Kopfverletzung verloren Mäuse mit überaktiver NF-κB in Astrozyten mehr Gewicht, zeigten schlechtere frühe neurologische Scores und hatten größere, hartnäckigere Hirnläsionen sowohl in Gewebeschnitten als auch in MRT-Aufnahmen. Anstatt eine saubere, gut definierte Narbe zu bilden, die den geschädigten Kern abgrenzt, produzierten ihre Astrozyten eine dicke, ungeordnete Grenzschicht, die die Wunde im Zeitverlauf nicht verkleinerte. Das normale Gleichgewicht der umgebenden Matrixproteine war gestört, und eine wichtige äußere Barrierestruktur — das gliale Limitans — bildete sich schlecht, sodass das umliegende Gehirn weniger geschützt blieb.
Wenn Heilungsprogramme aus dem Takt geraten
Auf molekularer Ebene isolierte das Team Astrozyten und nahegelegene Immunzellen zur genauen Analyse. Bei gesunden Tieren unterdrückt eine Verletzung normalerweise einige alltägliche Hausmeisterfunktionen von Astrozyten und schaltet gleichzeitig Gene an, die Wundverschluss und Regeneration unterstützen. Im Gegensatz dazu sahen Astrozyten mit chronisch aktivem NF-κB bereits vor dem Trauma „verletzter“ aus, und nach dem Aufprall gelang es ihnen nicht, vorteilhafte Reparaturprogramme vollständig zu aktivieren — etwa solche, die mit einer kontrollierten Umwandlung verbunden sind, die Zellen hilft, eine effektive Grenze zu bilden. Stattdessen bevorzugten sie stark entzündliche Gene, nahmen Merkmale eines toxischen Astrozytenzustands an, wie er mit Alterung und neurodegenerativen Erkrankungen verbunden ist, und zeigten Anzeichen eines seneszenzähnlichen sekretorischen Profils, das mit chronischen, nicht abklingenden Wunden einhergeht.
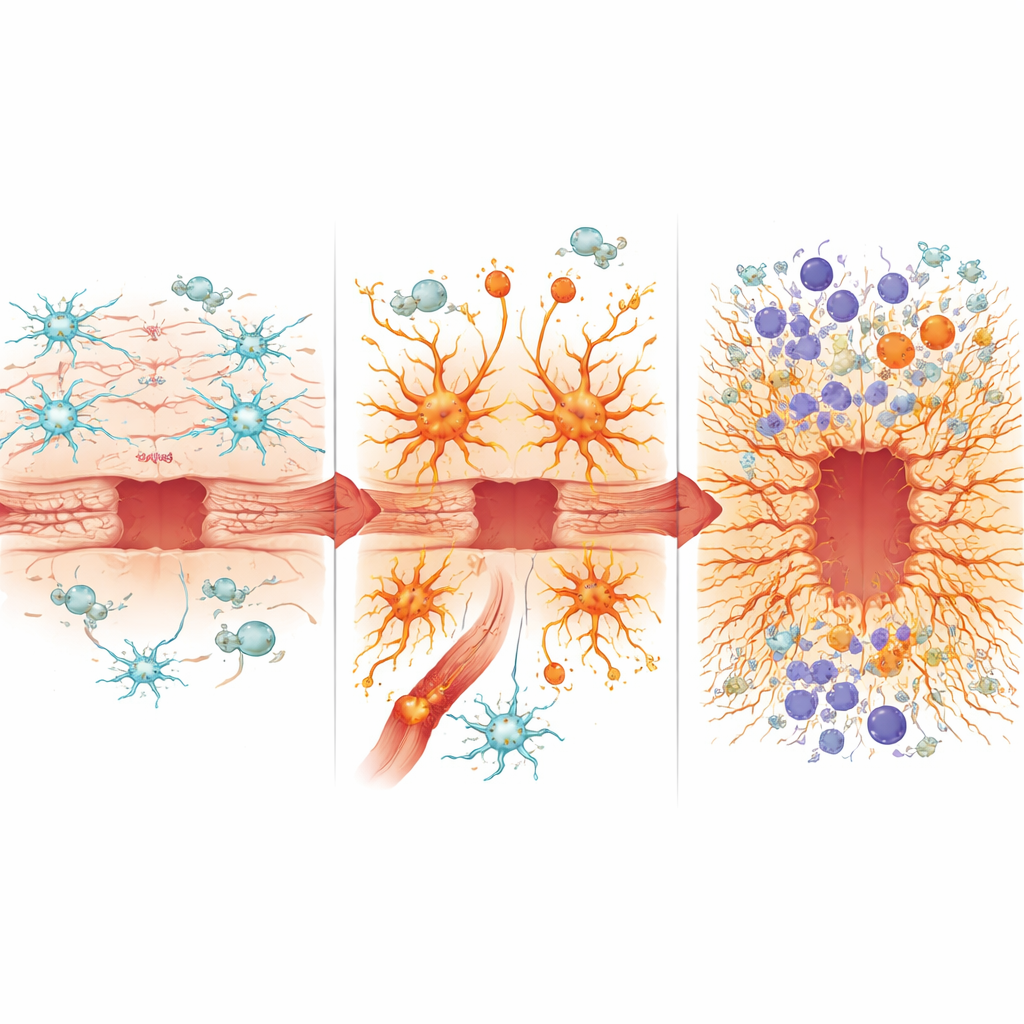
Das Anfachen des Immunfeuers
Diese fehlprogrammierten Astrozyten veränderten auch die Immunlandschaft im Gehirn. Die Blut-Hirn-Schranke wurde durchlässiger, sodass mehr periphere Immunzellen eindringen konnten. Mäuse mit überaktivem NF-κB in Astrozyten zeigten eine stärkere Infiltration entzündlicher myeloider Zellen und veränderte Zusammensetzungen von Neutrophilen, Monozyten und dendritischen Zellen sowie vermehrte zytotoxische T-Zellen, die das Gewebe weiter schädigen können. Immunzellen in diesem Umfeld zeigten stärkere Signale, die durch Interferon- und Inflammasom-Wege angetrieben werden — beides verbunden mit aggressiver, potenziell neurotoxischer Entzündung. Gleichzeitig waren die Spiegel mehrerer schützender oder pro-reparativer Proteine, wie Osteopontin, reduziert, während andere, die mit oxidativem Stress, Eisenüberladung und Vernarbung assoziiert sind — darunter Hämoxygenase-1 und Lipocalin-2 — erhöht waren. Das Verhältnis zwischen Osteopontin und Lipocalin-2 erwies sich als einfacher Marker, der das bessere oder schlechtere Heilungsverhalten in den verschiedenen Mäusestämmen nachzeichnete.
Was das für die Erholung nach Kopfverletzungen bedeutet
Zusammen zeigen die Ergebnisse, dass bei chronisch erhöhter Aktivität des NF-κB-Stresswegs in Astrozyten diese Zellen von unterstützender, organisierter Reparatur zu treibenden Kräften chaotischer Vernarbung und anhaltender Entzündung umschwenken. Anstatt eine saubere Grenze zu bauen, die den Schaden einschließt und Gewebsumbau erlaubt, tragen sie zur Entstehung einer durchlässigen, entzündlichen Nische bei, die die Läsion vergrößert und das Langzeitergebnis verschlechtert. Obwohl die Arbeit an männlichen Mäusen durchgeführt wurde, macht sie NF-κB in Astrozyten zu einem vielversprechenden Ziel für Therapien, die die Erholung nach traumatischer Hirnverletzung verbessern sollen, und deutet darauf hin, dass Blutspiegel von Molekülen wie Osteopontin und Lipocalin-2 eines Tages Klinikern helfen könnten, die Heilung des Gehirns zu überwachen.
Zitation: Hein, T.M., Nespoli, E., Hakani, M. et al. NF-κB activation in astrocytes impairs wound healing after traumatic brain injury in male mice. Nat Commun 17, 2323 (2026). https://doi.org/10.1038/s41467-026-70304-7
Schlüsselwörter: traumatische Hirnverletzung, Astrozyten, Neuroinflammation, Gehirnvernarbung, NF-kappa B