Clear Sky Science · de
Mechanismen der Hemmung von PfDNMT2 und PfATP6-vermittelte Resistenz gegen den Malariawirkstoffkandidaten SC83288 in Plasmodium falciparum
Warum das für Malaria wichtig ist
Da Malariaparasiten gegen die heute verfügbaren Medikamente resistent werden, gehen Ärzten die Optionen zur Behandlung einer Krankheit aus, die weiterhin Hunderttausende Menschen pro Jahr tötet — überwiegend kleine Kinder. Diese Studie untersucht, wie ein vielversprechender experimenteller Wirkstoff, SC83288, den tödlichsten Malariaparasiten angreift und wie der Parasit sich gelegentlich dagegen zur Wehr setzt. Das Verständnis sowohl der Wirkung des Arzneimittels als auch der Abwehrmechanismen des Parasiten ist entscheidend, um SC83288 zu einer künftigen Therapie zu machen, die so lange wie möglich wirksam bleibt. 
Eine neue Waffe gegen einen tödlichen Parasiten
SC83288 entstand aus Bemühungen, ein altes Tierarzneimittel zu verbessern, und gilt inzwischen als potenter Antimalariakandidat. In Labortests und Tiermodellen räumt es sehr schnell Parasiten aus dem Blut bei sehr niedrigen Konzentrationen aus dem Weg, auch Stämme, die bereits gegen Standardtherapien wie artemisininbasierte Kombinationen sowie ältere Mittel wie Antifolate und Chinoline resistent sind. Es wirkt zudem auf die Parasitenstadien, die auf Mücken übertragbar sind. Umfangreiche Sicherheitstests in Tieren haben bislang keine schwerwiegenden Warnsignale gezeigt, sodass SC83288 als realistischer Kandidat für klinische Prüfungen am Menschen gilt.
Wie das Medikament das Parasitenwachstum stoppt
Die Forschenden verfolgten den 48‑stündigen Zyklus des Parasiten in roten Blutkörperchen und setzten SC83288 zu verschiedenen Zeitpunkten zu. War das Medikament während der ersten zwei Drittel dieses Zyklus präsent, brachen die Parasiten die DNA‑Replikation ab und teilten ihre Zellkerne nicht, ein Prozess, der Karyokinese genannt wird. Unter dem Mikroskop wurden die behandelten Parasiten klein und kondensiert, ein Kennzeichen sterbender Zellen, während spätere Schritte wie die Bildung von Tochterparasiten und das Austreten aus dem Erythrozyten unbeeinträchtigt blieben, sofern die Teilung bereits abgeschlossen war. Damit ließ sich die Hauptwirkung von SC83288 auf das kritische Zeitfenster eingrenzen, in dem das genetische Material des Parasiten zur Produktion vieler Nachkommen verdoppelt wird.
Angriff auf das epigenetische Kontrollzentrum des Parasiten
Um zu verstehen, was SC83288 im Parasiten trifft, kombinierten die Forschenden Genexpressionsanalysen, Stoffwechselmessungen und direkte Enzymtests. Sie fanden starke Hinweise darauf, dass das Medikament die Nutzung winziger chemischer Markierungen zur Kontrolle von DNA und RNA stört. Die Konzentration eines wichtigen Donormoleküls für diese Markierungen, S‑adenosylmethionin, geriet aus dem Gleichgewicht, und globale Markierungen auf DNA und RNA fielen nach der Behandlung deutlich ab. Im Fokus stand ein zentrales Enzym, PfDNMT2, das normalerweise Methylgruppen sowohl an DNA als auch an eine spezifische Transfer‑RNA anbringt. Die Wissenschaftler zeigten, dass SC83288 seine Aktivität direkt in Reagenzgläsern und in Parasiten hemmt. Parasiten, die gentechnisch so verändert wurden, dass sie deutlich mehr PfDNMT2 produzieren, wurden weniger empfindlich gegenüber dem Wirkstoff, während zusätzliche Mengen an Methyl‑Donormolekülen die Parasiten teilweise vor SC83288 schützten. Zusammen stützen diese Ergebnisse ein Modell, in dem SC83288 durch Schwächung des epigenetischen und genexpressiven Apparats des Parasiten tötet, was zu gestoppter DNA‑Replikation und Zelltod führt. 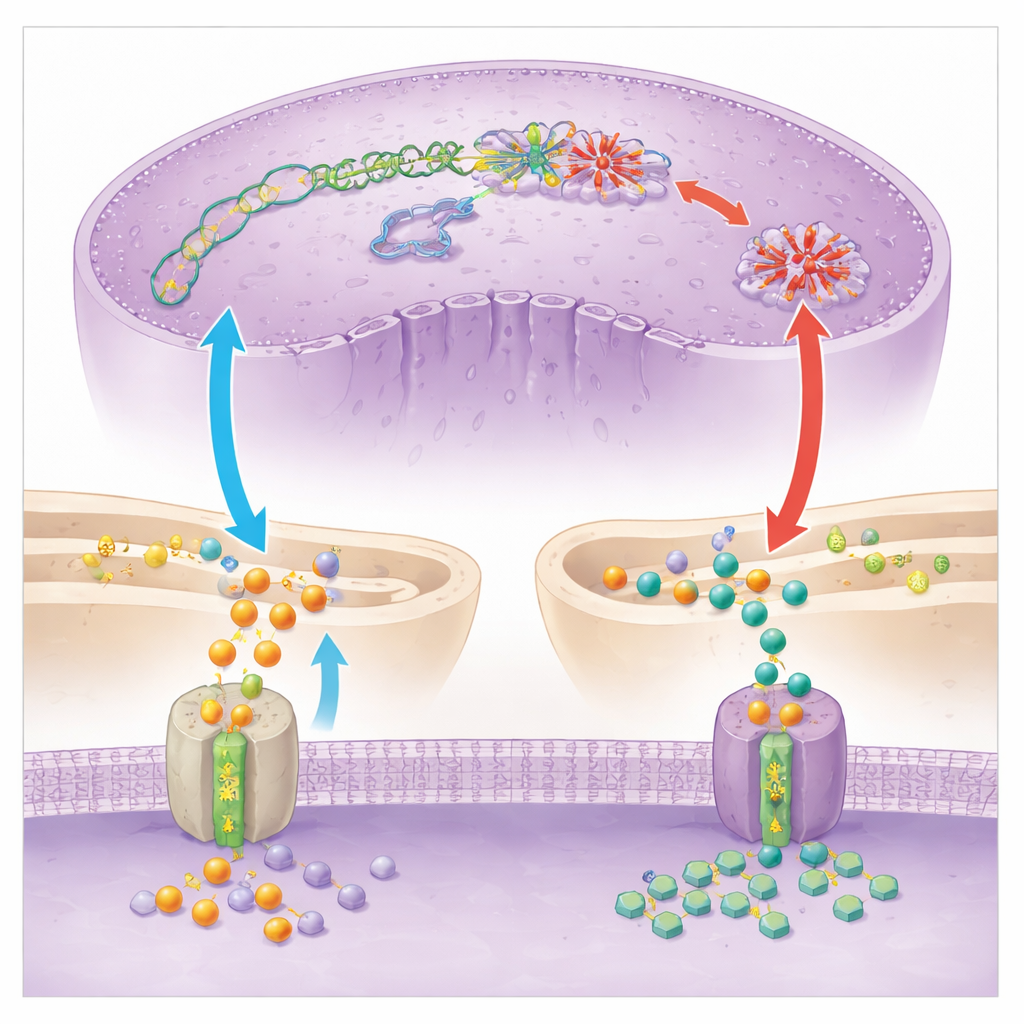
Wie der Parasit dem Schlag ausweicht
Kein wirksames Medikament ist frei von Resistenzrisiken, und SC83288 bildet da keine Ausnahme. Nach langzeitiger Exposition in Kultur erwarben einige Parasitenlinien Veränderungen nicht im Zielenzym PfDNMT2, sondern in einer Membranpumpe namens PfATP6, die normalerweise hilft, den Kalziumspiegel im endoplasmatischen Retikulum des Parasiten zu kontrollieren — einem Netzwerk interner Membranen. Mithilfe von Gentechnik führten die Forschenden eine dieser Mutationen in einen Standardstamm ein und zeigten, dass sie die Empfindlichkeit der Parasiten gegenüber SC83288 um etwa das Tausendfache verringerte. Detaillierte Transportexperimente in Hefe und in Parasiten sowie Bildgebung mit einer klickbaren fluoreszenten Version des Wirkstoffs erklärten, warum: Mutiertes PfATP6 wirkt wie ein Staubsauger und zieht SC83288 aus dem Kernbereich in das endoplasmatische Retikulum. Das Medikament gelangt zwar weiterhin in infizierte rote Blutkörperchen, wird aber nun in einem Kompartiment gebunden, in dem es die nukleären Prozesse weniger schädigen kann.
Die verborgenen Kosten der Resistenz
Obwohl die PfATP6‑Mutation die Parasiten vor SC83288 schützt, hat sie einen hohen Preis. Resistente Parasiten wuchsen deutlich langsamer als ihre nicht mutierten Gegenstücke und zeigten eine gestörte Kalzium‑Balance, was darauf hinweist, dass die veränderte Pumpe ihre normale Funktion schlecht erfüllt. In gemischten Kulturen setzten sich die fitteren Wildtyp‑Parasiten schnell gegen die Mutanten durch, wenn kein Medikament vorhanden war. Das deutet darauf hin, dass eine solche Resistenz zwar unter starkem Arzneimitteldruck entstehen kann, sich aber in Feldbedingungen wahrscheinlich nicht weit verbreiten würde, da resistente Parasiten ohne SC83288 im Nachteil wären. Aus Public‑Health‑Perspektive macht diese hohe Fitnesskostenlast, kombiniert mit der neuartigen Wirkungsweise des Medikaments gegen das epigenetische Kontrollsystem des Parasiten, SC83288 zu einem besonders attraktiven Kandidaten im Rennen, der Malaria vorauszubleiben.
Zitation: Sanchez, C.P., Duffey, M., Celada, R.V. et al. Mechanisms of PfDNMT2 inhibition and PfATP6-mediated resistance to the antimalarial candidate SC83288 in Plasmodium falciparum. Nat Commun 17, 2327 (2026). https://doi.org/10.1038/s41467-026-70280-y
Schlüsselwörter: Malaria‑Arzneimittelresistenz, Plasmodium falciparum, epigenetische Therapie, DNA‑Methylierung, Entwicklung von Antimalariamitteln