Clear Sky Science · de
NAA40 und NAC arbeiten bei der kotranslationellen Histonacetylierung beim Menschen zusammen
Wie Zellen ihre genetischen Schalter feinjustieren
In jeder menschlichen Zelle werden neu synthetisierte Proteine chemisch verändert, während sie aus den Proteinproduktionsmaschinen der Zelle — den Ribosomen — herauskommen. Diese kleinen Modifikationen können bestimmen, wohin ein Protein gelangt, wie lange es vorliegt und sogar, ob Gene ein- oder ausgeschaltet werden. Diese Studie konzentriert sich auf ein sehr spezifisches Enzym, NAA40, und einen Helferkomplex namens NAC. Sie zeigt, wie beide am Ribosom zusammenwirken, um Histonproteine — die Spulen, um die DNA gewickelt ist — zu modifizieren und damit die Genaktivität und potenziell die Krebsentstehung zu beeinflussen.
Eine winzige Kappe, die das Verhalten von Histonen verändert
Viele menschliche Proteine erhalten an ihrem N‑Terminus eine kleine chemische Kappe, einen Prozess, der als N‑terminale Acetylierung bekannt ist. Die Histone H2A und H4, die bei der Verpackung der DNA in Chromatin helfen, sind nahezu immer auf diese Weise „gekappt“. NAA40 ist unter Enzymen ungewöhnlich, weil es sich fast ausschließlich darauf spezialisiert, genau diese Kappe an diesen Histonen während ihrer Entstehung anzubringen. Diese Acetylmarke steht im Wettbewerb mit anderen chemischen Markierungen wie Phosphorylierung und Methylierung in derselben Region der Histone; ob NAA40 wirkt oder nicht, kann daher beeinflussen, wie dicht DNA verpackt ist und wie Gene reguliert werden. Wichtig ist, dass veränderte Niveaus von NAA40 mit verschiedenen Krebsarten in Verbindung gebracht wurden, was es zu einem vielversprechenden Ziel für neue Therapien macht.
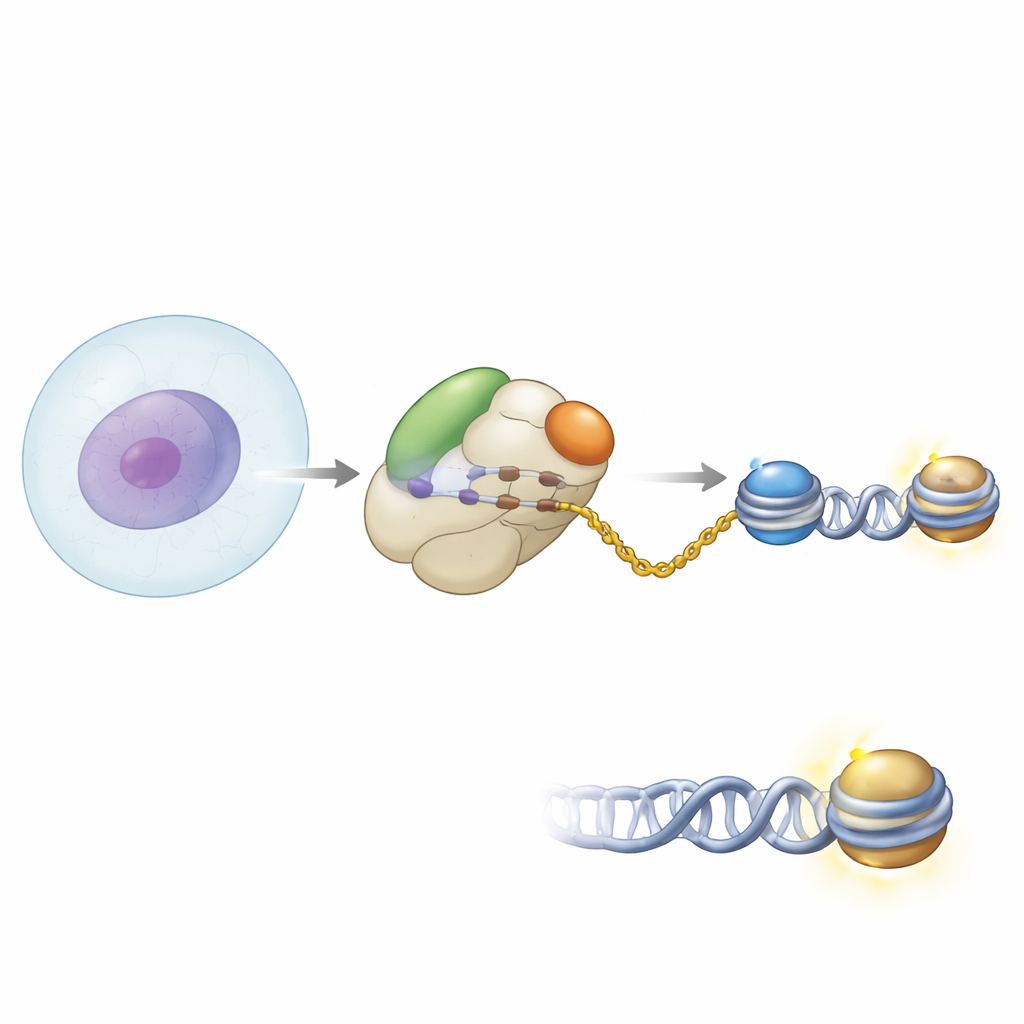
Partnerschaft am Tor der Proteinfabrik
Die Autoren verwendeten biochemische Methoden und hochauflösende Kryo‑Elektronenmikroskopie, um zu sehen, wie NAA40 am menschlichen Ribosom positioniert ist. Sie fanden heraus, dass NAA40 direkt am Ausgangstunnel sitzt, an dem frisch synthetisierte Proteinketten hervortreten. Dort arbeitet es nicht allein: Es bindet neben dem nascent polypeptide–associated complex, kurz NAC, einem häufig an Ribosomen gebundenen Helfer, der neu entstehende Proteine überwacht. Strukturelle Aufnahmen zeigten NAA40 verankert am Ribosom durch ein einzigartiges, positiv geladenes Helixsegment am N‑Terminus, während NAC über eine seiner Untereinheiten an der Ribosomenoberfläche befestigt ist. Eine flexible Domäne von NAC reicht herüber und kontaktiert NAA40, womit der Komplex das Enzym effektiv mit dem Ribosom verbindet.
Warum NAC für die Histon‑Feinabstimmung nötig ist
Um die Bedeutung dieser Partnerschaft zu prüfen, rekonstruierten die Forscher diese Wechselwirkungen mit gereinigten Komponenten in Reagenzgläsern. Sie beobachteten, dass NAA40 alleine nur schwach an Ribosomen bindet, die Bindung an Ribosomen aber deutlich stärker wird, wenn NAC vorhanden ist. Entfernten sie eine spezifische „UBA“-Region von NAC, die NAA40 kontaktiert, verschwand diese verstärkte Bindung. In menschlichen Zellen führte die Verminderung von NAC zu reduzierter NAA40‑abhängiger Acetylierung von Histon H4 und gleichzeitig zu einem Anstieg einer konkurrierenden Phosphorylierungsmarke am selben Histonschwanz. Diese Änderung trat auf, ohne dass Menge oder Lokalisation von NAA40 selbst verändert wurden, was darauf hindeutet, dass NAC hauptsächlich NAA40 rekrutiert und korrekt am translierenden Ribosom positioniert, damit Histone während der Synthese effizient modifiziert werden können.
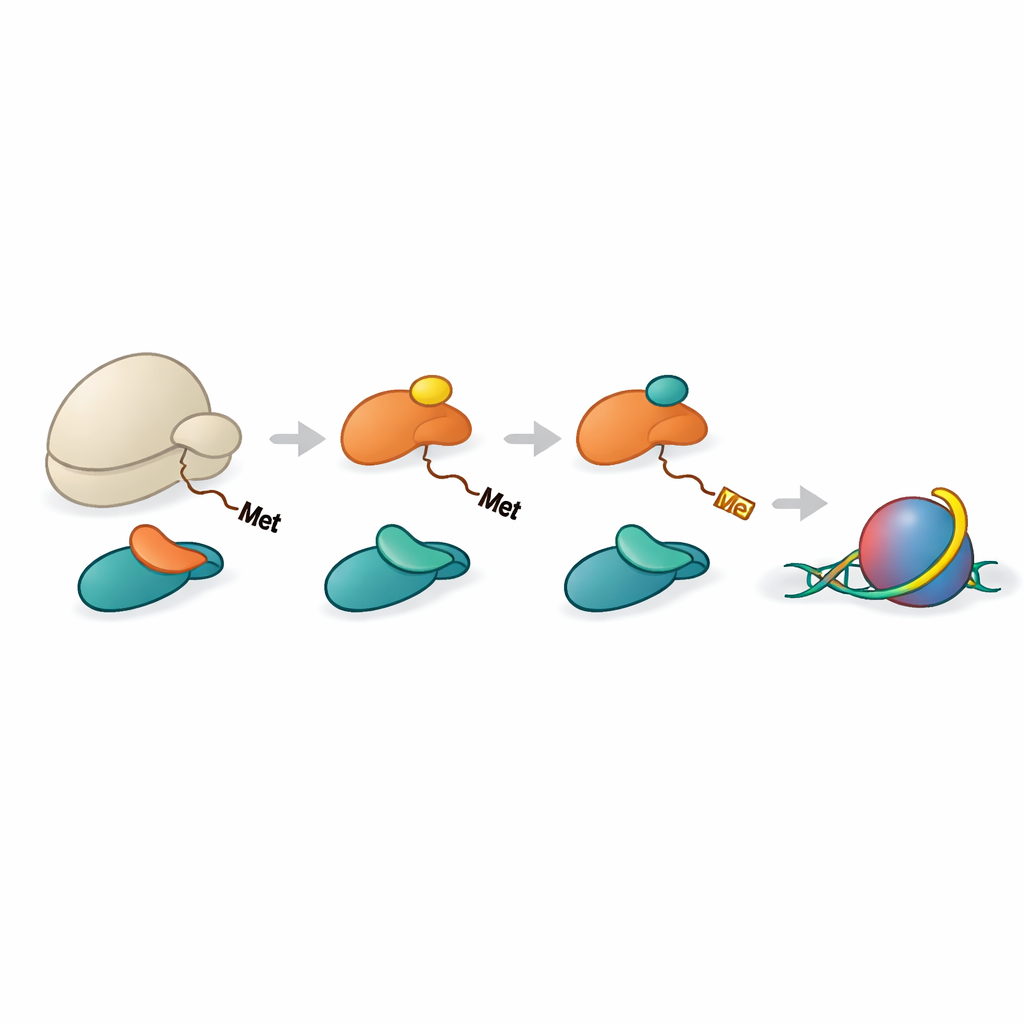
Eine koordinierte Fließband‑Organisation für die Histonverarbeitung
Die Histone H2A und H4 müssen zunächst ihr anfängliches Methionin verlieren, bevor NAA40 sie erkennen kann. Ein anderes Enzym, METAP1, übernimmt dieses Entfernen. Das Team zeigte, dass NAC helfen kann, METAP1 und NAA40 zusammen mit dem Ribosom zusammenzuführen und so eine Multi‑Enzym‑Einheit am Peptidausgang zu bilden. Hochauflösende Strukturen rekonstruierter Komplexe zeigten METAP1 und NAA40 nebeneinander am Ribosom gebunden, mit ihren aktiven Zentren in annähernd gleichem Abstand zum Austrittstunnel. Diese Geometrie bedeutet, dass, sobald ein Histonschwanz nur ein Dutzend oder so Aminosäuren über das Ribosom hinausreicht, METAP1 das Startmethionin entfernen und NAA40 unmittelbar die Acetylkappe anbringen kann, wodurch Verzögerungen zwischen den beiden Schritten minimiert werden.
Folgen für Genkontrolle und Krebs
Insgesamt zeigt die Studie, dass NAA40 nicht einfach durch die Zelle diffundiert, um Histone zu finden. Stattdessen wird es vom NAC am Ribosom angedockt und ist Teil einer organisierten Verarbeitungsstation, die Histone sofort bei ihrer Synthese vorbereitet. Durch die enge Koppelung von Methioninentfernung und Acetylierung stellt die Zelle sicher, dass Histon H2A, H4 und die mit DNA‑Schäden assoziierte Variante H2A.X schnell eine Acetylmarke erhalten, die Chromatinstruktur und Genexpression beeinflussen kann. Da Störungen in diesem frühen Histonmarkierungs‑Schritt krebsfördernd wirken können, liefert das Verständnis der präzisen Anordnung von NAA40, NAC und METAP1 am Ribosom einen strukturellen Bauplan, der die Entwicklung von Wirkstoffen leiten könnte, die diesen kritischen epigenetischen Kontrollpunkt feinjustieren.
Zitation: Guan, D., Denk, T., Klavaris, A. et al. NAA40 and NAC cooperate in co-translational histone acetylation in humans. Nat Commun 17, 2486 (2026). https://doi.org/10.1038/s41467-026-70279-5
Schlüsselwörter: Histonacetylierung, NAA40, Ribosom, nascent polypeptide-associated complex, epigenetische Regulation