Clear Sky Science · de
Ein zellzyklusabhängiger Übergang von Acetylierung zu Phosphorylierung reguliert die rechtzeitige Zentrosomreifung
Unser genetisches Gepäck auf Kurs halten
Jedes Mal, wenn eine Zelle in unserem Körper sich teilt, muss sie ihre DNA mit höchster Präzision aufteilen. Geht dieser Prozess schief, können Zellen Chromosomen gewinnen oder verlieren — ein gefährlicher Zustand, der mit Krebs und anderen Erkrankungen verknüpft ist. Diese Studie deckt ein molekulares Zeitmessgerät auf, das Zellen dabei hilft, die winzigen Strukturen zu bauen, die nötig sind, um Chromosomen korrekt zu trennen, und zeigt so eine potenzielle Schwachstelle, die künftige Krebstherapien ausnutzen könnten.
Die winzigen Verkehrsknoten der Zelle
Im Zentrum jeder teilenden Zelle sitzen Zentrosome, kleine Strukturen, die wie Verkehrsknoten für die Fasern fungieren, die Chromosomen auseinanderziehen. Bevor eine Zelle in die Teilung geht, müssen diese Knoten „reifen“: Sie reichern Hilfsproteine an und werden zu starken Organisatoren von Mikrotubuli, den dynamischen Fasern, die die Teilungsspindel bilden. Wenn diese Reifung zu früh, zu spät oder gar nicht stattfindet, können Chromosomen falsch verteilt werden, was zu Zellen mit abnormer Chromosomenanzahl führt. Zu verstehen, wie Zellen Zentrosome genau zum richtigen Zeitpunkt aktivieren, war eine lange offene Frage der Zellbiologie.
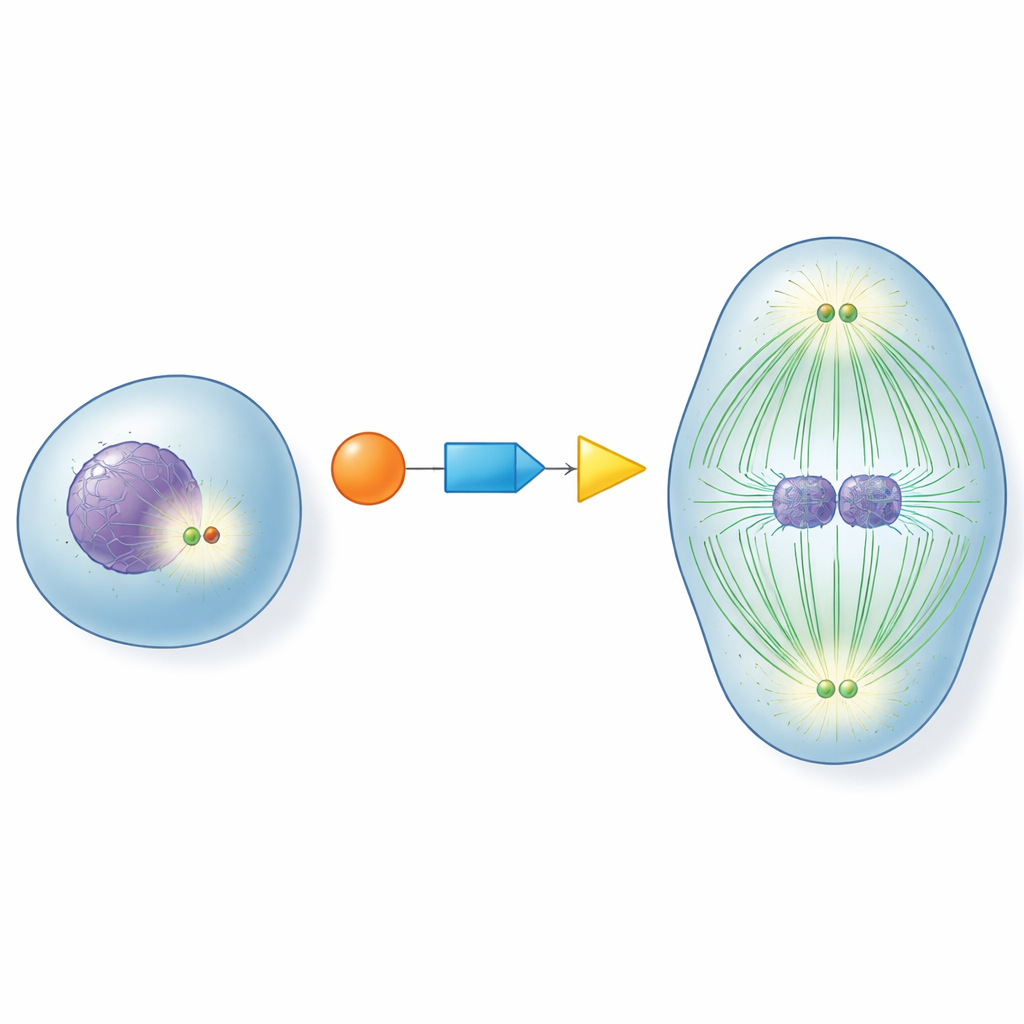
Ein molekulares Staffelspiel für perfekte Timing
Die Autoren konzentrierten sich auf drei Schlüsselproteine, die zusammen als Staffel fungieren: CDK1, ein zentraler Zellzykluskontroller; RNF40, bisher vor allem für Modifikationen von DNA-verpackenden Proteinen bekannt; und PLK1, ein wichtiger Treiber der Zellteilung. Sie entdeckten, dass RNF40 während des gesamten Zellzyklus physisch an Zentrosomen präsent ist und PLK1 direkt bindet. Wenn sich die Zelle der Teilung nähert, markiert CDK1 RNF40 an zwei spezifischen Stellen chemisch, was RNF40 wiederum zu einer besseren Andockstelle für PLK1 macht. Diese CDK1–RNF40–PLK1-Kette stellt sicher, dass PLK1 genau in der späten Vorbereitungsphase der Teilung an Zentrosomen eintrifft und so eine robuste Zentrosomreifung, Mikrotubuliwachstum und den Aufbau einer gut ausgebildeten bipolaren Spindel auslöst.
Ein formwandelnder Proteinschalter
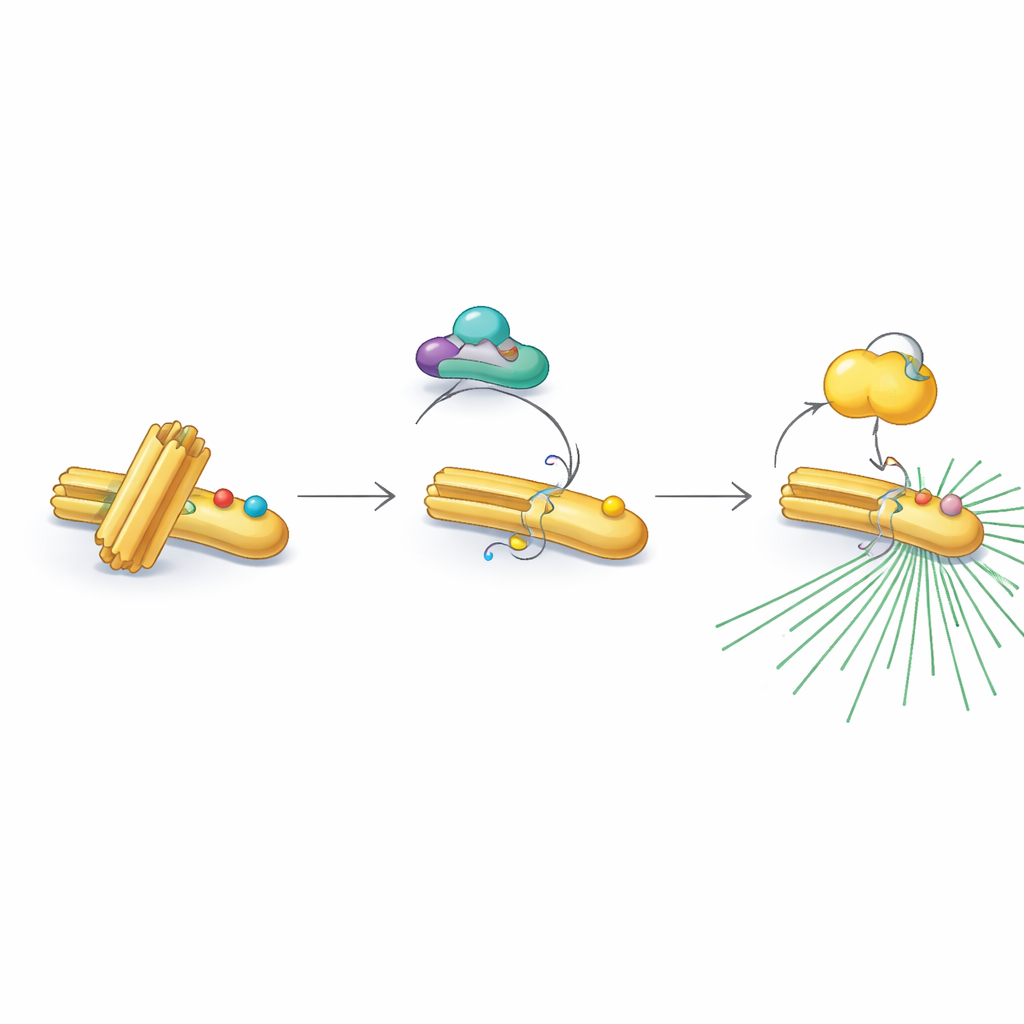
Interessanterweise nimmt RNF40 diese aktivierenden Markierungen nicht immer an. In nicht teilenden Phasen und während der DNA-Replikation trägt RNF40 eine andere chemische Kennzeichnung — Acetylgruppen — an zwei benachbarten Positionen. Diese Acetylmarken werden von einem Enzym namens PCAF angefügt und später von einem Deacetylasepartner, HDAC1, entfernt. Die acetylierte Version von RNF40 widersteht der Modifikation durch CDK1 und blockiert damit effektiv den nächsten Schritt der Staffel. Wenn die Zellen in die letzte Vorbereitungsphase der Teilung eintreten, entfernt HDAC1 nach und nach die Acetylmarken, sodass CDK1 stattdessen Phosphatgruppen anbringen kann. Dieser sorgfältig zeitliche Wechsel von Acetylierung zu Phosphorylierung verwandelt RNF40 vom „Bereitschafts“- in den „Aktiv“-Zustand, bereit, PLK1 anzuwerben und das Zentrosom hochzufahren.
Was geschieht, wenn das Timing versagt
Um zu untersuchen, wie entscheidend dieser Schalter ist, konstruierten die Forscher Zellen, in denen RNF40 nicht mehr phosphoryliert werden konnte oder in denen es gezwungen wurde, in einem acetylierungsähnlichen Zustand zu verbleiben. In beiden Fällen sammelte sich PLK1 nicht richtig an den Zentrosomen. Diese Zellen zeigten abgeschwächtes Mikrotubuliwachstum von den Zentrosomen, missgebildete Spindeln und fehlplatzierte Chromosomen. Viele wiesen schließlich zusätzliche oder fehlende Chromosomen auf — ein abnormer Zustand, bekannt als Aneuploidie — und einige wurden binukleär, ein Zeichen katastrophaler Teilungsfehler. In Krebsmodellen bildeten Zellen, die im „acetylieren“ RNF40-Zustand verharrten, kleinere Tumoren in Mäusen und waren empfindlicher gegenüber gängigen Chemotherapeutika zur Behandlung von Darmkrebs. Das deutet darauf hin, dass die Störung dieses Schalters das Tumorwachstum bremsen kann.
Verbindungen zu menschlichem Krebs und zukünftige Möglichkeiten
Das Team untersuchte außerdem Patientendaten und Tumorproben. Sie fanden heraus, dass RNF40 in Darmkrebserkrankungen oft ungewöhnlich stark vorkommt und dass bestimmte krebsassoziierte Mutationen nahe seinen Modifikationsstellen dessen Phosphorylierung stören und so die richtige Zentrosomfunktion untergraben. Diese Beobachtungen verbinden den neu beschriebenen Zeitmechanismus direkt mit menschlichen Erkrankungen. Indem sie ein spezifisches Protein identifizieren, das koordiniert, wann Zentrosome reifen und wie Chromosomen getrennt werden, hebt die Studie einen Signal-„Knoten“ hervor, der gezielt angegriffen werden könnte, um schnell teilende Krebszellen in tödliche Teilungsfehler zu treiben, während gesunde Zellen weniger betroffen bleiben.
Ein neuer Ansatz für zuverlässige Zellteilung
Für Nicht-Spezialisten lautet die Kernbotschaft: Zellen verlassen sich auf einen fein abgestimmten chemischen Schalter an einem einzelnen Protein, RNF40, um genau zu entscheiden, wann die Maschinerie zur Trennung der Chromosomen aktiviert werden soll. Dieser Übergang von Acetylierung zu Phosphorylierung verhält sich wie eine Ampel an einer stark befahrenen Kreuzung, die erst dann auf Grün schaltet, wenn die Zelle wirklich bereit zur Teilung ist. Wenn die Ampel ausfällt, stolpern Zellen durch die Teilung, häufen genetische Fehler an und können krebsartig werden. Das Verständnis und die Kontrolle dieses Schalters könnten neue Wege zu Therapien eröffnen, die Krebszellen selektiv destabilisieren, indem sie deren Fähigkeit zur sauberen Teilung sabotieren.
Zitation: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
Schlüsselwörter: Zentrosomreifung, Zellteilung, Chromosomeninstabilität, PLK1-Signalgebung, Darmkrebs