Clear Sky Science · de
Wiederherstellung früher postnataler synaptischer Dysregulation rettet Motoneuronen vor Degeneration in einem Mausmodell der spino-bulbären Muskelatrophie
Warum winzige frühe Veränderungen später Muskelschwäche bewirken können
Die spino-bulbäre Muskelatrophie (SBMA) ist eine seltene erbliche Erkrankung, bei der Erwachsene, meist Männer, langsam Muskelkraft in Gliedmaßen, Rumpf und Rachen verlieren. Symptome treten im mittleren Lebensalter auf, doch subtile Probleme beginnen deutlich früher. Diese Studie stellt eine überraschende Frage: Könnten kurze Ereignisse in den ersten Lebenstagen still und leise die Grundlage für den Verlust von Nervenzellen Jahrzehnte später legen — und könnte das Korrigieren dieser frühen Störungen die Bewegung schützen?
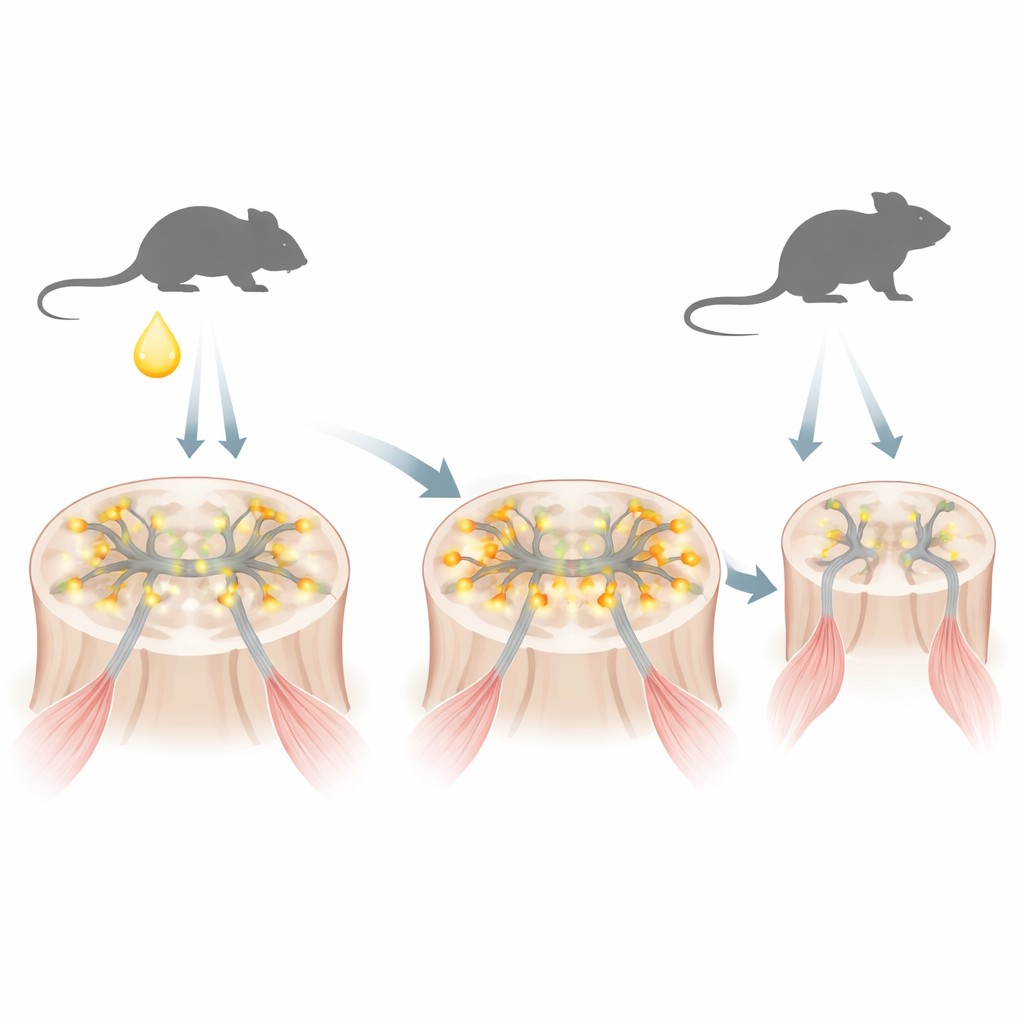
Eine Erkrankung, verwurzelt in einem hormonempfindlichen Schalter
SBMA wird durch eine veränderte Version des Androgenrezeptors verursacht, eines Proteins, das männliche Hormone wie Testosteron erkennt. Der veränderte Rezeptor trägt eine übermäßig lange Folge der Aminosäure Glutamin. In einem Mausmodell, das die menschliche Erkrankung nachahmt, fanden die Autor:innen heraus, dass sich unmittelbar nach der Geburt — wenn bei männlichen Neugeborenen kurzzeitig Testosteron ansteigt — dieser mutierte Rezeptor rasch in den Zellkernen der Motoneuronen ansammelt, also der Nervenzellen, die Muskeln steuern. In diesem frühen Stadium hat sich das Protein noch nicht in die typischen großen Aggregate verklumpt, die mit Neurodegeneration in Verbindung gebracht werden, verändert aber bereits, welche Gene an- oder abgeschaltet sind.
Frühe synaptische Überaktivität und ruhelose Motoneuronen
Mithilfe einer genomweiten RNA-Sequenzierung von Rückenmarkgewebe neugeborener Mäuse entdeckte das Team, dass viele Gene, die an exzitatorischen Synapsen — den Kontaktstellen, an denen Nervenzellen miteinander kommunizieren — beteiligt sind, ungewöhnlich aktiv waren. Viele dieser Gene codieren Glutamatrezeptoren, die Neuronen feuern lassen. Die Forscher:innen führten dieses Muster auf eine Störung von REST zurück, einem zentralen „Brems“-Protein, das solche synaptischen Gene während der Entwicklung normalerweise streng kontrolliert. In SBMA-Mäusen und in aus induzierten pluripotenten Stammzellen gewachsenen Motoneuronen von Patient:innen war die REST-Aktivität geschwächt, und eine verkürzte Form namens REST4 wurde bevorzugt, wodurch die Bremse gelöst und glutamaterge Synapsengene hochreguliert wurden. Entsprechend zeigten neugeborene SBMA-Motoneuronen höhere c-Fos-Werte, einen Marker kürzlicher Aktivität, und menschliche patientenabgeleitete Motoneuronen zeigten stärkere und häufigere Kalziumausbrüche — Kennzeichen von Hyperexzitabilität.
Kurzfristige frühe Behandlung, die den Lebensverlauf ändert
Die Forschenden fragten dann, ob das Herunterregulieren des mutierten Rezeptors oder die Wiederherstellung der REST-Bremse nur während dieses neonatalen Zeitfensters den langfristigen Krankheitsverlauf verändern könnte. Sie verabreichten Antisense-Oligonukleotide — kurze Stränge modifizierten genetischen Materials — in die Flüssigkeit rund um Gehirn und Rückenmark ein tägiger SBMA-Mäuse. Ein Typ von Oligonukleotid senkte vorübergehend sowohl den mutierten als auch den normalen Androgenrezeptor im Zentralnervensystem. Ein zweiter Typ beeinflusste das REST-Spleißen zugunsten der vollen REST-Länge statt REST4 und bändigte so synaptische Gene. Bemerkenswerterweise lebten die Mäuse länger, liefen besser auf einer Rotarod-Prüfung und behielten später eine stärkere Greifkraft, obwohl diese Behandlungen nur einmal verabreicht wurden und ihre direkten molekularen Effekte nach einigen Wochen nachließen. Ihre Motoneuronen und Muskelfasern waren weniger geschrumpft, und frühe Marker neuronaler Überaktivität sowie spätere Anstiege stressbezogener Neuropeptide waren abgeschwächt.
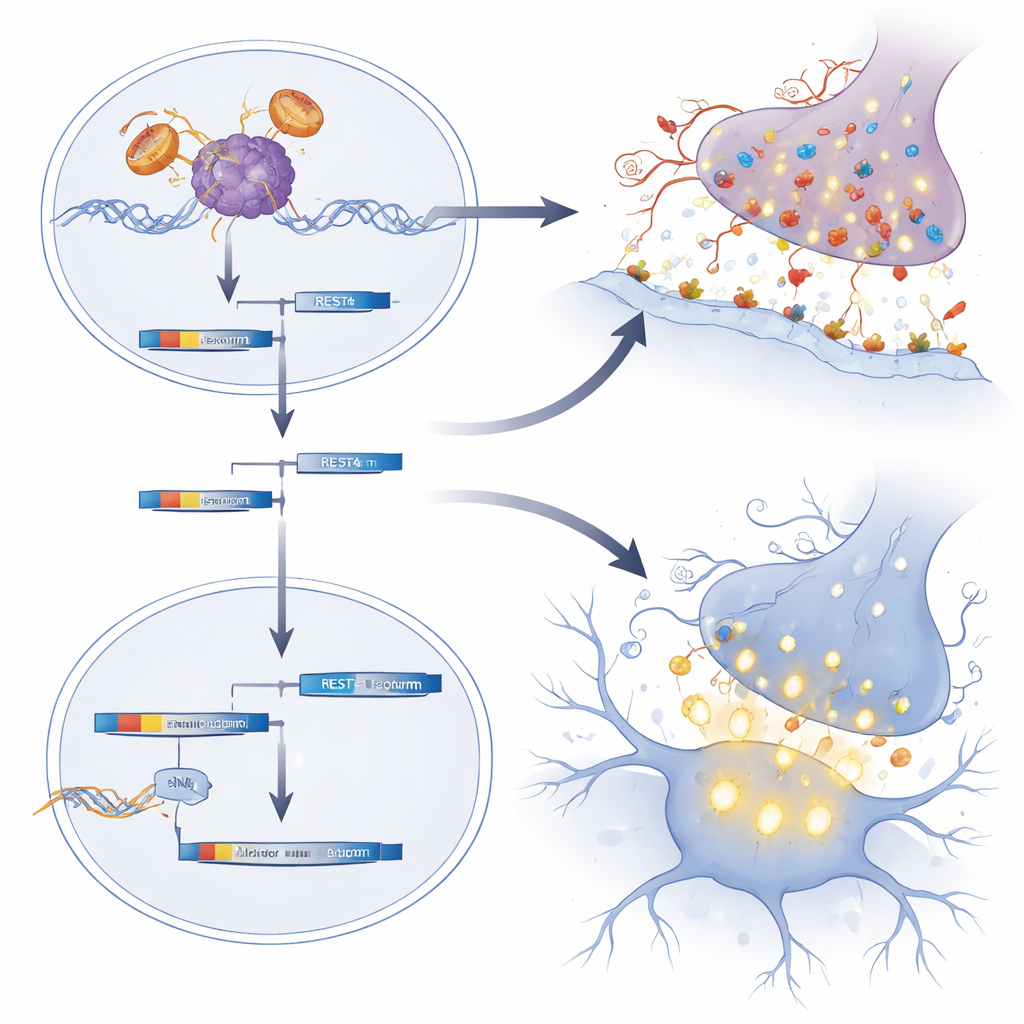
Wie frühe Hormone und Genabstimmung Verwundbarkeit formen
Die Arbeit unterstreicht außerdem die besondere Verwundbarkeit der Motoneuronen gegenüber dem kurzen Testosteronanstieg kurz nach der Geburt. Als neugeborenen SBMA-Mäusen zusätzliches Testosteron verabreicht wurde, verschlechterten sich ihre spätere Schwäche und Gewichtsabnahme, und Genprogramme, die mit gesunder Motoneuronenreifung verbunden sind, wurden weiter gestört. Normale Mäuse zeigten diese Schäden nicht, was betont, dass die Kombination aus mutiertem Rezeptor und hormonellem Schub schädlich ist. Insgesamt deuten die Befunde darauf hin, dass bei SBMA zu viele exzitatorische Synapsen und zu reizbare Motoneuronen im frühen Leben das System langsam in Richtung Versagen treiben, obwohl offensichtliche Symptome erst im mittleren Alter auftreten.
Was das für Menschen mit SBMA bedeutet
Für Nicht-Spezialist:innen ist die Kernaussage, dass SBMA teilweise eine Erkrankung fehlzeitig und fehlverdrahteter Synapsen in den ersten Lebenstagen sein könnte. Ein fehlerhafter Hormonsensor drängt sich entwickelnde Motoneuronen in einen übererregten Zustand, und dieser frühe Stress trägt schließlich Jahre später zu ihrer Degeneration bei. Ermutigend ist, dass sorgfältig entwickelte genetische Medikamente, die während dieser kritischen Fenster verabreicht werden, das Gleichgewicht der Signale in Motoneuronen zurücksetzen, ihre Überaktivität beruhigen und bei Tieren den Verlust von Nervenzellen später im Leben deutlich verzögern oder verringern können. Die Übertragung solcher Interventionen in das frühe Leben beim Menschen erfordert zwar große Sorgfalt und weitere Studien, aber diese Ergebnisse weisen auf neue Strategien, die die Wurzeln von SBMA lange vor dem Auftreten von Schwäche ansprechen.
Zitation: Hirunagi, T., Sahashi, K., Iida, M. et al. Restoring early postnatal synaptic dysregulation rescues motor neuron degeneration in a mouse model of Spinal and Bulbar Muscular Atrophy. Nat Commun 17, 2412 (2026). https://doi.org/10.1038/s41467-026-70244-2
Schlüsselwörter: spino-bulbäre Muskelatrophie, Hyperexzitabilität von Motoneuronen, Androgenrezeptor, REST synaptische Regulation, Antisense-Oligonukleotid-Therapie