Clear Sky Science · de
Wegeselektion zwischen Click‑ und Acylübertragungsreaktionen gesteuert durch Aminoacylphosphate
Warum Timing in alltäglicher Chemie wichtig ist
In jeder Zelle werden wichtige Moleküle in einer sehr genauen Reihenfolge aufgebaut und verändert, ähnlich den Schritten eines Rezepts. Dieses Timing entscheidet, ob ein Protein an- oder abgeschaltet wird oder seine Gestalt ändert. Chemiker möchten solche eingebauten Zeitpläne mit einfachen, unbelebten Molekülen in Wasser nachbilden, ohne Enzyme oder äußere Auslöser wie Licht‑ oder pH‑Sprünge zu verwenden. Dieser Artikel beschreibt ein künstliches Reaktionssystem, das genau das leistet: Es nutzt die Struktur kleiner Peptide und eine verbreitete Bindungsbildung aus der „Click‑Chemie“, um zu bestimmen, welcher chemische Schritt zuerst abläuft und welcher warten muss.
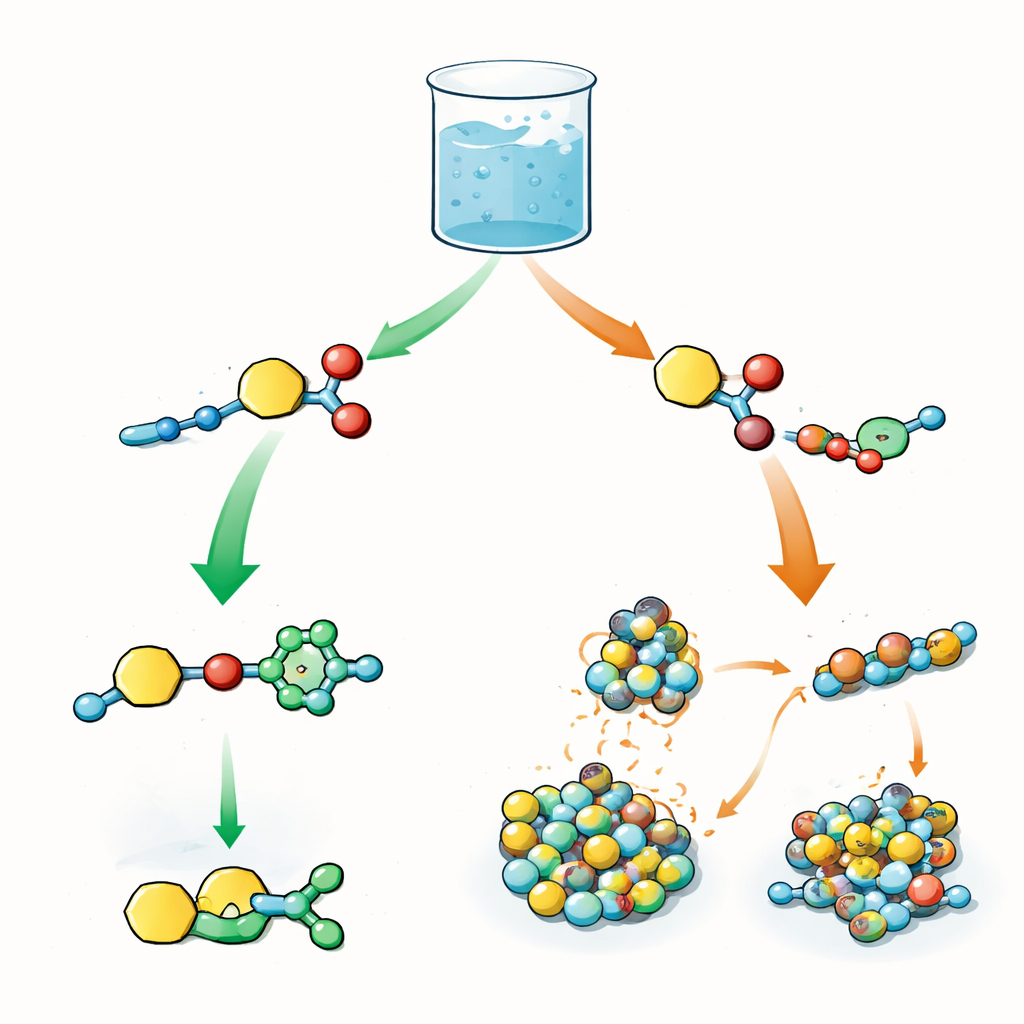
Zwei rivalisierende Reaktionen in einem Gefäß
Die Autoren entwerfen einen zentralen Baustein, der zwei reaktive Merkmale trägt: eines, das eine Acylgruppe weitergeben kann (ein kleines chemisches Fragment, das häufig zur Modifikation von Proteinen verwendet wird), und ein anderes, das eine Click‑Reaktion durchlaufen kann, die als kupferkatalysierte Azid‑Alkin Cycloaddition bekannt ist. Im selben Gefäß wird dieser Baustein mit Aziden und kurzen Peptiden gemischt, die als Nukleophile fungieren und die Acylgruppe greifen. In der Biologie steuern die Reihenfolge solcher Schritte – Aktivierung, Übertragung und spätere Modifikationen – das Verhalten von Proteinen. Hier ist die Frage ähnlich: Wenn beide Reaktionen gleichzeitig möglich sind, entscheidet sich das System für die Click‑Reaktion zuerst, die Acylübertragung zuerst oder für eine Mischung beider?
Langsamer Sauerstoff, schnelles Schwefel
Das Team untersucht zunächst Peptide, die Tyrosin enthalten, eine Aminosäure mit einer sauerstoffbasierten Seitenkette. Unter mild basischen Bedingungen läuft die Click‑Reaktion schnell voran: Alkin und Azid verbinden sich rasch, während die Acylübertragung auf die Tyrosinseitenkette träge verläuft und kaum nachweisbare Zwischenprodukte anreichert. Mehrere aus der Click‑Reaktion abgeleitete Produkte koexistieren, und es gibt kaum eine klare zeitliche Verzögerung zwischen den Schritten. Wenn die Forscher zu Cystein wechseln, einer Aminosäure mit einer schwefelhaltigen Seitenkette, dreht sich das Bild um. Cystein bildet schnell Thioester—schwefelgebundene Acylprodukte—die in hoher Ausbeute lange vor allen Click‑Produkten auftreten. Erst nach vielen Stunden treten Click‑Produkte auf. Diese Verschiebung entsteht, weil der Schwefel nicht nur reaktiver ist, sondern auch Kupferionen bindet, den Katalysator einbindet und den Click‑Pfad vorübergehend „pausiert“.
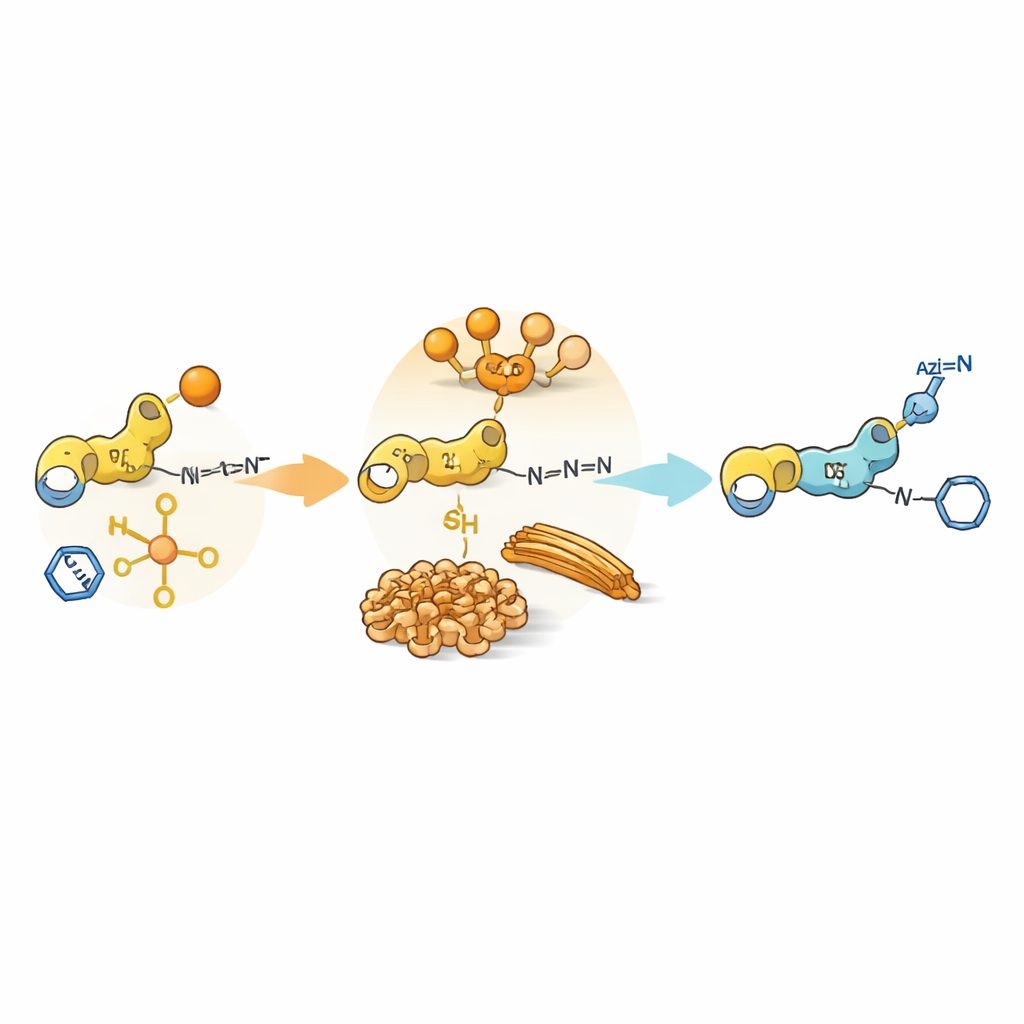
Selbstassemblierung als chemische Sperre
Über die einfache Reaktivität hinaus können die Peptide selbst in Wasser zu größeren Strukturen verklumpen und weiche Gele oder Fasern bilden. Diese Assemblierungen schaffen winzige Domänen, in denen einige Partner konzentriert und andere ausgeschlossen sind. Für bestimmte Tyrosin‑ oder Cystein‑haltige Dipeptide mit zusätzlichen aromatischen Gruppen bilden sich Zwischenprodukte, die zu Fibrillen oder dichten Partikeln selbstorganisieren. Innerhalb dieser gepackten Bereiche wird die Acylübertragung begünstigt, weil Nukleophil und Acyl‑Donor nebeneinander sitzen, während Azid und Kupferkatalysator größtenteils in der umgebenden Lösung verbleiben. Infolgedessen, obwohl die Click‑Reaktion in freier Lösung intrinsisch schnell ist, wird sie dadurch verlangsamt, dass sie zu den eingebetteten Reaktionsstellen gelangen muss. Diese „Phasen‑Mismatch“ zwischen dem Aufenthaltsort des Katalysators und dem der Substrate verlängert die Lebensdauer acylierten Zwischenprodukte und verzögert den Beginn der Click‑Chemie.
Kaskaden und Auswahl programmieren
Um zu testen, wie weit sie dieses eingebaute Timing treiben können, entwerfen die Autoren komplexere Situationen. In einem Fall enthält ein einzelnes Peptid sowohl Cystein als auch Tyrosin und bietet zwei verschiedene Acylübertragungsstellen. Die Reaktion verläuft als dreistufige Kaskade: Zuerst bildet sich ein Thioester am Cystein, dann wandert eine zweite Acylgruppe auf das Tyrosin, und erst nach diesen Schritten erscheinen Click‑Produkte. In einer anderen Versuchsreihe konkurrieren zwei verschiedene Azide—einer flexibel und aliphatisch, der andere starr und aromatisch—um dasselbe reaktive Zentrum. Überraschenderweise bevorzugt das System konsistent das aliphatische Azid, was zeigt, dass sogar Form und elektronische Eigenschaften des Azids beeinflussen können, welche Produkte dominieren, während das Timing der Acylübertragung weiterhin durch das Peptid gesteuert wird.
Was das für zukünftige smarte Materialien bedeutet
Vereinfacht ausgedrückt zeigt diese Arbeit, wie man mehrere potenziell konkurrierende Reaktionen in derselben einfachen wasserbasierten Mischung verpacken und dennoch in einer festgelegten Reihenfolge ablaufen lassen kann—ohne Enzyme, Pumpen oder äußere Schalter. Durch die Wahl, ob ein Peptid Sauerstoff oder Schwefel trägt, durch Anpassung seiner Neigung zur Selbstassemblierung und durch Veränderung der Natur des Azidpartners kodieren die Autoren eine Art innere Uhr in ein kleines chemisches Netzwerk. Frühe, reversible Acylübertragungen erzeugen kurzlebige Zwischenprodukte, die bestimmen, wann und wie der robuste, nahezu irreversible Click‑Schritt eintritt. Solche programmierten Sequenzen könnten die Grundlage für smarte Materialien und synthetische Reaktionsnetzwerke werden, die im Laufe der Zeit ihre eigenen Wege „entscheiden“, ähnlich der sorgfältig getakteten Chemie in lebenden Zellen.
Zitation: Bhattacharjee, D., Sharma, A., Dai, K. et al. Pathway selection between click and acyl transfer reactions driven by aminoacyl phosphates. Nat Commun 17, 2407 (2026). https://doi.org/10.1038/s41467-026-70199-4
Schlüsselwörter: Click‑Chemie, Acylübertragung, supramolekulare Assemblierung, Reaktionsnetze, Peptidchemie