Clear Sky Science · de
Molekulare Kartierung in DNA-PAINT mittels modifiziertem Gaussian Mixture Modeling
Die unsichtbare Welt der Moleküle sichtbar machen
Die moderne Biologie verlässt sich zunehmend auf Mikroskope, die nicht nur Zellen, sondern einzelne Moleküle in ihnen erkennen können. Doch aus dem schwachen, flackernden Licht dieser Moleküle eine verlässliche „Karte“ ihrer Positionen zu erstellen, ist überraschend schwierig. Diese Studie stellt eine neue rechnerische Methode vor, G5M genannt, die diese molekularen Karten deutlich genauer und detaillierter macht und Forschern hilft zu verstehen, wie Proteine in echten Zellen angeordnet und gruppiert sind — bis hinunter auf wenige Nanometer.
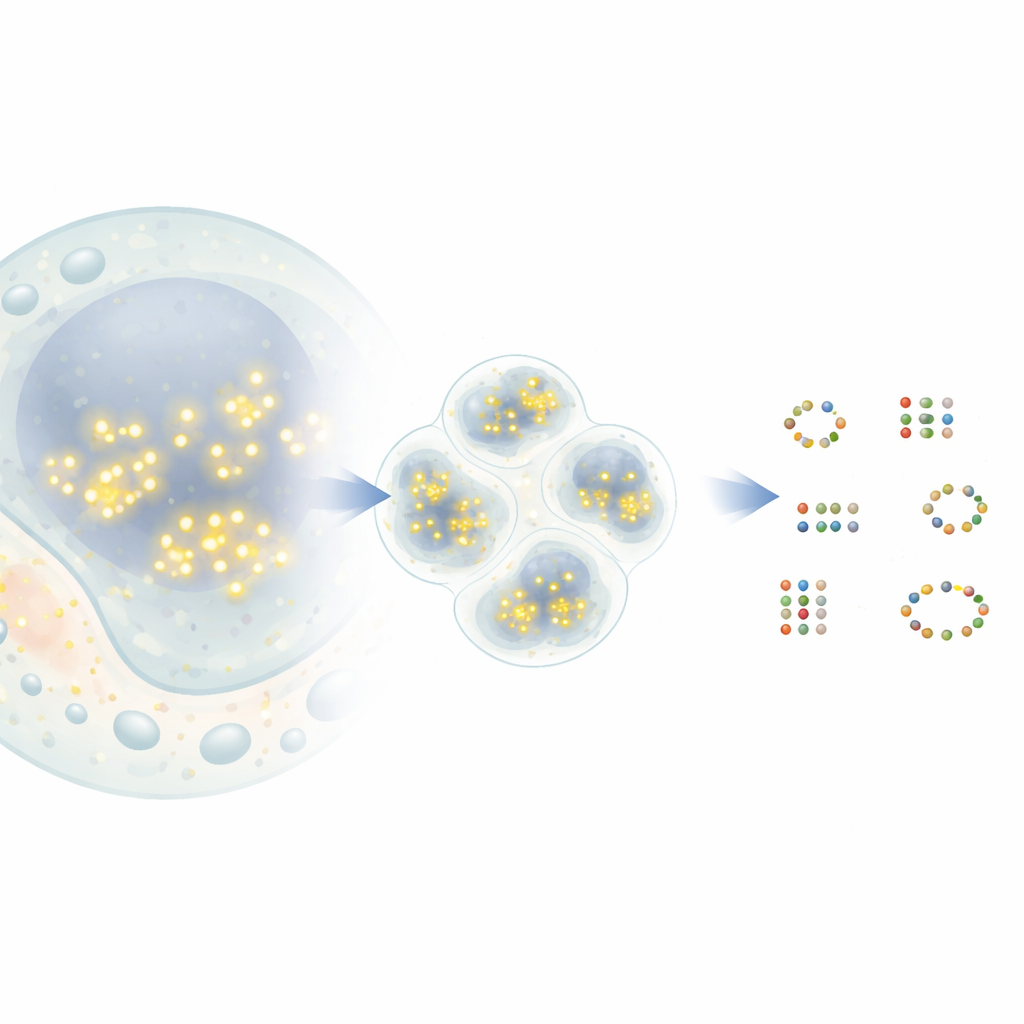
Von blinkenden Punkten zu molekularen Karten
Bei einer verbreiteten Super‑Auflösungstechnik namens DNA‑PAINT binden und lösen sich kurze DNA-Stränge mit Fluoreszenzfarbstoffen kurzzeitig an passende DNA‑Tags, die an Zielproteinen befestigt sind. Jedes Mal, wenn ein Farbstoff bindet, erscheint er als heller Punkt im Mikroskop, bevor er wieder verschwindet. Im Laufe der Zeit entsteht um jedes Protein eine Wolke solcher Ereignisse. Prinzipiell markiert das Zentrum jeder Wolke die wahre Position eines Proteins mit Nanometerpräzision. In der Praxis können sich jedoch Wolken benachbarter Proteine überschneiden, und einige Punkte stammen aus zufälligem Hintergrund. Bestehende Analysewerkzeuge fassen nahe beieinanderliegende Punkte oft zu einem einzigen Protein zusammen oder erfinden umgekehrt Proteine, die nicht existieren, was die biologische Aussagekraft einschränkt.
Ein klügerer Weg, echte Moleküle zu finden
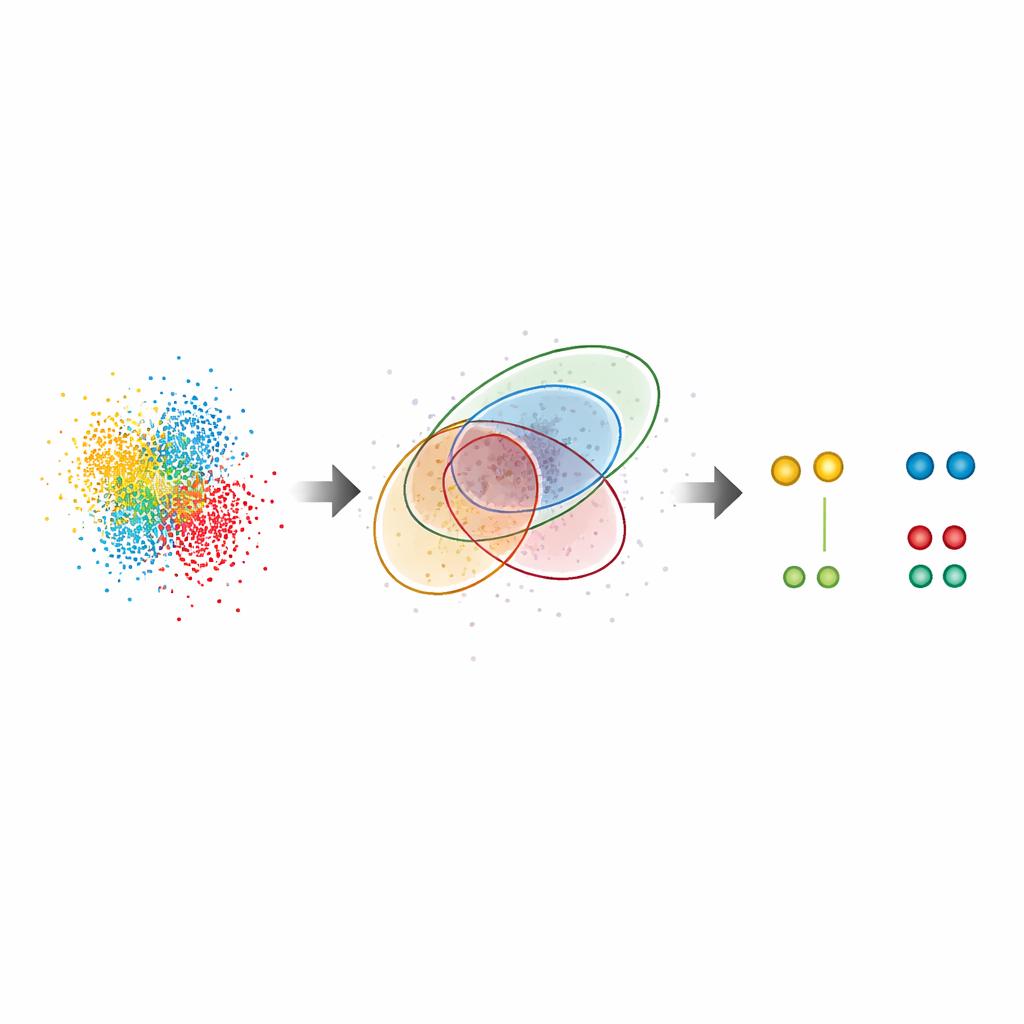
Die neue Methode G5M behandelt die Ansammlung von Punkten als Mischung einfacher, glockenförmiger Wolken, von denen jede einem echten Molekül entspricht. Statt nur nahe Punkte nach Dichte zu gruppieren, nutzt G5M ein probabilistisches Modell, das bereits bekannte Informationen über das Experiment einbezieht: wie genau Positionen gemessen werden können, wie schnell DNA‑Stränge binden und dissoziieren und wie das Mikroskop Licht in zwei oder drei Dimensionen verwischt. Anschließend prüft es verschiedene mögliche Erklärungen — unterschiedliche Anzahlen und Formen von Wolken — und wählt automatisch diejenige, die am besten Passung und Einfachheit ausbalanciert. Zusätzliche Schutzmechanismen verwerfen verdächtige Lösungen, etwa Wolken, die zu schmal, zu breit, auf zu wenigen Punkten basieren oder nicht deutlich voneinander getrennt sind.
Leistungsnachweis in Simulationen und DNA-Nanostrukturen
Zum Testen von G5M nutzten die Autoren zunächst realistische Computersimulationen einfacher Szenen: Paare von Molekülen und kleine Gitter aus zwölf Molekülen, die nur wenige Nanometer auseinander lagen. Im Vergleich zur derzeit führenden Methode, bekannt als Gradient Ascent, fand G5M deutlich mehr der Moleküle, die bei der theoretischen Auflösungsgrenze sichtbar sein sollten, und meldete kaum jemals Moleküle, die nicht existierten. In entscheidenden Fällen erkannte es eng beieinanderliegende Paare 27‑mal häufiger als die ältere Methode und verbesserte die effektive Auflösung um mehr als die Hälfte. Das Team bestätigte diese Vorteile experimentell mit DNA‑Origami‑Strukturen — künstlichen DNA‑Formen mit exakt platzierten Docking‑Stellen — und zeigte, dass G5M nahezu alle erwarteten Stellen zuverlässig zählen und lokalisieren konnte unter verschiedenen Bildgebungsbedingungen.
Verborgene Muster in echten Zellen aufdecken
Über Testproben hinaus wurde G5M auf komplexe biologische Systeme angewandt. In Kernporenkomplexen, den großen Toren des Zellkerns, rekonstruiert die Methode die bekannte ringförmige Anordnung eines Schlüsselproteins, Nup96, selbst dort, wo Partner nur etwa zehn Nanometer auseinanderlagen. Sie fand nahezu doppelt so viele Proteinpaare wie die Standardmethode und reproduzierte unabhängige Schätzungen der Markierungseffizienz, was darauf hindeutet, dass sie weder viele Moleküle übersieht noch fälschlicherweise hinzufügt. Die Autoren untersuchten zudem CD20, einen Oberflächenrezeptor, der bei Blutkrebs eine Rolle spielt und Ziel therapeutischer Antikörper ist. Hier zeigte G5M deutlich mehr kleine Cluster (Dimere, Trimere und Tetramere) von CD20 auf der Zellmembran und klärte, wie ein Antikörper gegen Krebs und verwandte Arzneiformate diese Rezeptoren umorganisieren. Es verbesserte sogar die Leistung eines ultrahochauflösenden Verfahrens namens RESI, das darauf beruht, Signale über mehrere Aufnahmerunden zu trennen.
Was das für die zukünftige Mikroskopie bedeutet
Indem es verlässlichere Informationen aus bestehenden DNA‑PAINT‑Daten gewinnt, zeigt G5M, dass bessere Software allein neue biologische Details erschließen kann, ohne Mikroskope oder Farbstoffe zu ändern. Der Algorithmus hält falsch positive Detektionen äußerst gering, während er Moleküle auflöst, die fast aneinanderstoßen — entscheidend, wenn man wissen will, wie viele Proteine in einem Komplex sitzen, wie sie angeordnet sind oder wie ein Medikament ihre Verteilung verändert. In die Open‑Source‑Plattform Picasso integriert und robust gegenüber typischen Einstellungen ist G5M auf dem besten Weg, ein Standardwerkzeug zu werden, um blinkende Fluoreszenz in verlässliche molekulare Karten zu verwandeln und Forschern dabei zu helfen, die nanoskalige Organisation des Lebens in Zellen zu kartieren.
Zitation: Kowalewski, R., Reinhardt, S.C.M., Pachmayr, I. et al. Molecular mapping in DNA-PAINT via modified Gaussian Mixture Modeling. Nat Commun 17, 2315 (2026). https://doi.org/10.1038/s41467-026-70198-5
Schlüsselwörter: Superauflösungsmikroskopie, DNA-PAINT, molekulare Kartierung, Protein-Oligomerisierung, Bildanalyse-Algorithmen