Clear Sky Science · de
Einzelzell‑Multiomik enthüllt eine mechanosensible endothelialen PIEZO1‑IL‑33‑Achse, die Lungenfibrose antreibt
Warum steife Lungen wichtig sind
Lungenfibrose ist eine verheerende Lungenerkrankung, bei der einst elastische Lungenbläschen allmählich in steifes Narbengewebe verwandelt werden, sodass jeder Atemzug zur Anstrengung wird. Ärztinnen und Ärzte können die Krankheit derzeit nur verlangsamen, nicht aufhalten oder umkehren. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Wie spüren die Zellen, die die Blutgefäße in der Lunge auskleiden, dass das umliegende Gewebe ungewöhnlich steif geworden ist, und wie wird dieses Empfinden in mehr Narbenbildung umgesetzt? Indem die Forschenden diese Ereigniskette bis auf einzelne Zellen und Gene zurückverfolgen, entdecken sie einen mechanischen „Schalter“ in Blutgefäßen, der potenziell medikamentös angreifbar ist.
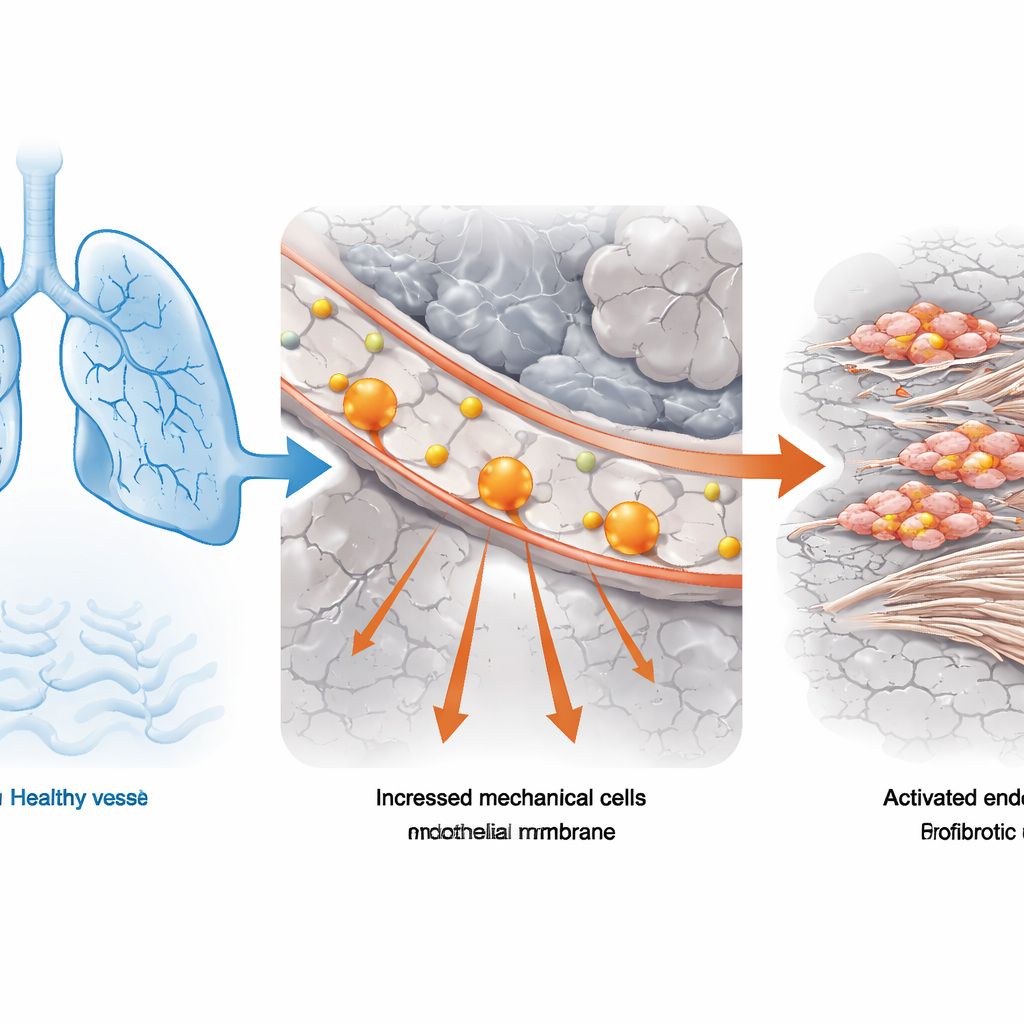
Von Lungenfunktionstests zu Einzelzellen
Das Team begann mit Lungengewebe von Menschen mit idiopathischer Lungenfibrose, der häufigsten Form der Erkrankung, und von Spendern mit normalen Lungen. Sie kombinierten standardisierte Lungenfunktionsmessungen (wie viel Luft eine Person kraftvoll ausatmen kann) mit leistungsfähiger Einzelzell‑RNA‑Sequenzierung, die abliest, welche Gene in tausenden einzelnen Zellen aktiv sind. Mithilfe eines rechnerischen Werkzeugs, das aggregierte klinische Daten mit Einzelzellprofilen verknüpft, identifizierten sie die Zelltypen, die am engsten mit stark eingeschränkter Lungenfunktion assoziiert waren. Vaskuläre Endothelzellen — die Zellen, die die Innenschicht der Blutgefäße bilden — fielen bei Patientinnen und Patienten mit weniger als der Hälfte der normalen Lungenkapazität besonders stark auf. In diesen Endothelzellen waren Genprogramme, die mit „mechanischem Stress“ zusammenhängen, konsequent hochreguliert, was darauf hindeutet, dass abnorme physikalische Kräfte Teil des Problems sind.
Mechanischer Stress als versteckter Treiber
Um zu prüfen, ob der Zusammenhang zwischen Stress‑Wahrnehmung und Krankheit allgemein gilt, wandten sich die Forschenden zwei Mausmodellen der Lungenvernarbung zu: eines ausgelöst durch das Chemotherapeutikum Bleomycin, das andere durch langfristige Exposition gegenüber Silikastaub, ein berufliches Risiko. Mit Einzelzellmethoden auf diesen experimentellen Lungen fanden sie erneut, dass Endothelzellen deutliche Signaturen erhöhten mechanischen Stresses trugen. In beiden Modellen schien die Gefäßinnenhaut in einen maladaptiven Zustand zu wechseln, während sich das umliegende Lungengewebe verdickte und versteifte. Diese Konvergenz zwischen humanen Proben und Tiermodellen stärkt die Idee, dass verzerrte physikalische Kräfte in der Lunge — und nicht nur Entzündung oder Immunaktivität — zentral dafür sind, wie Fibrose entsteht und fortschreitet.
Ein Drucksensor mit entscheidender Rolle
Tiefer gehend suchte das Team nach spezifischen „Mechanosensoren“ — Proteinen, die physische Dehnung in biochemische Signale umwandeln —, die in gestressten Endothelzellen hochreguliert waren. Ein Kanalprotein namens PIEZO1 tauchte wiederholt als Hauptverdächtiger auf. Sowohl bei Mäusen als auch bei Menschen mit Fibrose waren die PIEZO1‑Spiegel in vaskulären Endothelzellen deutlich höher als bei gesunden Kontrollen. Als die Forschenden Mäuse erzeugten, bei denen PIEZO1 nur im Endothel entfernt wurde, waren diese Tiere weitgehend resistent gegen bleomycin‑induzierte Lungenvernarbung: Sie zeigten weniger Kollagenablagerung, weniger aktivierte narbenbildende Zellen und niedrigere Werte eines chemischen Fibrosemarkers. Das pharmakologische Blockieren von PIEZO1 mit einem Peptidinhibitor verringerte ebenfalls die Vernarbung, während dessen Aktivierung die Fibrose verschlimmerte — es sei denn, der Rezeptor fehlte in den Endothelzellen. Zusammengenommen zeigen diese Experimente, dass PIEZO1 in den gefäßauskleidenden Zellen kein bloßer Zuschauer, sondern ein notwendiger Treiber der Erkrankung ist.
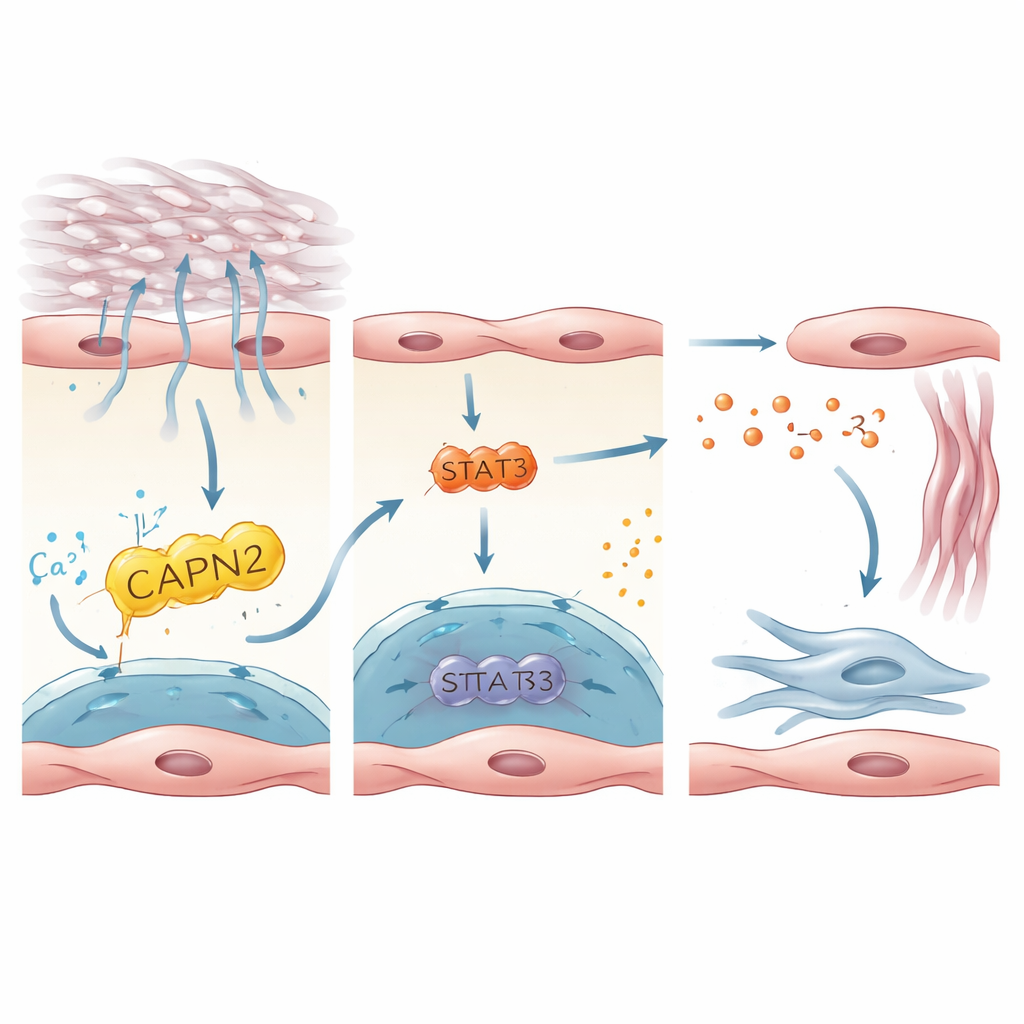
Eine Signalkette, die narbenbildende Zellen weckt
Die Studie verfolgte anschließend, wie die Aktivierung von PIEZO1 in Endothelzellen in Signale übersetzt wird, die Fibroblasten — die Zellen, die Narbengewebe bilden — wecken. Durch Integration menschlicher und Maus‑Datensätze konzentrierten sich die Autorinnen und Autoren auf Interleukin‑33 (IL‑33), ein kleines Protein, das von gestressten oder beschädigten Zellen freigesetzt wird, als Schlüsselbotenstoff. IL‑33 wurde stark in PIEZO1‑positiven Endothelzellen exprimiert und war in Lungen von Patientinnen, Patienten und Mäusen mit Fibrose erhöht. In kultivierten humanen Endothelzellen, die auf starren Substraten wuchsen oder gedehnt wurden, um das Atmen gegen eine steife Lunge zu simulieren, steigerte die Aktivierung von PIEZO1 die IL‑33‑Produktion. Dies hing von einem nachgeschalteten Enzym, CAPN2, und einem Transkriptionsfaktor, STAT3, ab, die zusammen die IL‑33‑Genaktivität regulierten. In Mäusen schützte das gezielte Entfernen von IL‑33 in Endothelzellen vor Fibrose, während das erzwungene Überproduzieren von IL‑33 in Endothelzellen den schützenden Effekt des PIEZO1‑Verlusts aufhob. Diese Ergebnisse skizzieren eine lineare Achse: mechanischer Stress → PIEZO1 → CAPN2/STAT3 → IL‑33 → Aktivierung der Fibroblasten und Narbenbildung.
Was das für zukünftige Therapien bedeutet
Für Nicht‑Spezialistinnen und Nicht‑Spezialisten lautet die Botschaft, dass Lungenfibrose nicht allein von fehlgeleiteten Immunzellen angetrieben wird; sie ist auch eine Erkrankung fehlerhafter „Tastsinne“ in den Blutgefäßen. Endothelzellen registrieren, dass ihre Umgebung zu steif geworden ist, schalten den PIEZO1‑Schalter ein und setzen als Reaktion IL‑33 frei, ein Gefahrensignal, das benachbarte Fibroblasten dazu antreibt, weiter Narbengewebe abzulegen. Indem diese Kette von mechanischer Kraft bis zur Genexpression auseinandergenommen wird, hebt die Arbeit mehrere vielversprechende Angriffspunkte hervor — PIEZO1 selbst, das CAPN2‑STAT3‑Relais und IL‑33 — für Therapien, die darauf abzielen, den sich selbst verstärkenden Kreislauf aus Steifigkeit und Vernarbung zu unterbrechen. Zwar sind weitere Studien nötig, um diese Wege beim Menschen sicher zu modulieren, doch bietet diese mechanosensible endotheliale Achse einen neuen, physikalisch fundierten Ansatz zur Bekämpfung einer Krankheit, die lange Zeit nur schwer wirksam zu behandeln war.
Zitation: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
Schlüsselwörter: Lungenfibrose, Endothelzellen, Mechanotransduktion, PIEZO1, IL-33