Clear Sky Science · de
Einzelzell-Genomik hebt MYC-assoziierte Stoffwechselaktivierung und veränderte Zellinteraktionen bei der Progression der T-Prolymphozytenleukämie hervor
Warum diese langsam verlaufende Leukämie wichtig ist
Die T‑Prolymphozytenleukämie (T‑PLL) ist eine seltene Blutkrebserkrankung, die meist wie ein medizinsches Flächenfeuer auftritt: sie breitet sich schnell aus und ist schwer zu kontrollieren. Bei bis zu einem Viertel der Patienten jedoch glimmt die Krankheit jahrelang ruhig vor sich hin, bevor sie plötzlich in eine aggressive Phase übergeht. Diese Studie stellt eine einfache, aber entscheidende Frage: Welche Veränderungen treten in diesen fehlgeleiteten Immunzellen auf, wenn sie vom ruhigen in einen schnell wachsenden Zustand übergehen? Durch die Verfolgung von Tausenden einzelner Zellen über die Zeit zeigen die Autoren, wie T‑PLL‑Zellen nach und nach stoffwechselseitige „Autarkie“ erlangen und ihre Bindung an die normalen Kontrollmechanismen des Körpers lockern. Diese Einsichten könnten auf neue, präzisere Behandlungsstrategien hinweisen.
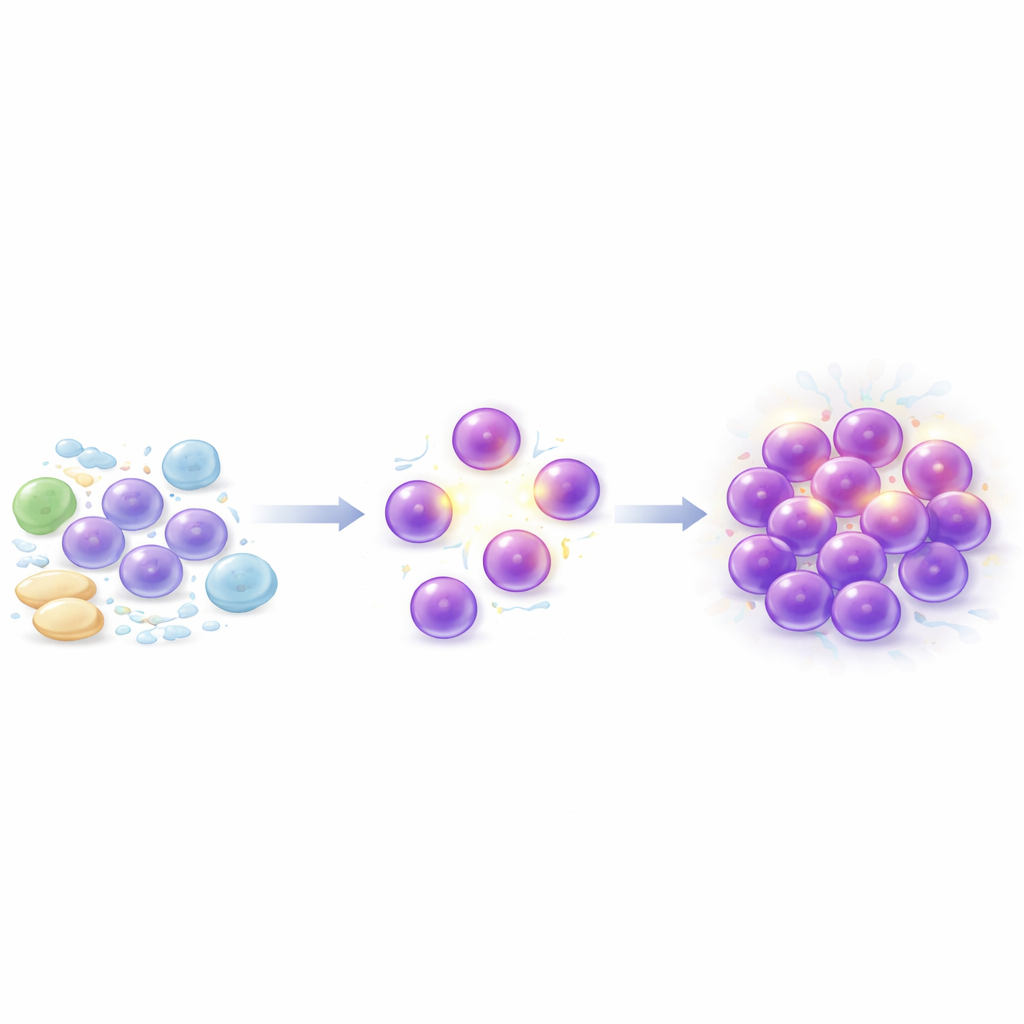
Krebszellen einzeln verfolgen
Die Forschenden sammelten Blutproben von 17 unbehandelten T‑PLL‑Patienten, darunter 11, die über die Zeit von einer frühen, langsamen Phase bis zu einer späteren aggressiven Phase verfolgt wurden. Mit Einzelzell-RNA-Sequenzierung ermittelten sie, welche Gene in mehr als 200.000 einzelnen Zellen aktiv waren, und verglichen diese mit Immunzellen gesunder Spender. Zusätzlich führten sie bei einer Teilmenge von Patienten eine Ganzgenomsequenzierung durch, um zu sehen, welche DNA-Veränderungen mit dem Fortschreiten der Erkrankung auftraten. Diese Kombination erlaubte es ihnen, nicht nur vorhandene genetische Läsionen zu identifizieren, sondern auch zu beobachten, wie sich verschiedene Subgruppen der Leukämiezellen im Zeitverlauf ausdehnten oder zurückgingen und wie die umliegende Immunumgebung reagierte.
Das innere Triebwerk der Zelle aufdrehen
Eine zentrale Entdeckung war, dass aggressive T‑PLL‑Zellen ein von MYC gesteuertes Genprogramm stark hochfuhren — MYC ist ein bekanntes krebsförderndes Gen. Zellen in der aktiven Phase zeigten höhere MYC-Level, mehr Kopien der MYC‑Region in ihrem DNA‑Material und stärkere Aktivität MYC‑regulierter Gene als Zellen in der indolenten Phase oder gesunde T‑Zellen. Diese durch MYC angetriebenen Programme standen in engem Zusammenhang mit Wegen, die das „Triebwerk“ der Zelle antreiben, darunter oxidative Phosphorylierung und Glykolyse, die Hauptwege zur Energiegewinnung. Funktionelle Tests mit einem Stoffwechselanalysator bestätigten, dass Zellen aus der aktiven Phase mehr Sauerstoff verbrauchten und mehr Säure produzierten — Anzeichen gesteigerter Energieproduktion — während Zellen aus der frühen Phase stoffwechselmäßig eingeschränkt blieben und schlecht auf Stimuli reagierten. Zusammengenommen deuten diese Ergebnisse darauf hin, dass T‑PLL‑Zellen mit dem Fortschreiten energetische Begrenzungen überwinden und schnelles Wachstum durch das Hochfahren ihrer inneren Kraftwerke antreiben.
Weniger auf äußere Wachstums‑Signale angewiesen
Gesunde T‑Zellen sind normalerweise auf Signale aus ihrer Umgebung angewiesen — vor allem über den T‑Zell‑Rezeptor, der Antigene erkennt und Wachstum sowie Überleben steuert. In der frühen T‑PLL ist diese Signalkaskade bereits durch bekannte onkogene Treiber gestört, spielt aber dennoch eine wichtige Rolle. Die neuen Daten zeigen, dass viele T‑PLL‑Subklone während der Progression zur aktiven Erkrankung Komponenten der T‑Zell‑Rezeptor‑Maschinerie herunterregulieren und bei experimenteller Stimulation des Rezeptors schwächere Reaktionen zeigen. Wichtige nachgeschaltete Transkriptionsfaktoren werden weniger aktiv, und bei einigen Patienten verlieren Leukämiezellen Moleküle wie CD45 oder reduzieren deren Menge, die beim Abstimmen der Rezeptorsignale helfen. Im Kern entwickeln die Tumorzellen eine geringere Abhängigkeit von externen Überlebenshinweisen und stützen sich stattdessen auf ihren gesteigerten Stoffwechsel und die MYC‑getriebenen Programme.
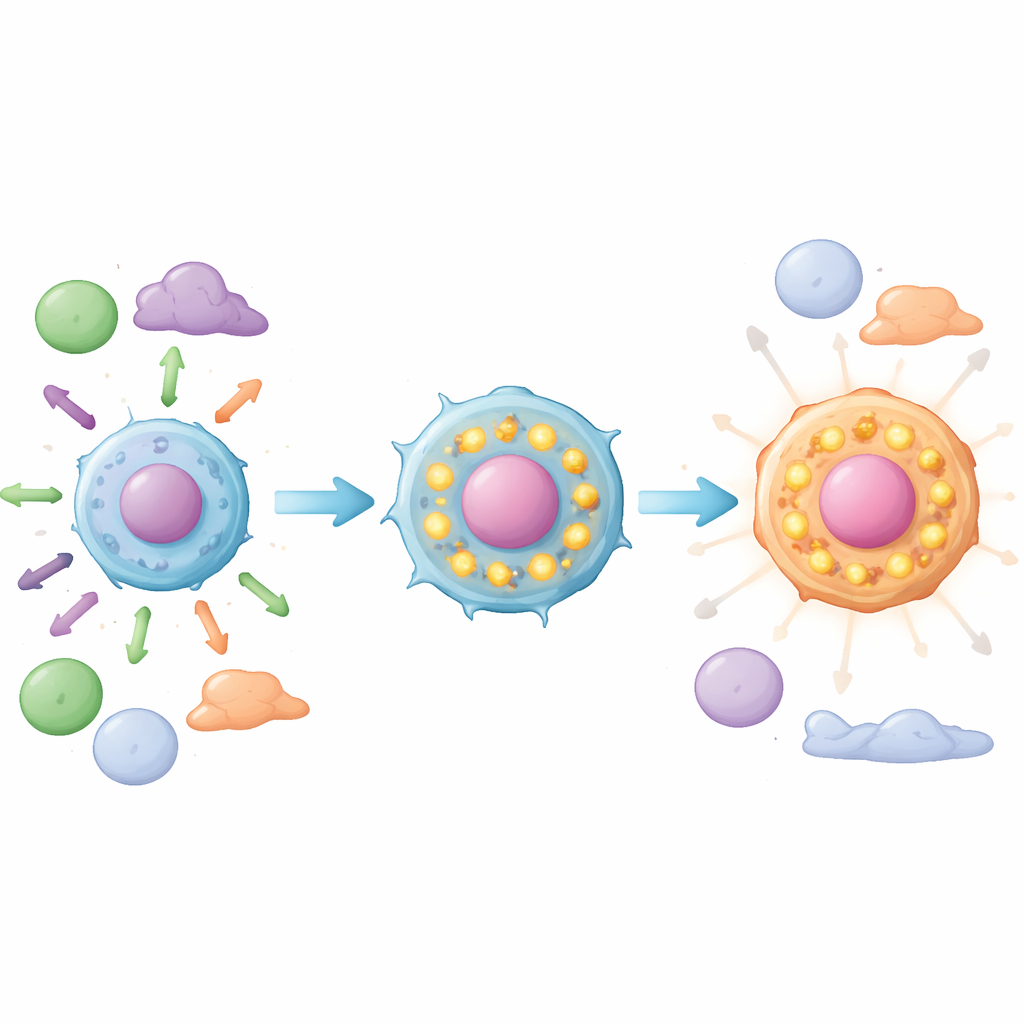
Dem wachsamen Immunumfeld entkommen
Die Studie betrachtet auch nicht‑krebsartige Immunzellen in denselben Blutproben. Wenn T‑PLL in eine aktive Phase übergeht, nehmen Monozyten und bestimmte dendritische Zelltypen zu, doch ihre Genaktivität verändert sich in einer Weise, die auf abgeschwächte Entzündungsreaktionen und veränderte Interferon‑Signalgebung hindeutet. Über mehrere Immunzelltypen hinweg sind Gene, die an Antigenpräsentation und Immunantworten beteiligt sind, gedämpft. Gleichzeitig zeigen rechnerische Modelle zur Zell‑zu‑Zell‑Kommunikation, dass Leukämiezellen in der aggressiven Phase weniger mit den meisten umgebenden Immunzellen interagieren, während spezifische Signale in Richtung Monozyten stärker werden. Moleküle wie Annexin A1 und reduzierte Mengen des Oberflächenproteins CD48 werden als mögliche Faktoren für ein immun‑flüchtiges, tumorförderliches Umfeld hervorgehoben.
Was das für Patienten bedeutet
In der Summe skizzieren die Befunde einen schrittweisen Weg von ruhiger zu aggressiver T‑PLL: Frühe Leukämiezellen werden noch teilweise durch begrenzte Energieversorgung, Abhängigkeit von externen Wachstums‑Signalen und Immunüberwachung in Schach gehalten. Im Laufe der Zeit erhalten Subklone, die MYC amplifizieren, ihre Energieproduktion steigern und ihre Abhängigkeit von äußeren Signalen verringern, einen Selektionsvorteil und dominieren schließlich, was zu einer raschen Ausbreitung der Erkrankung führt. Für Patientinnen und Patienten legt dies nahe, dass Therapien, die MYC‑verwandte Wege, den zellulären Stoffwechsel oder spezifische Tumor‑Immun‑Interaktionen ansprechen, in der aktiven Phase — und möglicherweise bereits früher, bevor die Leukämie diese natürlichen Bremsen vollständig überwindet — besonders wertvoll sein könnten.
Zitation: Wahnschaffe, L., Jungherz, D., Müller, T.A. et al. Single-cell genomics highlight MYC-associated metabolic activation and altered cell interactions in T-prolymphocytic leukemia progression. Nat Commun 17, 2319 (2026). https://doi.org/10.1038/s41467-026-70185-w
Schlüsselwörter: T-Prolymphozytenleukämie, Einzelzell-Genomik, MYC-Signalgebung, Krebsstoffwechsel, Tumormikroumgebung