Clear Sky Science · de
Anpassungen in Plasmodium-Tubulin bestimmen unterschiedliche Mikrotubulus-Architekturen, Mechanik und Wirkstoffempfindlichkeit
Warum das Skelett der Malaria zählt
Malariaparasiten überleben in menschlichen Blutzellen, müssen sich aber auch durch Mücken und verschiedenes Gewebe zwängen. Dafür sind sie auf ein inneres Gerüst aus mikroskopischen Röhren angewiesen, den Mikrotubuli. Diese Studie stellt eine einfache, aber folgenschwere Frage: Wie können die Mikrotubuli des Parasiten so spezialisiert und stabil sein, obwohl ihre Grundbausteine denjenigen in unseren Zellen so ähnlich sehen? Die Antwort offenbart nicht nur, wie der Parasit seine Form bewahrt, sondern auch, wie wir Wirkstoffe entwerfen könnten, die sein Skelett angreifen, ohne das unsere zu schädigen. 
Die winzigen Röhren, die einen tödlichen Parasiten formen
Mikrotubuli sind hohle Proteindruckröhren, die Zellen beim Teilen, Bewegen und bei der Formgebung unterstützen. Sie bestehen aus gepaarten Proteineinheiten, dem Tubulin. Über Tiere, Pflanzen und Parasiten hinweg ist Tubulin überraschend ähnlich, was es schwer macht zu erklären, warum Mikrotubuli in verschiedenen Organismen so unterschiedlich aussehen und sich so verschieden verhalten können. Beim Malariaparasiten Plasmodium falciparum bilden Mikrotubuli vielfältige Anordnungen: Einige sind dynamisch und helfen bei der Zellteilung, andere sind lange, steife Stützen unter der Außenmembran des Parasiten. Da diese Strukturen für Wachstum und Übertragung des Parasiten essentiell sind, sind sie attraktive Ziele für Antimalariamittel — besonders angesichts wachsender Resistenzen gegen bestehende Behandlungen.
Parasiten-Tubulin in atomaren Details sehen
Die Forschenden reinigten Tubulin direkt aus P. falciparum-Parasiten und nutzten hochauflösende Kryo-Elektronenmikroskopie, um zu sehen, wie es sich zu Mikrotubuli zusammenfügt. Sie verglichen diese Strukturen mit den gut untersuchten Mikrotubuli aus Säugerhirn. Auf den ersten Blick wirkt das Parasiten-Tubulin dem menschlichen sehr ähnlich und nimmt dieselbe Grundfaltung an. Sorgfältige Vergleiche zeigten jedoch Gruppen kleiner Sequenzänderungen um Schlüsselstellen — dort, wo energietragende Moleküle (GTP und GDP) binden und wo bestimmte Wirkstoffe ansetzen. Diese subtilen Verschiebungen verändern die Positionierung benachbarter Helices und Schleifen, insbesondere an der Oberfläche des Tubulindimers, wo andere Proteine und Arzneistoffe anhaften. Die Arbeit legt nahe, dass zwar der Gesamtbauplan erhalten bleibt, aber lokale Feinabstimmungen beim Parasiten diese wichtigen Stellen dezent umgestalten.
Steifere Röhren durch stärkere Seiten‑zu‑Seiten‑Verbindungen
Mikrotubuli sind Polymere: Viele Tubulindimere schichten sich längs zu Protofilamenten auf, und mehrere Protofilamente reihen sich seitlich aneinander zur Röhrenwand. Das Team fand, dass bei Parasitenmikrotubuli die longitudinalen Kontakte entlang jedes Protofilaments denjenigen in Hirn-Mikrotubuli sehr ähnlich sind. Der Unterschied zeigt sich in den seitlichen, also lateralen Kontakten zwischen benachbarten Protofilamenten. Obwohl die Kontaktfläche beim Parasiten tatsächlich etwas kleiner ist, zeigen Simulationen, dass diese lateralen Verbindungen insgesamt stärker sind und das Gitter steifer machen. Computermodelle von Bereichen der Mikrotubuluswand zeigten, dass Parasiten-Tubulin sich weniger biegt und weniger verdreht als Hirn-Tubulin. Elektronentomographie echter Mikrotubulusenden bestätigte, dass Parasitenmikrotubuli kürzere, weniger gespreizte Protofilamentkringel aufweisen — ein Kennzeichen für eine stabilere Röhre. 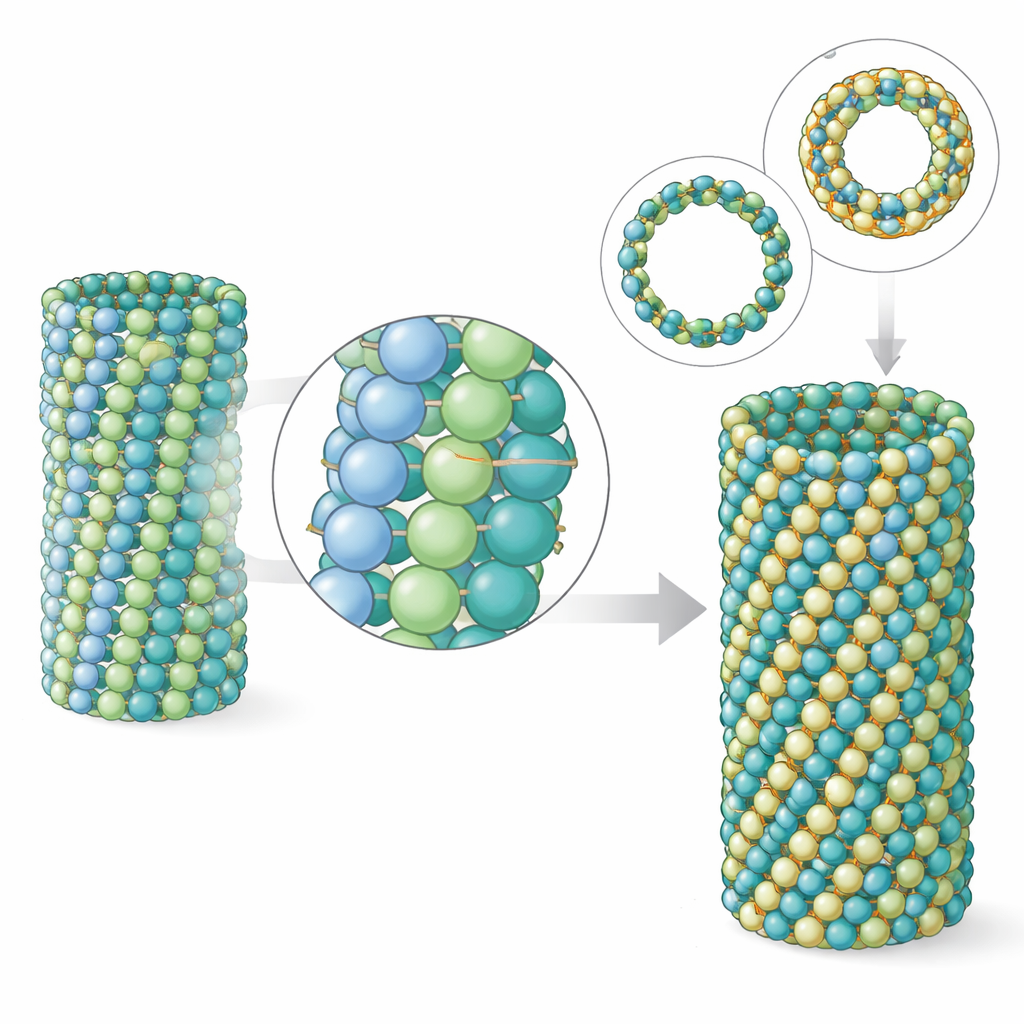
Ungewöhnliche Rohrgrößen, die zum Parasiten passen
Ein weiteres auffälliges Merkmal von P. falciparum ist, dass in manchen Lebensstadien seine Mikrotubuli mehr Bausteine um den Umfang enthalten als die üblichen 13, die in den meisten Tierzellen vorkommen — häufig 15 oder sogar 17 Protofilamentreihen. Das Team rekonstruierte dieses Verhalten im Reagenzglas, indem es das während der Assemblierung verwendete Nukleotid variierte. Mit einem GTP-ähnlichen Molekül, das den wachstumsstabilen Zustand unterstützt, bevorzugte Parasiten-Tubulin natürlich 15-Protofilament-Mikrotubuli. Die Autorinnen und Autoren lösten die Struktur dieser dickeren Röhren und zeigten, wie sie die zusätzlichen Protofilamente durch eine leichte Schräglage des Gitters aufnehmen und dennoch nahezu perfekt zylindrisch bleiben. Der Vergleich dieser im Labor gezüchteten 15-Protofilament-Röhren mit denen aus Parasitenzellen offenbarte eine bemerkenswert enge Übereinstimmung in Form und Abmessungen, was darauf hinweist, dass intrinsische Eigenschaften des Tubulins selbst — und nicht eine Vielzahl von Helferproteinen — ausreichen, um die charakteristischen Architekturen des Parasiten zu erzeugen.
Hinweise für zukünftige, parasitenspezifische Wirkstoffe
Die Schlussfolgerung der Studie lautet, dass die Evolution das Tubulin des Parasiten durch kleine, verstreute Sequenzänderungen feinabgestimmt hat, die zusammen Mikrotubulus-Mechanik, Architektur und Wirkstoffempfindlichkeit verändern. Diese Modifikationen machen die Mikrotubuli des Parasiten steifer und ermöglichen die Bildung nichtstandardmäßiger Rohrgrößen, die zu seinem anspruchsvollen Lebenszyklus passen, während das grundlegende Tubulin-Design weiterhin erkennbar bleibt. Wichtiger für die Medizin ist, dass manche Wirkstoffbindestellen zwischen Parasit und Wirt nahezu identisch erscheinen (wie beim Krebsmedikament Paclitaxel) und daher wenig geeignet sind für selektive Antimalariamittel. Andere Stellen, etwa die Region, die vermutlich an das herbizidähnliche Oryzalin bindet, zeigen sowohl Sequenzverschiebungen als auch subtile strukturelle Verlagerungen, die erklären könnten, warum Parasitenmikrotubuli dort anfälliger sind als menschliche. Das kartieren dieser nuancierten Unterschiede liefert eine Roadmap für das Design künftiger Wirkstoffe, die das Skelett des Malariaparasiten stören, während unsere Zellen größtenteils verschont bleiben.
Zitation: Bangera, M., Wu, J., Beckett, D. et al. Adaptations in Plasmodium tubulin determine distinct microtubule architectures, mechanics and drug susceptibility. Nat Commun 17, 2275 (2026). https://doi.org/10.1038/s41467-026-70181-0
Schlüsselwörter: Malaria-Parasit, Mikrotubuli, Tubulinstruktur, Wirkstoffziel, Cryo-Elektronenmikroskopie