Clear Sky Science · de
Die Ausbildung eines kovalenten Wirkstücks in der Fostriecin-Biosynthese umfasst Malonylierung‑Lactonisierung durch eine bifunktionelle Thioesterase und enzymatische Demalonylierung
Wie die Natur ein winziges chemisches Wirkstück baut
Krebsmedikamente und Antibiotika beruhen oft auf wenigen Atomen, die genau so angeordnet sind – ein winziges „Wirkstück“, das an ein Protein anklammert und es ausschaltet. Die natürliche Verbindung Fostriecin ist ein solches Molekül und zeigt starke Aktivität gegen Enzyme, die am Zellwachstum beteiligt sind. Ihre komplexe Struktur erschwert jedoch die Herstellung oder Modifikation im Labor. Diese Studie legt Schritt für Schritt offen, wie Bakterien das entscheidende Wirkstück von Fostriecin zusammensetzen und offenbart dabei enzymatische Tricks, die Chemiker nun nutzen können, um neue Wirkstoffe zu entwerfen.
Der besondere Haken in potenten Naturstoffen
Viele vielversprechende Wirkstoffe aus Bodenbakterien gehören zur Familie der Polyketide. Innerhalb dieser Familie trägt eine Untergruppe einen reaktiven Ring, den Chemiker als α,β‑ungesättigte δ‑Lactonstruktur bezeichnen – er wirkt wie ein molekularer Fischhaken. Er kann eine dauerhafte Bindung an bestimmte Aminosäuren in Proteinen eingehen und so zentrale biologische Schalter ausschalten. Bei Fostriecin und verwandten Molekülen ist dieser Haken mit einer Phosphatgruppe kombiniert, die ihnen hilft, gezielt bestimmte Enzyme zu erreichen, die die Zellteilung steuern. Diese Eigenschaften machen sie zu attraktiven Wirkstoffkandidaten gegen Krebs, doch dieselbe Reaktivität und strukturelle Komplexität erschweren die Synthese und machen sie während der Lagerung instabil.
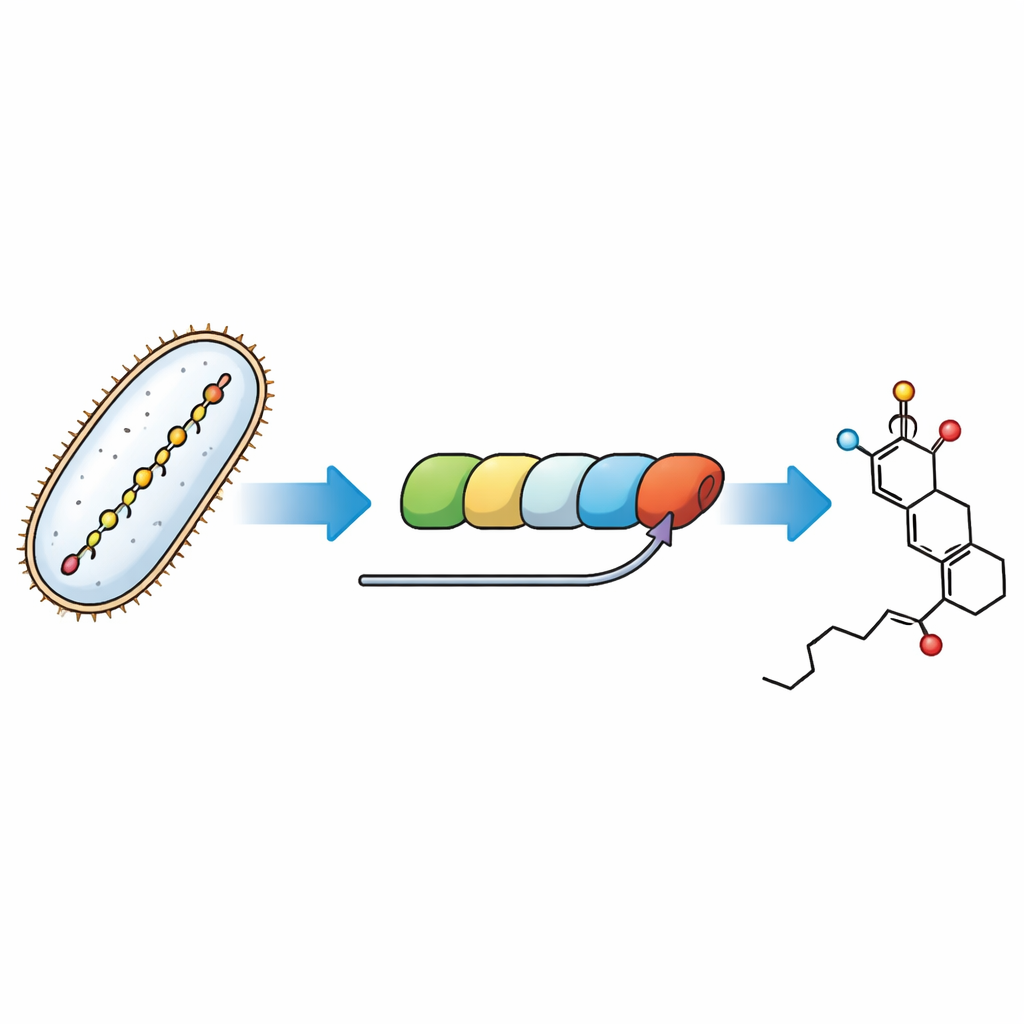
Die letzten Schritte einer molekularen Produktionsstraße verfolgen
Bakterien bauen Fostriecin mithilfe einer riesigen modularen Proteinfabrik auf, einer Polyketidsynthase – einer Produktionsstraße, in der jede Station eine wachsende Kohlenstoffkette verlängert und formt. Das hier behandelte Rätsel ist, wie das letzte Modul dieser Maschine den Wirkstück‑Ring schmiedet und eine temporäre „Schlaufe“ namens Malonylgruppe anbringt, die später wieder entfernt werden muss. Durch die Rekonstruktion des Weges in Reagenzgläsern mit gereinigten Enzymen und gezielt entworfenen kleinmolekularen Stellvertretern der natürlichen Zwischenprodukte konnten die Forschenden einzelne Schritte beobachten und sie bestimmten Teilen der Produktionsstraße zuordnen.
Ein multitaskingfähiges Enzym mit unerwartetem Talent
Das Team entdeckte, dass die letzte Station der Produktionsstraße, eine Domäne namens FosTE, sich ungewöhnlich verhält. Übliche Varianten dieser Domäne schneiden fertige Produkte einfach von der Produktionsstraße ab. FosTE hingegen nimmt zunächst ein Malonylfragment von einem häufigen zellulären Baustein auf und überträgt es auf eine bestimmte Sauerstoffstelle der wachsenden Kette, und unterstützt dann das Umschlagen der Kette zur Schließung des Wirkstück‑Rings. Die Mutation einer einzelnen reaktiven Serin‑Aminosäure in FosTE schaltet beide Aktivitäten aus. Strukturmodellierung weist auf zwei positiv geladene Argininreste im aktiven Zentrum hin, die das Malonylfragment halten und für die Übertragung positionieren – Funktionen, die normalerweise von einem anderen Enzymtyp übernommen werden. Der Austausch dieser Arginine gegen neutrale Reste eliminiert den Malonyl‑Transfer, während die grundsätzliche Ringbildung weitgehend unangetastet bleibt, was ihre kritische Rolle bestätigt.
Das Wirkstück fixieren und Verschwendung verhindern
Sobald der Ring gebildet ist und seine temporäre Malonylgruppe trägt, muss ein anderes Enzym, FosM, diese Gruppe entfernen, um das vollständig bewaffnete Wirkstück freizulegen. Die Studie zeigt, dass FosM nur effizient arbeitet, nachdem ein weiteres Enzym, eine breit spezifische Kinase namens FosH, an einer benachbarten Position des Moleküls ein Phosphat angefügt hat. Wenn die Forschenden den malonylierten Ring allein FosM anboten, erfolgte nur eine mäßige Umwandlung. Fügte man zuvor FosH hinzu, führte dies zur nahezu vollständigen Entfernung der Malonylgruppe und zur Entstehung der finalen reaktiven Einheit. Wichtig ist, dass FosH auch verwandte „Nebenweg“-Zwischenprodukte phosphorylieren kann, die durch Seitenreaktionen entstehen, und diese dadurch rettet, sodass sie korrekt weiterverarbeitet werden können, anstatt als Sackgassen verloren zu gehen.
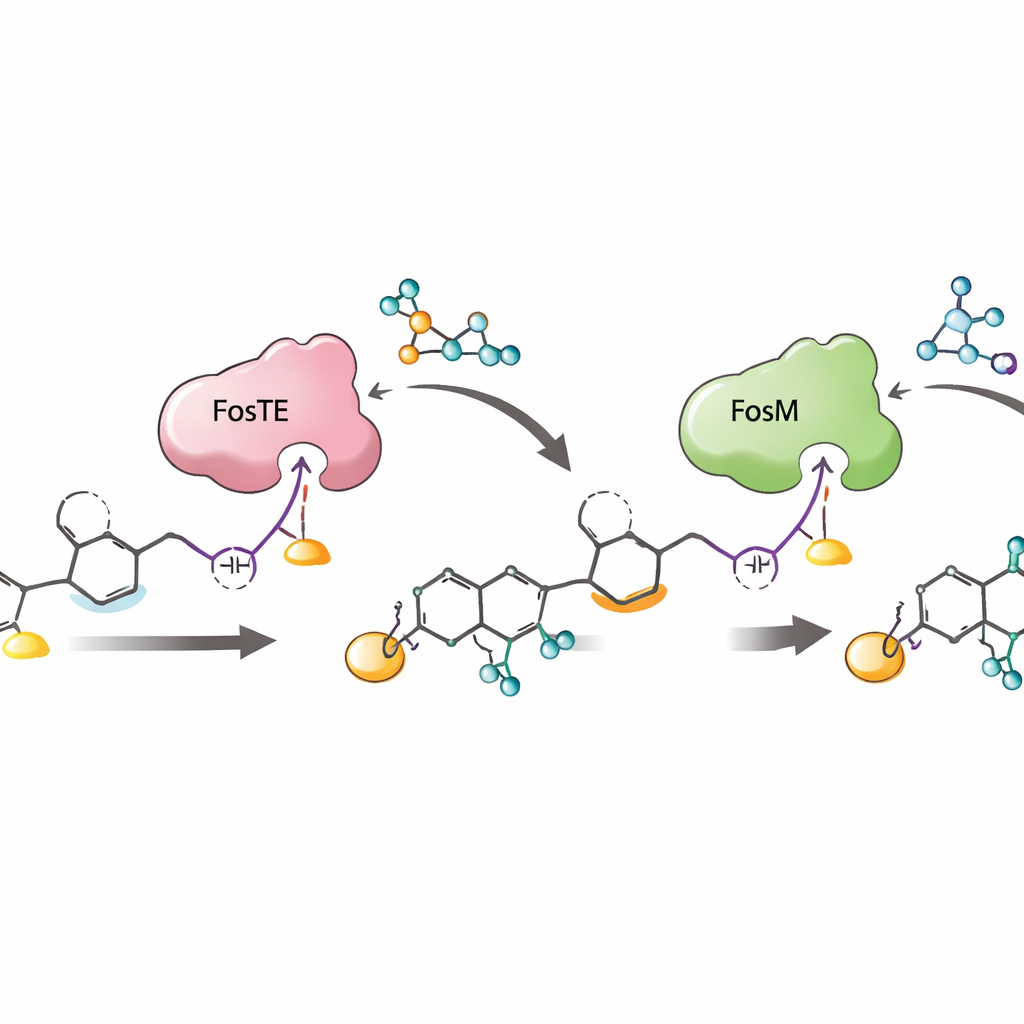
Warum diese enzymatische Choreographie wichtig ist
In der Summe zeigt die Arbeit eine eng abgestimmte Abfolge: Kettenverlängerung an der Produktionsstraße, FosTE‑vermittelte Malonylanfügung und Ringverschluss, FosH‑Phosphorylierung und schließlich FosM‑vermittelte Demalonylierung. Diese Reihenfolge baut das empfindliche Wirkstück nicht nur effizient auf, sie schützt auch instabile Zwischenprodukte davor, sich zu zersetzen, und maximiert die Produktion der gewünschten, phosphorylierten Form, die als Wirkstoffkandidat am aktivsten ist. Indem die Studie offenlegt, wie eine einzelne Enzymdomäne sowohl ein wachsendes Molekül dekorieren als auch freisetzen kann – und wie Partnerenzyme reaktive Zwischenprodukte feinjustieren und retten – liefert sie eine Blaupause, um neue Polyketide mit Wirkstücken zu konstruieren und kürzere, effizientere Syntheserouten zu komplexen Krebswirkstoffen wie Fostriecin zu entwickeln.
Zitation: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
Schlüsselwörter: fostriecin, Polyketid‑Biosynthese, Enzymtechnik, natürliche Wirkstücke, chemoenzymatische Synthese