Clear Sky Science · de
Endotheliales C‑typ‑natriuretisches Peptid/Guanylylcyclase‑B‑Signal verhindert pulmonale arterielle Hypertonie
Warum das für Lunge und Herz wichtig ist
Die pulmonale arterielle Hypertonie ist eine seltene, aber tödliche Erkrankung, bei der die Blutgefäße, die das Blut vom Herzen zur Lunge führen, gefährlich eng und verdickt werden. Diese Belastung kann zu Rechtsherzinsuffizienz und schließlich zum Tod führen. Die derzeit verfügbaren Medikamente weiten hauptsächlich diese Gefäße, leisten aber wenig, um den zugrunde liegenden Schaden an der Gefäßwand zu stoppen. Die hier beschriebene Studie enthüllt ein natürliches Schutzsignal, das von den Zellen ausgeht, die die Lungenblutgefäße auskleiden, und zeigt, wie die Verstärkung dieses Signals sowohl die Krankheit verhindern als auch behandeln könnte.
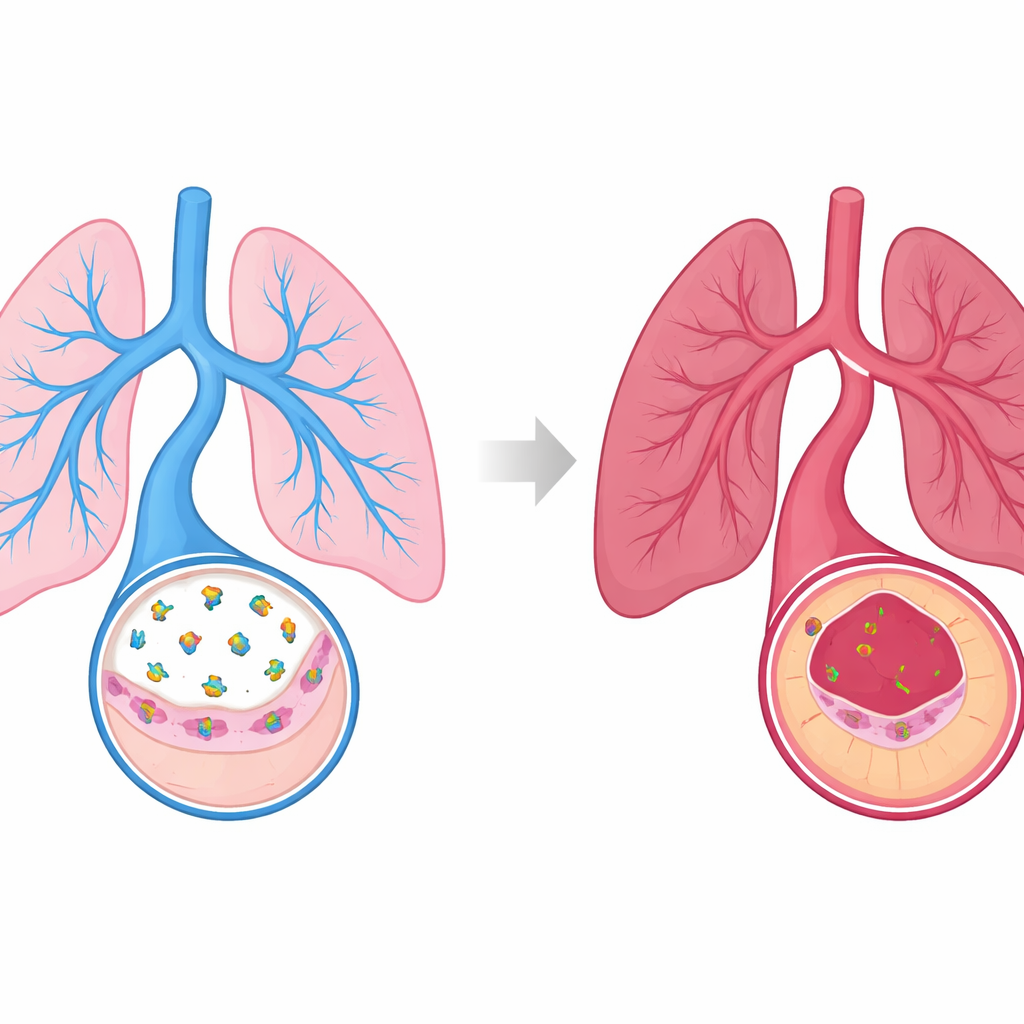
Eine schützende Botschaft aus der Gefäßauskleidung
Die innere Auskleidung der Blutgefäße besteht aus Endothelzellen, die fortwährend mit der umgebenden Muskelschicht kommunizieren, um Gefäße offen und gesund zu halten. Die Autoren konzentrierten sich auf ein kleines Hormon, das C‑typ‑natriuretische Peptid (CNP), das diese Endothelzellen in der Lunge freisetzen. CNP wirkt lokal auf ein Rezeptorprotein namens Guanylylcyclase‑B auf denselben Zellen und löst einen chemischen Botenstoff aus, der hilft, die Gefäße zu entspannen und vor Schäden zu schützen. Anhand von Mäusen, die zwei verschiedenen Auslösern pulmonaler Hypertonie ausgesetzt waren — einer giftigen Chemikalie und sauerstoffarmer Luft — fanden die Forschenden heraus, dass in erkrankten Lungen die Mengen sowohl an CNP als auch an seinem Rezeptor deutlich niedriger waren als in gesunden Lungen.
Das Abschalten des Signals verschlechtert die Erkrankung bei Tieren
Um zu prüfen, ob der Verlust der CNP‑Signalübertragung tatsächlich die Erkrankung antreibt, erzeugte das Team Mäuse, bei denen entweder CNP selbst oder sein Rezeptor GC‑B nur in Endothelzellen entfernt wurde. Wurden diese Mäuse den gleichen Krankheitsauslösern ausgesetzt, verengten sich ihre Lungenarterien stärker, der Druck in der rechten Herzhälfte stieg höher und die Herzmuskelwand verdickte sich mehr als bei normalen Mäusen. Im Gegensatz dazu verschlechterte das Entfernen des Rezeptors nur in den umgebenden glatten Muskelzellen die Erkrankung nicht. Das identifizierte die entscheidende Rolle von CNP, das auf Endothelzellen selbst wirkt, statt direkt auf die Muskelschicht.
Wie das Signal die Gefäßwand beruhigt
Bei näherer Untersuchung entdeckten die Forschenden, dass der CNP–GC‑B‑Weg in Endothelzellen als Bremse für mehrere schädliche Reaktionen dient. Ohne ihn produzierten diese Zellen mehr Endothelin‑1, ein stark gefäßverengendes Molekül, sowie höhere Mengen an entzündungsfördernden Botenstoffen wie Interleukin‑6, CCL2 und TGF‑β1. In Zellkulturexperimenten dämpfte die Wiederherstellung von CNP diese Signale, allerdings nur, wenn der GC‑B‑Rezeptor vorhanden war. CNP trug außerdem dazu bei, zwei konkurrierende wachstumsregulierende Systeme innerhalb der Zellen — bekannt als SMAD2/3 und SMAD1/5/9 — wieder ins Gleichgewicht zu bringen, die gemeinsam entscheiden, ob die Gefäßwand stabil bleibt oder dicker wird. Wenn die CNP‑Signalübertragung intakt war, blieben Gene aktiv, die mit gesunden, nicht überwachsenen Arterien verbunden sind; war sie nicht vorhanden, verschob sich das Gleichgewicht hin zu Überwuchs und Vernarbung.
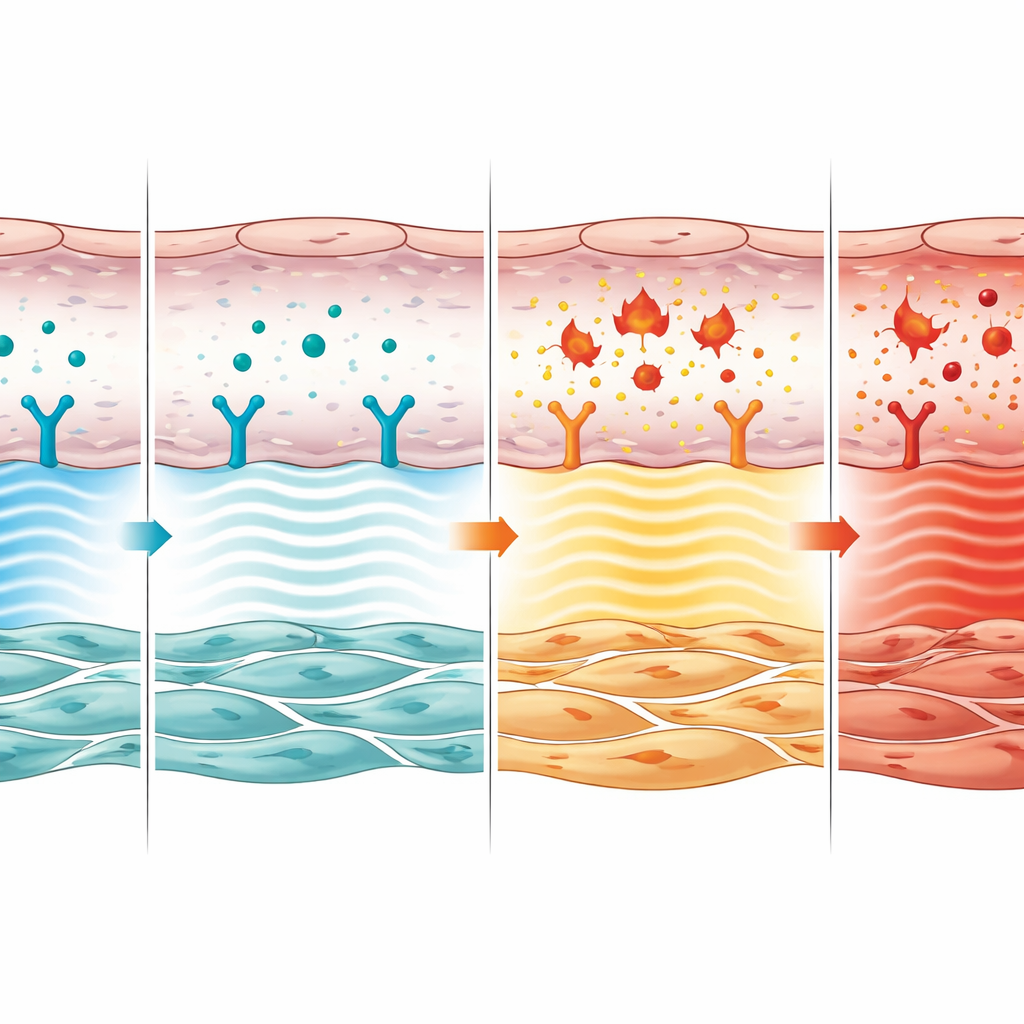
Von der Zellkommunikation zur Gefäßremodellierung
Das Team untersuchte dann, wie dieses endotheliale Signal die benachbarten glatten Muskelzellen beeinflusst, die tatsächlich die Gefäßwand verdicken. Sie zeigten, dass chemische Signale, die von gesunden, CNP‑ansprechenden Endothelzellen freigesetzt werden, das Wachstum und die Migration glatter Muskelzellen im Labor verlangsamen. Wurde der CNP‑Rezeptor aus Endothelzellen entfernt, förderten diese Signale stattdessen die Vermehrung und Bewegung glatter Muskelzellen und ahmten so die bei der Erkrankung beobachtete Gefäßwand‑Remodellierung nach. In den Lungen von Mäusen enthielten Arterien ohne endotheliales CNP‑Signal mehr teilende und weniger sterbende glatte Muskelzellen, was bestätigte, dass dieser Weg normalerweise den Überwuchs, der den Blutfluss abschnürt, zurückhält.
Test eines arzneimittelähnlichen CNP in schweren Modellen
Ermutigt durch diese Befunde testeten die Autoren eine länger wirkende Form von CNP, genannt CNP‑53, die kontinuierlich mittels winziger Pumpen bei Nagetieren verabreicht wurde. Bei Mäusen verhinderte die Gabe von CNP‑53 während der Exposition gegenüber Krankheitsauslösern den Anstieg des Lungenblutdrucks und die Verdickung der Gefäßwand — jedoch nur, wenn Endothelzellen noch den GC‑B‑Rezeptor trugen. In Ratten und Mäusen mit einer besonders schweren, dem Menschen ähnlichen Form pulmonaler Hypertonie verringerte der Beginn der CNP‑53‑Behandlung nach Etablierung der Erkrankung den Lungenblutdruck und verbesserte Herzparameter. In Kombination mit zwei bereits verfügbaren Medikamenten — einem Endothelin‑Blocker und einem Wirkstoff, der einen verwandten Wachstumsweg anvisiert — brachte CNP‑53 zusätzlichen Nutzen, ohne den normalen Blutdruck zu senken.
Was das für künftige Therapien bedeutet
Insgesamt zeigt die Studie, dass ein natürliches Hormon der Lungengefäßauskleidung als Wächter gegen pulmonale arterielle Hypertonie wirkt. Wenn das CNP–GC‑B‑Signal reduziert ist, geraten Entzündung, gefäßverengende Substanzen und Wachstumswege außer Kontrolle, wodurch die Arterienwand dicker wird und das Herz überlastet. Die Wiederherstellung oder Verstärkung dieses Signals mit CNP‑basierten Medikamenten, insbesondere Varianten, die im Körper länger wirksam sind, könnte einen neuen Behandlungsansatz eröffnen, der den Krankheitsprozess selbst angreift, statt nur die Gefäße zu erweitern. Obwohl weitere Arbeit nötig ist, um diese Ergebnisse in menschliche Therapien zu übertragen, deuten die Befunde darauf hin, dass das richtige Zusammenspiel der Gefäßauskleidung entscheidend sein könnte, um Patienten mit dieser verheerenden Lungen‑Herz‑Erkrankung zu schützen.
Zitation: Yanagisawa, H., Kuwahara, K., Nakagawa, Y. et al. Endothelial C-type natriuretic peptide/guanylyl cyclase-B signaling prevents pulmonary arterial hypertension. Nat Commun 17, 2331 (2026). https://doi.org/10.1038/s41467-026-70139-2
Schlüsselwörter: pulmonale arterielle Hypertonie, endotheliales Signal, C‑typ‑natriuretisches Peptid, gefäßremodellierung, Lungenkreislauf